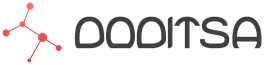साइट अनुभाग
संपादक की पसंद:
- नाखूनों पर सफेद धब्बे, क्या करें, नाखूनों पर सफेद धब्बे और लोक लक्षण
- तेजी से बढ़ते रक्त ल्यूकोसाइट्स के लिए उपलब्ध तरीके
- नाखून और त्वचा के कवक कॉफी के मैदान का विरोध नहीं करेंगे
- क्रोकस फर्नीचर प्रदर्शनी। फर्नीचर प्रदर्शनियों
- भुजा मूल्य पर उल्लू का टैटू
- दुनिया में सबसे बड़े सदस्य हैं
- फोटो के पैर की उंगलियों के फंगल का फ्रैक्चर
- "बुरा" और "अच्छा" कोलेस्ट्रॉल क्या है
- नाखूनों के आसपास की त्वचा सूख जाए तो क्या करें
- सबसे सुरक्षित प्राकृतिक वार्निश सूची
विज्ञापन
| भड़काऊ प्रतिक्रिया की रोगजनक भूमिका। भड़काऊ मध्यस्थ: वर्गीकरण |
|
एक रोगविज्ञानी कारक की कार्रवाई के जवाब में भड़काऊ प्रक्रियाओं की उपस्थिति शरीर की पर्याप्त प्रतिक्रिया है। सूजन एक जटिल प्रक्रिया है जो स्थानीय या सामान्य स्तर पर विकसित होती है, जो विदेशी एजेंटों की कार्रवाई के जवाब में उत्पन्न होती है। विकास का मुख्य कार्य भड़काऊ प्रतिक्रिया इसका उद्देश्य पैथोलॉजिकल प्रभावों को खत्म करना और शरीर को बहाल करना है। भड़काऊ मध्यस्थ मध्यस्थ सीधे इन प्रक्रियाओं में शामिल होते हैं। भड़काऊ प्रतिक्रियाओं के सिद्धांतों के बारे में संक्षेप मेंप्रतिरक्षा प्रणाली मानव स्वास्थ्य का संरक्षक है। जब आवश्यक हो, यह लड़ाई में प्रवेश करता है और बैक्टीरिया, वायरस, कवक को नष्ट करता है। हालांकि, काम की तीव्रता में वृद्धि के साथ, सूक्ष्मजीवों का मुकाबला करने की प्रक्रिया को नेत्रहीन रूप से देखा जा सकता है या नैदानिक तस्वीर की उपस्थिति महसूस कर सकता है। यह ऐसे मामलों में है कि सूजन शरीर की सुरक्षात्मक प्रतिक्रिया के रूप में विकसित होती है। भड़काऊ प्रतिक्रिया और इसके क्रोनिक कोर्स की एक तीव्र प्रक्रिया है। पहला एक अड़चन (आघात, चोट, एलर्जी प्रभाव, संक्रमण) की अचानक कार्रवाई के परिणामस्वरूप होता है। पुरानी सूजन में एक विकृत प्रकृति और कम स्पष्ट नैदानिक संकेत हैं। चोट या चोट के क्षेत्र में प्रतिरक्षा प्रणाली की स्थानीय प्रतिक्रिया के मामले में, एक भड़काऊ प्रतिक्रिया के निम्नलिखित लक्षण दिखाई देते हैं:
सूजन के विकास का चरणसूजन की प्रक्रिया त्वचा, रक्त और प्रतिरक्षा कोशिकाओं के सुरक्षात्मक कारकों की एक साथ बातचीत पर आधारित है। एक विदेशी एजेंट के संपर्क के तुरंत बाद, शरीर सीधे आघात के क्षेत्र में रक्त वाहिकाओं के स्थानीय विस्तार के साथ प्रतिक्रिया करता है। उनकी दीवारों की पारगम्यता में वृद्धि हुई है और स्थानीय microcirculation में वृद्धि हुई है। साथ में हास्य सुरक्षा के रक्त प्रवाह कोशिकाएं यहां आती हैं। दूसरे चरण में, प्रतिरक्षा कोशिकाएं सूक्ष्मजीवों के खिलाफ लड़ाई शुरू करती हैं जो चोट के स्थान पर होती हैं। फागोसाइटोसिस नामक प्रक्रिया शुरू होती है। न्यूट्रोफिल कोशिकाएं अपना आकार बदलती हैं और पैथोलॉजिकल एजेंटों को अवशोषित करती हैं। अगला, बैक्टीरिया और वायरस के विनाश के उद्देश्य से विशेष पदार्थ हैं। सूक्ष्मजीवों के समानांतर में, न्यूट्रोफिल सूजन के क्षेत्र में स्थित पुरानी मृत कोशिकाओं को नष्ट कर देते हैं। इस प्रकार, जीव की प्रतिक्रिया के तीसरे चरण का विकास शुरू होता है। सूजन का फोकस जैसे कि पूरे शरीर से सुरक्षित हो। कभी-कभी इस जगह में एक धड़कन महसूस की जा सकती है। सेलुलर भड़काऊ मध्यस्थों का उत्पादन शुरू होता है। मस्तूल कोशिकाएँयह आपको विषाक्त पदार्थों, स्लैग और अन्य पदार्थों से घायल क्षेत्र को साफ करने की अनुमति देता है।
मध्यस्थों के बारे में सामान्य अवधारणाएँभड़काऊ मध्यस्थ जैविक मूल के सक्रिय पदार्थ हैं, जिनमें से रिलीज परिवर्तन के मुख्य चरणों के साथ होता है। वे भड़काऊ प्रतिक्रियाओं की घटना के लिए जिम्मेदार हैं। उदाहरण के लिए, पोत की दीवारों की वृद्धि हुई पारगम्यता या आघात के क्षेत्र में तापमान में स्थानीय वृद्धि। मुख्य भड़काऊ मध्यस्थ न केवल रोग प्रक्रिया के विकास के साथ बाहर खड़े होते हैं। उनका उत्पादन लगातार होता है। इसका उद्देश्य ऊतक और सेलुलर स्तरों पर शरीर के कार्यों को विनियमित करना है। कार्रवाई की दिशा के आधार पर, न्यूनाधिक प्रभाव होता है:
क्षति की उपस्थिति के साथ या सूक्ष्मजीवों की कार्रवाई के स्थान पर, मध्यस्थ लिंक भड़काऊ प्रभावकारों की बातचीत और प्रक्रिया के विशिष्ट चरणों के परिवर्तन को नियंत्रित करता है। भड़काऊ मध्यस्थों के प्रकारसभी भड़काऊ मॉड्यूलों को उनके मूल के आधार पर दो बड़े समूहों में विभाजित किया जाता है:
पैथोलॉजिकल फैक्टर के संपर्क में आने से पहले ह्यूमर भड़काऊ मध्यस्थ मानव शरीर में होते हैं, यानी शरीर को इन पदार्थों की आपूर्ति होती है। उनका निरूपण एक निष्क्रिय रूप में कोशिकाओं में होता है। वासोएक्टिव एमाइन, न्यूरोपेप्टाइड, और लाइसोसोमल कारक भी प्रीसिस्टिंग मोडुलेटर हैं। सेलुलर मध्यस्थों के समूह से संबंधित शेष पदार्थ सीधे भड़काऊ प्रतिक्रिया के विकास के दौरान उत्पन्न होते हैं।
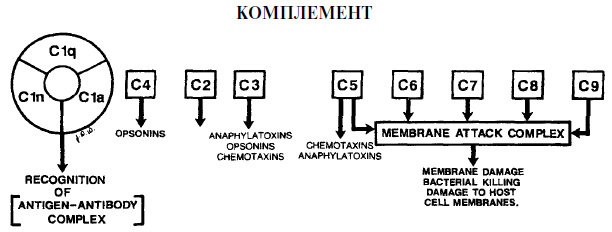
पूरक व्युत्पन्नसूजन के मध्यस्थ तारीफ के डेरिवेटिव हैं। जैविक रूप से सक्रिय पदार्थों के इस समूह को विनोदी न्यूनाधिक के बीच सबसे महत्वपूर्ण माना जाता है। डेरिवेटिव्स में 22 अलग-अलग प्रोटीन शामिल होते हैं, जिसका गठन तब होता है जब पूरक सक्रिय होता है (प्रतिरक्षा जटिल या इम्युनोग्लोबुलिन का गठन)।
मध्यस्थों का यह समूह प्लाज्मा और ऊतक द्रव से उत्पन्न होता है। पैथोलॉजिकल ज़ोन में प्रवेश के कारण, एक्सयूडीशन प्रक्रियाएं होती हैं। पूरक डेरिवेटिव की मदद से, इंटरल्यूकिन, न्यूरोट्रांसमीटर, ल्यूकोट्रिएनेस, प्रोस्टाग्लैंडिंस और प्लेटलेट सक्रिय करने वाले कारक जारी किए जाते हैं। kininsपदार्थों का यह समूह वासोडिलेटर है। वे विशिष्ट ग्लोब्युलिन से ऊतक द्रव और प्लाज्मा में बनते हैं। समूह के मुख्य प्रतिनिधि ब्रैडीकाइनिन और कैलिडिन हैं, जिसका प्रभाव निम्नानुसार प्रकट होता है:
ब्रैडीकिनिन की कार्रवाई सूजन के स्थल तक रक्त प्लाज्मा की पहुंच को खोलने के उद्देश्य से है। किनिन्स सूजन के दर्द के मध्यस्थ हैं। वे स्थानीय रिसेप्टर्स को परेशान करते हैं, जिससे असुविधा होती है, दर्दनाक सनसनीखुजली। prostaglandinsसूजन के सेल मध्यस्थ प्रोस्टाग्लैंडीन हैं। पदार्थों का यह समूह एराकिडोनिक एसिड डेरिवेटिव से संबंधित है। प्रोस्टाग्लैंडिन्स के स्रोत मैक्रोफेज, प्लेटलेट्स, ग्रैनुलोसाइट्स और मोनोसाइट्स हैं।
प्रोस्टाग्लैंडिंस भड़काऊ मध्यस्थ हैं जो निम्नलिखित गतिविधि का प्रदर्शन करते हैं:
leukotrienesनवगठित मध्यस्थों से संबंधित। यही है, शरीर में बाकी प्रतिरक्षा प्रणाली की स्थिति में, उनकी संख्या एक कष्टप्रद कारक की तत्काल प्रतिक्रिया के लिए पर्याप्त नहीं है। ल्यूकोट्रिएन्स ने संवहनी दीवार की पारगम्यता और विकृति विज्ञान के क्षेत्र में सफेद रक्त कोशिकाओं के लिए खुली पहुंच को भड़काया। भड़काऊ दर्द की उत्पत्ति में पदार्थ। लाल रक्त कोशिकाओं को छोड़कर, सभी रक्त कोशिकाओं में पदार्थों को संश्लेषित किया जा सकता है, साथ ही साथ फेफड़े, रक्त वाहिकाओं और मस्तूल कोशिकाओं की कोशिकाओं में भी हो सकता है। विकास के मामले में भड़काऊ प्रक्रिया बैक्टीरिया, वायरस, या एलर्जी कारकों के जवाब में, ल्यूकोट्रिएन्स ब्रोंकोस्पास्म का कारण बनता है, जिससे एडिमा का विकास होता है। प्रभाव हिस्टामाइन की कार्रवाई के समान है, लेकिन लंबे समय तक। सक्रिय पदार्थों के लिए लक्ष्य अंग हृदय है। बड़ी संख्या में बाहर खड़े होकर, वे हृदय की मांसपेशियों पर कार्य करते हैं, कोरोनरी रक्त प्रवाह को धीमा करते हैं और भड़काऊ प्रतिक्रिया के स्तर को बढ़ाते हैं। थ्राम्बाक्सेनोंप्लेटलेट्स में तिल्ली, मस्तिष्क कोशिकाओं, फेफड़े, और रक्त कोशिकाओं के ऊतकों में सक्रिय मॉड्यूलेटर का यह समूह बनता है। वे जहाजों पर एक स्पास्टिक प्रभाव डालते हैं, हृदय इस्किमिया के दौरान घनास्त्रता की प्रक्रियाओं को बढ़ाते हैं, प्लेटलेट्स के एकत्रीकरण और आसंजन की प्रक्रियाओं में योगदान करते हैं। बायोजेनिक अमीनप्राथमिक भड़काऊ मध्यस्थ - हिस्टामाइन और सेरोटोनिन। पैथोलॉजी के क्षेत्र में पदार्थ प्रारंभिक माइक्रोकिरकुलेशन विकारों के उत्तेजक हैं। सेरोटोनिन एक न्यूरोट्रांसमीटर है जो मस्तूल कोशिकाओं, एंटरोक्रोमैसेफिन और प्लेटलेट्स में उत्पन्न होता है। सेरोटोनिन की क्रिया शरीर में अपने स्तर के साथ बदलती है। सामान्य परिस्थितियों में, जब मध्यस्थ की मात्रा शारीरिक होती है, तो यह जहाजों की ऐंठन को बढ़ाता है और उनके स्वर को बढ़ाता है। भड़काऊ प्रतिक्रियाओं के विकास के साथ, संख्या नाटकीय रूप से बढ़ जाती है। सेरोटोनिन वैसोडिलेटर बन जाता है, जिससे संवहनी दीवार की पारगम्यता बढ़ जाती है और रक्त वाहिकाओं का विस्तार होता है। इसके अलावा, इसकी कार्रवाई बायोजेनिक एमाइन के दूसरे न्यूरोट्रांसमीटर से सौ गुना अधिक प्रभावी है।
हिस्टामाइन सूजन का मध्यस्थ है जो रक्त वाहिकाओं और कोशिकाओं पर विविध प्रभाव डालता है। हिस्टामाइन-संवेदनशील रिसेप्टर्स के एक समूह पर कार्य करते हुए, पदार्थ धमनियों को पतला करता है और ल्यूकोसाइट्स के आंदोलन को रोकता है। जब दूसरे के संपर्क में आता है, तो यह नसों को संकरा कर देता है, इंट्रा कैपेलर के दबाव में वृद्धि का कारण बनता है और, इसके विपरीत, ल्यूकोसाइट्स के आंदोलन को उत्तेजित करता है। न्युट्रोफिल रिसेप्टर्स पर कार्य करना, हिस्टामाइन अपनी कार्यक्षमता को सीमित करता है, मोनोसाइट रिसेप्टर्स पर - बाद को उत्तेजित करता है। इस प्रकार, न्यूरोट्रांसमीटर एक साथ एक भड़काऊ विरोधी भड़काऊ प्रभाव हो सकता है। हिस्टामाइन का वैसोडिलेटर प्रभाव एसिटाइलकोलाइन, ब्रैडीकाइनिन और सेरोटोनिन के साथ एक कॉम्प्लेक्स के प्रभाव में बढ़ाया जाता है। लाइसोसोमल एंजाइमइम्यून इंफ्लेमेटरी मध्यस्थों को उत्तेजना, उत्प्रवास, फैगोसाइटोसिस, कोशिका क्षति और मृत्यु के दौरान रोग प्रक्रिया के स्थल पर मोनोसाइट्स और ग्रैनुलोसाइट्स द्वारा निर्मित किया जाता है। प्रोटीन, जो लाइसोसोमल एंजाइमों का मुख्य घटक है, एक रोगाणुरोधी क्रिया है, जो विदेशी रोग संबंधी सूक्ष्मजीवों को प्रभावित करता है। इसके अलावा, सक्रिय पदार्थ संवहनी दीवारों की पारगम्यता बढ़ाने में मदद करते हैं, ल्यूकोसाइट घुसपैठ को नियंत्रित करते हैं। पृथक एंजाइमों की संख्या के आधार पर, वे ल्यूकोसाइट कोशिकाओं के प्रवास को बढ़ा या कमजोर कर सकते हैं। भड़काऊ प्रतिक्रिया विकसित होती है और इस तथ्य के कारण लंबे समय तक बनी रहती है कि लाइसोसोमल एंजाइम पूरक प्रणाली को सक्रिय करते हैं, साइटोकिन्स और लिमोकाइन को छोड़ते हैं, थक्के और फाइब्रिनोलिसिस को सक्रिय करते हैं।
Cationic प्रोटीनभड़काऊ मध्यस्थों में न्युट्रोफिल कणिकाओं में निहित प्रोटीन और उच्च माइक्रोबिसाइड शामिल हैं। ये पदार्थ विदेशी कोशिका पर सीधे कार्य करते हैं, इसकी संरचनात्मक झिल्ली को तोड़ते हैं। यह पैथोलॉजिकल एजेंट की मृत्यु का कारण बनता है। अगला, लाइसोसोमल प्रोटीन द्वारा विनाश और दरार की प्रक्रिया। Cationic प्रोटीन न्यूरोट्रांसमीटर हिस्टामाइन की रिहाई को बढ़ावा देते हैं, संवहनी पारगम्यता को बढ़ाते हैं, ल्यूकोसाइट कोशिकाओं के आसंजन और प्रवास को तेज करते हैं। साइटोकिन्सये निम्नलिखित कोशिकाओं द्वारा निर्मित सूजन के सेलुलर मध्यस्थ हैं:
न्युट्रोफिल पर कार्य करना, साइटोकिन्स संवहनी दीवार की पारगम्यता को बढ़ाता है। वे विदेशी उपनिवेशी सूक्ष्मजीवों को मारने, अवशोषित करने और नष्ट करने के लिए ल्यूकोसाइट कोशिकाओं को उत्तेजित करते हैं और फागोसाइटोसिस की प्रक्रिया को बढ़ाते हैं। पैथोलॉजिकल एजेंटों को मारने के बाद, साइटोकिन्स नई कोशिकाओं के पुनर्जनन और प्रसार को उत्तेजित करते हैं। पदार्थ मध्यस्थों, प्रोस्टाग्लैंडिंस, न्यूरोपैप्टाइड्स के अपने समूह के प्रतिनिधियों के साथ बातचीत करते हैं। ऑक्सीजन के सक्रिय चयापचयोंमुक्त कणों का एक समूह जो अप्रकाशित इलेक्ट्रॉनों की उपस्थिति के कारण, अन्य अणुओं के साथ बातचीत करने में सक्षम होता है, जो भड़काऊ प्रक्रिया के विकास में प्रत्यक्ष हिस्सा लेता है। ऑक्सीजन मेटाबोलाइट्स जो मध्यस्थों का हिस्सा हैं, उनमें शामिल हैं:
इन सक्रिय पदार्थों का स्रोत उनकी उत्तेजना के दौरान एराकिडोनिक एसिड, फागोसाइटोसिस विस्फोट की बाहरी परत है, साथ ही साथ छोटे अणुओं का ऑक्सीकरण भी है।
ऑक्सीजन मेटाबोलाइट्स विदेशी एजेंटों को नष्ट करने के लिए फैगोसाइटोसिस कोशिकाओं की क्षमता को बढ़ाते हैं, जिससे वसा का ऑक्सीकरण होता है, अमीनो एसिड, न्यूक्लिक एसिड, कार्बोहाइड्रेट को नुकसान होता है, जो संवहनी पारगम्यता को बढ़ाता है। न्यूनाधिक के रूप में, मेटाबोलाइट्स सूजन को बढ़ाने में सक्षम हैं या एक विरोधी भड़काऊ प्रभाव है। पुरानी बीमारियों के विकास में बहुत महत्व है। neuropeptidesइस समूह में कैल्सीटोनिन, न्यूरोकेनिन ए और पदार्थ आर शामिल हैं। ये न्यूरोपैप्टाइड्स के सबसे प्रसिद्ध मॉड्यूल हैं। पदार्थ का प्रभाव निम्नलिखित प्रक्रियाओं पर आधारित है:
उपरोक्त सभी के अलावा, एसिटाइलकोलाइन, एपिनेफ्रीन और नॉरपेनेफ्रिन भी सक्रिय मध्यस्थ हैं। एसिटाइलकोलाइन धमनी हाइपरिमिया के गठन में शामिल है, विकृति में रक्त वाहिकाओं को पतला करता है। Norepinephrine और एड्रेनालाईन सूजन के न्यूनाधिक के रूप में कार्य करते हैं, संवहनी पारगम्यता के विकास को रोकते हैं। भड़काऊ प्रतिक्रिया का विकास शरीर का उल्लंघन नहीं है। इसके विपरीत, यह एक संकेतक है कि प्रतिरक्षा प्रणाली अपने कार्यों से मुकाबला करती है। सूजन का पैथोफिज़ियोलॉजी (व्याख्यान संख्या IX) भाग 1। 1. सूजन की अवधारणा। 2. प्राथमिक और द्वितीयक क्षति। 3. सूजन में चयापचय संबंधी विकार। 4. सूजन के मध्यस्थ। 5. सूजन में संवहनी प्रतिक्रिया के चरण। 6. एक्सयूडेट, इसके प्रकार और कार्य। सूजन (सूजन) संयोजी ऊतक, वाहिकाओं और पूरे जीव के तंत्रिका तंत्र की एक जटिल स्थानीय सुरक्षात्मक-अनुकूली प्रतिक्रिया है, जो नुकसान की प्रतिक्रिया में अत्यधिक संगठित प्राणियों से विकास की प्रक्रिया में विकसित होती है, जिसका उद्देश्य क्षति कारक को अलग करने और हटाने और क्षति के परिणामों को समाप्त करना है। यह चयापचय और रक्त परिसंचरण, फागोसाइटोसिस और प्रसार में परिवर्तन के साथ एक विशिष्ट रोग प्रक्रिया है। किसी भी सूजन का आधार है: 1) क्षति और 2) सुरक्षात्मक प्रतिक्रियाएं। क्षति का विरोध करने की क्षमता, घावों को भरने की क्षमता, कम से कम कुछ खोए हुए ऊतकों को बहाल करने के लिए जीवित जीवों की सबसे महत्वपूर्ण संपत्ति है। और इन गुणों को इस तथ्य से निर्धारित किया जाता है कि एक स्वस्थ शरीर सामान्य और स्थानीय प्रतिक्रियाओं की एक श्रृंखला द्वारा क्षति के लिए तुरंत प्रतिक्रिया करता है। सामान्य प्रतिक्रियाएँ शरीर के तंत्रिका, अंतःस्रावी और प्रतिरक्षा प्रणाली के कार्यात्मक अवस्था में अधिक या कम स्पष्ट परिवर्तनों के कारण। वे पूरे जीव की प्रतिक्रियाशीलता में परिवर्तन के साथ हैं। स्थानीय प्रतिक्रियाएं जो क्षति क्षेत्र में और इसके आसपास के क्षेत्र में होती हैं, सूजन नामक एक प्रक्रिया की विशेषता है। जैविक अर्थ सूजन को सीमित करना, देरी करना, क्षति के विकास को रोकना है और आगे, यदि यह सफल होता है, तो क्षय उत्पादों और नष्ट ऊतकों से नुकसान के क्षेत्र को साफ़ करें, इस प्रकार वास्तविक बहाली प्रक्रियाओं के लिए जमीन तैयार करना। 18 वीं शताब्दी में, सेलस ने सूजन के 4 मुख्य नैदानिक लक्षणों का वर्णन किया: लालिमा (रबोर), सूजन (ट्यूमर), दर्द (डोलर) और बुखार (कैलोर)। गैलेन ने पांचवां संकेत जोड़ा - शिथिलता (फंक्शियो लाईसा)। रुबेर, ट्यूमर, डोलर, कैलोर एट फंक्शनलियो लासा लक्षणा इन्फ्लुएंटिस संट। सूजन के कारण : ए) भौतिक कारक, बी) रासायनिक कारक, सी) जैविक कारक, डी) संचार संबंधी विकार, ई) ट्यूमर की वृद्धि, ई) प्रतिरक्षा प्रतिक्रियाएं। अलग 4 चरणों: 1. परिवर्तन (परिवर्तन अनुपात) 2. एक्सयूडीशन (एक्सोडुडियो) 3. उत्प्रवास (इमिग्रेटियो) 4. प्रसार (प्रसार)। बदलने की शक्तिवाला- यह मुख्य लिंक है, वास्तव में - ट्रिगर तंत्र। परिवर्तन प्राथमिक या माध्यमिक हो सकता है। मुख्य परिवर्तन हानिकारक कारक के प्रभाव के तुरंत बाद विकसित होता है और अंग के कार्यात्मक तत्व के स्तर पर बनता है। प्राथमिक परिवर्तन स्वयं को विशिष्ट परिवर्तनों के साथ-साथ गैर-विशिष्ट परिवर्तनों के रूप में प्रकट कर सकता है जो रोगजनक कारक के गुणों और विशेषताओं की परवाह किए बिना स्टीरियोटाइप रूप से विकसित होते हैं। ये परिवर्तन संबंधित हैं: 1) झिल्ली संरचनाओं को नुकसान के साथ, 2) माइटोकॉन्ड्रियल झिल्ली क्षति के साथ, 3) लाइसोसोम को नुकसान के साथ। कोशिका झिल्ली संरचना के विघटन से सेलुलर पंपों का विघटन होता है। इसलिए, पर्यावरणीय होमियोस्टैसिस में अपने स्वयं के चयापचय में बदलाव करके कोशिका की पर्याप्त प्रतिक्रिया करने की क्षमता खो जाती है, एंजाइम सिस्टम और माइटोकॉन्ड्रिया बदल जाते हैं। कोशिका में ऑक्सीकृत मेटाबोलाइट्स जमा होते हैं: पाइरुविक, लैक्टिक और स्यूसिनिक एसिड। प्रारंभ में, ये परिवर्तन प्रतिवर्ती हैं और गायब हो सकते हैं यदि एटियलॉजिकल कारक बंद हो गया है। सेल पूरी तरह से अपने कार्य को ठीक करता है। यदि क्षति जारी है और लाइसोसोम प्रक्रिया में शामिल हैं, तो परिवर्तन अपरिवर्तनीय हैं। इसलिए, लाइसोसोम को "भड़काऊ लॉन्च साइट" कहा जाता है और यह उनसे है कि माध्यमिक परिवर्तन का गठन शुरू होता है। माध्यमिक परिवर्तन लाइसोसोमल एंजाइमों के हानिकारक प्रभाव के कारण। ग्लाइकोलाइसिस, लिपोलिसिस और प्रोटियोलिसिस को बढ़ाया जाता है। ऊतकों में प्रोटीन के टूटने के परिणामस्वरूप, पॉलीपेप्टाइड्स और अमीनो एसिड की संख्या बढ़ जाती है; वसा के टूटने में, फैटी एसिड में वृद्धि होती है; कार्बोहाइड्रेट चयापचय के विघटन से लैक्टिक एसिड का संचय होता है। यह सब ऊतकों में शारीरिक और रासायनिक विकारों का कारण बनता है और हाइपरोस्मिया K +, Na +, Ca 2+, Cl - आयनों की एकाग्रता में वृद्धि के साथ विकसित होता है; हाइपरकोनिया - छोटे में बड़े के टूटने के कारण प्रोटीन अणुओं की संख्या में वृद्धि; हाइपरयोनियम एच + - हाइड्रोजन आयनों की रिहाई के साथ बड़ी मात्रा में एसिड के पृथक्करण के कारण। और इस सब के परिणामस्वरूप, अम्लीय चयापचय उत्पादों में वृद्धि के कारण चयापचय एसिडोसिस विकसित होता है। ऊतक के सभी घटक प्रक्रिया में शामिल हैं और परिवर्तन अपरिवर्तनीय है, जिसके परिणामस्वरूप कोशिकाओं का ऑटोलिसिस है। पदार्थों का गठन जो न केवल मजबूत कर सकता है, बल्कि परिवर्तन को कमजोर कर सकता है, जिससे सूजन के विभिन्न घटकों को प्रभावित किया जा सकता है, अर्थात्। विनियमन microcirculation, exudation, leukocyte उत्प्रवास और संयोजी ऊतक कोशिकाओं के प्रसार। इन जैविक रूप से सक्रिय पदार्थों को कहा जाता है मध्यस्थों या भड़काऊ मॉड्यूलेटर। भड़काऊ मध्यस्थ अलग ● समय पर उनकी गतिविधि: जल्दी और देर से; ● आवेदन के बिंदु से: वाहिकाओं या कोशिकाओं को प्रभावित करना और ● मूल से: हास्य (प्लाज्मा) और सेलुलर। भड़काऊ मध्यस्थों के स्रोत रक्त प्रोटीन और बाह्य तरल पदार्थ हो सकते हैं, सभी रक्त कोशिकाएं, संयोजी ऊतक कोशिकाएं, तंत्रिका कोशिकाएं, संयोजी ऊतक के गैर-सेलुलर तत्व। होते हैं preformed और नवगठित मध्यस्थों। विकृत मध्यस्थों को बिना किसी नुकसान के लगातार संश्लेषित किया जाता है, विशेष दुकानों में जमा होता है और क्षति के तुरंत बाद जारी किया जाता है (उदाहरण के लिए, हिस्टामाइन)। प्रतिक्रिया के उपाय के रूप में क्षति के बाद अन्य मध्यस्थों का संश्लेषण शुरू होता है। ऐसे मध्यस्थों को नवगठित कहा जाता है (उदाहरण के लिए, प्रोस्टाग्लैंडिंस)। ऊतक को नुकसान विशेष प्रोटियोलिटिक रक्त प्रणालियों के सक्रियण के साथ होता है, जो विभिन्न पेप्टाइड्स के सूजन केंद्र में उपस्थिति की ओर जाता है जो भड़काऊ मध्यस्थों के रूप में कार्य करता है। वासोएक्टिव किनेन्स भी तब बनते हैं जब फाइब्रिनोलिटिक सिस्टम सक्रिय हेजमैन कारक द्वारा सक्रिय होता है, जो निष्क्रिय प्लास्मिनोजेन को रक्त में एक सक्रिय एंजाइम में बदल देता है। plasmin। प्लास्मिन क्लीव फाइब्रिन (और सफल घाव भरने के लिए फाइब्रिन का समय पर पाचन आवश्यक है)। एक ही समय में पेप्टाइड्स का गठन किया जाता है जो रक्त वाहिकाओं को पतला करने और बढ़े हुए संवहनी पारगम्यता को बनाए रखने में सक्षम होते हैं। प्लास्मिन पूरक प्रणाली को सक्रिय करता है। पूरक प्रणाली, जिसमें लगभग 20 विभिन्न प्रोटीन शामिल हैं, को हेजमैन कारक के अलावा दो और तरीकों से सक्रिय किया जाता है: क्लासिक प्रतिजन-एंटीबॉडी जटिल है और विकल्प माइक्रोबियल कोशिकाओं के लिपोपॉलेसेकेराइड है। पूरक के सी 3 ए और सी 5 ए घटक सूजन में शामिल होते हैं, जो बैक्टीरिया, वायरस और रोगजनक रूप से अन्य कोशिकाओं को बदल देते हैं; मध्यस्थों की रिहाई के साथ मस्तूल कोशिकाओं और बेसोफिल के क्षरण में योगदान करते हैं। पूरक घटक भी रक्त कोशिकाओं के आसंजन, एकत्रीकरण और गिरावट का कारण बनते हैं, लाइसोसोमल एंजाइमों की रिहाई, मुक्त कण का निर्माण, आईएल -1, केमोटैक्सिस, ल्यूकोपॉइसिस और इम्युनोग्लोबुलिन के संश्लेषण को उत्तेजित करते हैं। प्लाज्मा और सेलुलर मूल के मध्यस्थ परस्पर संबंधित होते हैं और प्रतिक्रिया और पारस्परिक प्रवर्धन के साथ ऑटोकैटलिटिक प्रतिक्रिया के सिद्धांत पर कार्य करते हैं। माइक्रोकिरकुलेशन डिसऑर्डर सूजन के फ़ोकस में माइक्रोकिरुलेटरी वाहिकाओं के स्वर में परिवर्तन की विशेषता होती है, वाहिका के बाहर रक्त के तरल भाग की वृद्धि हुई धारा (यानी, बाहर निकालना) और बाहर निकलना समान तत्व रक्त (यानी उत्प्रवास)। के लिए संवहनी प्रतिक्रिया विशेषता ४ मंच : 1) अल्पकालिक वैसोस्पैज़म, 2) धमनी हाइपरमिया, 3) शिरापरक हाइपरिमिया, ऐंठन वाहिकाओं ऊतक पर एक हानिकारक एजेंट की कार्रवाई के तहत उत्पन्न होती हैं और इस तथ्य से जुड़ी होती हैं कि वैसोकॉन्स्ट्रिक्टर्स पहले उत्तेजित होते हैं क्योंकि वे वासोडिलेटर की तुलना में अधिक संवेदनशील होते हैं। ऐंठन 40 सेकंड तक रहता है और जल्दी से धमनी हाइपरमिया द्वारा बदल दिया जाता है। धमनी हाइपरमिया निम्नलिखित तीन तरीकों से गठित: ● वाहिकासंकीर्णन के पक्षाघात के परिणामस्वरूप; Vasodilating गतिविधि के साथ मध्यस्थों के संपर्क के परिणामस्वरूप ●; ● एक्सोन रिफ्लेक्स के कार्यान्वयन के परिणामस्वरूप। Precapillary स्फिंक्टर आराम करते हैं, कार्यशील केशिकाओं की संख्या बढ़ जाती है, और क्षतिग्रस्त क्षेत्र के जहाजों के माध्यम से रक्त का प्रवाह बरकरार ऊतक की तुलना में दस गुना अधिक हो सकता है। Microcirculatory वाहिकाओं का विस्तार, कार्यशील केशिकाओं की संख्या में वृद्धि और शरीर में रक्त की आपूर्ति में वृद्धि सूजन का पहला स्थूल संकेत निर्धारित करता है - लालिमा। यदि त्वचा में सूजन विकसित होती है, जिसका तापमान रक्त प्रवाह के तापमान से नीचे है, तो सूजन वाले क्षेत्र का तापमान बढ़ता है - बुखार होता है। चूंकि पहली बार चोट लगने के बाद, सूजन के क्षेत्र में रैखिक और वॉल्यूमेट्रिक रक्त प्रवाह वेग काफी बड़ा है, सूजन के स्रोत से बहने वाले रक्त में अधिक ऑक्सीजन और कम बरामद हीमोग्लोबिन होता है और इसलिए एक चमकदार लाल रंग होता है। सूजन के दौरान धमनी हाइपरमिया लंबे समय तक नहीं रहता है (15 मिनट से एक घंटे तक) और हमेशा शिरापरक हाइपरिमिया में बदल जाता है, जिसमें शरीर में रक्त की आपूर्ति धीमी हो जाती है और यहां तक कि केशिका रक्त प्रवाह की पूर्ण समाप्ति भी होती है। शिरापरक हाइपरिमिया Precapillary स्फिंक्टर्स के अधिकतम विस्तार के साथ शुरू होता है, जो vasoconstrictor उत्तेजनाओं के प्रति असंवेदनशील हो जाता है और शिरापरक बहिर्वाह में बाधा उत्पन्न होती है। उसके बाद, केशिकाओं और धमनी में रक्त प्रवाह धीमा हो जाता है। शिरापरक हाइपरिमिया के विकास का मुख्य कारण एक्सयूडीशन है - रक्त के तरल भाग का माइक्रोवैस्कुलर से आसपास के ऊतक में बाहर निकलना। एक्सयूडीशन रक्त की चिपचिपाहट में वृद्धि के साथ होता है, रक्त प्रवाह में परिधीय प्रतिरोध बढ़ता है, रक्त प्रवाह की गति कम हो जाती है। इसके अलावा, एक्सयूडेट शिरापरक वाहिकाओं को संकुचित करता है, जो शिरापरक बहिर्वाह को जटिल करता है और शिरापरक हाइपरमिया भी बढ़ाता है। शिरापरक हाइपरिमिया के विकास को रक्त वाहिकाओं के अम्लीय वातावरण में सूजन, रक्त का गाढ़ा होना, बिगड़ा हुआ डिस्मोसोम, ल्यूकोसाइट्स के सीमांत खड़े होने, माइक्रोथ्रोम्बी के गठन द्वारा बढ़ावा दिया जाता है। वाहिकाओं में हाइड्रोस्टेटिक दबाव में वृद्धि के कारण रक्त प्रवाह धीरे-धीरे धीमा हो जाता है और नई गुणात्मक विशेषताओं को प्राप्त करता है: जब दिल के सिस्टोल के समय रक्त आगे बढ़ता है, और डायस्टोल के समय रक्त रुक जाता है। हाइड्रोस्टेटिक दबाव में और वृद्धि के साथ, सिस्टोल में रक्त आगे बढ़ता है, और डायस्टोल के समय यह वापस आता है - अर्थात, पेंडुलम जैसा आंदोलन उत्पन्न होता है। रक्त के पुश और पेंडुलम आंदोलन पल्सेटिंग दर्द की घटना को निर्धारित करता है। धीरे-धीरे बुझाने से स्टैसिस का विकास होता है - सूजन में एक सामान्य घटना। एक नियम के रूप में ठहराव इसकी पारगम्यता में तेज वृद्धि के कारण माइक्रोकिरकुलरी बेड के शिरापरक भाग के व्यक्तिगत जहाजों में होता है। इसी समय, रक्त का तरल भाग जल्दी से अतिरिक्त स्थान में गुजरता है और यह वाहिका रक्त कोशिकाओं के एक द्रव्यमान से भर जाती है जो एक दूसरे से निकटता से संबंधित होते हैं। इस तरह के द्रव्यमान की उच्च चिपचिपाहट इसे जहाजों के माध्यम से स्थानांतरित करना असंभव बना देती है और ठहराव होता है। लाल रक्त कोशिकाएं "सिक्का स्तंभ" बनाती हैं, उनके बीच की सीमाएं धीरे-धीरे मिट जाती हैं और पोत के लुमेन में एक ठोस द्रव्यमान बनता है - कीचड़ (अंग्रेजी से। कीचड़ - टीना, गंदगी)। एक्सिडेशन मैकेनिज्म: सूजन की वजह से होने वाली उत्तेजना मुख्य रूप से संवहनी एंडोथेलियम में एक महत्वपूर्ण परिवर्तन के परिणामस्वरूप प्रोटीन के लिए माइक्रोवैस्कुलर की पारगम्यता में वृद्धि के कारण होती है। Microcirculatory वाहिकाओं के एंडोथेलियल कोशिकाओं के गुणों में परिवर्तन मुख्य हैं, लेकिन सूजन के दौरान एक्सयूडीशन का एकमात्र कारण नहीं है। विभिन्न एक्सयूडेट्स का निर्माण माइक्रोकिरकुलरी वाहिकाओं के अंदर हाइड्रोस्टेटिक दबाव के विकास में योगदान देता है, जो एक्सटेरियोस्कुलर स्पेस में ऑस्मोटिक रूप से सक्रिय ऊतक गिरावट उत्पादों के संचय के कारण, धमनी के तरल पदार्थ के विस्तार के साथ जुड़ा होता है। अधिक महत्वपूर्ण रूप से, एक्सयूलेशन की प्रक्रिया को वीन्यूल्स और केशिकाओं में व्यक्त किया जाता है। एक्सफोलिएशन सूजन का चौथा संकेत बनाता है - सूजन (ट्यूमर)। एक्सयूडेट रचना (एक्ससुडाटम) रक्त का तरल भाग, रक्त के गठित तत्व और नष्ट हुए ऊतक होते हैं। एक्सयूडेट की संरचना 5 प्रकार की सूजन का उत्सर्जन करती है: ● गंभीर; ● कैटरल (श्लेष्म); ● तंतुमय; ● रक्तस्रावी; ● शुद्ध; ● आयशरस। कार्य निष्पादित करें - बुझाने के परिणामस्वरूप, बैक्टीरिया और अन्य विषाक्त पदार्थों की एकाग्रता रक्त प्लाज्मा में आने वाले प्रोटियोलिटिक एंजाइमों द्वारा पतला और नष्ट हो जाती है। एक्सयूडीशन के दौरान, सीरम एंटीबॉडी सूजन के फोकस में प्रवेश करते हैं, जो बैक्टीरिया के विषाक्त पदार्थों को बेअसर करते हैं और बैक्टीरिया को खोल देते हैं। भड़काऊ हाइपरिमिया रक्त ल्यूकोसाइट्स की सूजन के फोकस को एक संक्रमण प्रदान करता है, फागोसाइटोसिस को बढ़ावा देता है। फाइब्रिनोजेन एक्सयूडेट फाइब्रिन में बदल जाता है, जिसके धागे एक संरचना बनाते हैं जो घाव में ल्यूकोसाइट्स के संक्रमण की सुविधा प्रदान करता है। घावों की हीलिंग प्रक्रिया में फाइब्रिन महत्वपूर्ण भूमिका निभाता है। हालांकि, एक्सयूडीशन के नकारात्मक परिणाम भी हैं - ऊतक की सूजन से घुटन हो सकती है या इंट्राक्रानियल दबाव में वृद्धि हो सकती है जिससे जीवन को खतरा होता है। Microcirculation के विकार से इस्केमिक ऊतक क्षति हो सकती है। फाइब्रिन के अत्यधिक जमाव से क्षतिग्रस्त ऊतक की बाद की मरम्मत बाधित हो सकती है और संयोजी ऊतक के अत्यधिक प्रसार में योगदान कर सकती है। इसलिए, डॉक्टर को एक्सयूडीशन के विकास पर प्रभावी नियंत्रण करना चाहिए। सूजन का पैथोफिज़ियोलॉजी (व्याख्यान संख्या X) भाग 2। 1. सूजन के फोकस में ल्यूकोसाइट्स का उत्प्रवास। 2. सूजन के फोकस में ल्यूकोसाइट्स के कार्य। 3. तीव्र और पुरानी सूजन। 4. सूजन का जैविक सार। 5. सूजन का निदान। जब धमनी हाइपरिमिया शिरापरक ल्यूकोसाइट्स में गुजरता है, तो वे धीरे-धीरे अक्षीय परत से परिधीय - पार्श्विका परत की ओर बढ़ते हैं और एंडोथेलियम सतह का पालन करना शुरू करते हैं। "ल्यूकोसाइट सीमांत खड़े दिखाई देते हैं और इस क्षण से ल्यूकोसाइट्स का व्यापक प्रवास शुरू होता है सूजन केंद्र। ल्यूकोसाइट को दो बाधाओं को दूर करना चाहिए: एंडोथेलियम और तहखाने झिल्ली। ल्यूकोसाइट्स की एंडोथेलियम परत गुजरती है, एंडोथेलियल कोशिकाओं के बीच निचोड़, और तहखाने झिल्ली अस्थायी रूप से इसके प्रोटीज द्वारा भंग कर दी जाती है। पोत की दीवार के माध्यम से ल्यूकोसाइट के संक्रमण की पूरी प्रक्रिया 2 से 12 मिनट तक होती है और इससे पोत की दीवार को नुकसान नहीं होता है। ल्यूकोसाइट्स के उत्प्रवास का मुख्य स्थान पोस्टपेकिलरी वेन्यूल्स हैं। तीव्र सूजन में, सबसे पहले न्युट्रोफिल निकलते हैं और बहुत बाद में मोनोसाइट्स। ईोसिनोफिल्स, बेसोफिल्स और लिम्फोसाइट्स भी उत्सर्जन में सक्षम हैं। ल्यूकोसाइट प्रवासन भड़काऊ फोकस में विशेष मध्यस्थ हेमट्रेक्टेंट्स के उद्भव के साथ जुड़ा हुआ है। सबसे मजबूत हेमटाराक्टेंट लिपोपॉलीसेकेराइड हैं, जो बैक्टीरिया एंडोटॉक्सिन का हिस्सा हैं। सबसे शक्तिशाली अंतर्जात हेमट्रैक्टेंट में सूजन के दौरान सक्रिय पूरक के टुकड़े शामिल होते हैं, विशेष रूप से सी 5 ए, ल्यूकोट्रिन बी 4, प्लेटलेट सक्रिय करने वाला कारक और कैलीक्रिन। सूजन केंद्र में ल्यूकोसाइट्स का माइग्रेशन उनके आसंजन से शुरू होता है जो कि माइक्रोवैस्कुलर के संवहनी एंडोथेलियम से होता है। विशेष आरएनए अणुओं की एंडोथेलियल कोशिकाओं और उनके संबंधित प्रोटीन के बढ़ते गठन के परिणामस्वरूप आसंजन बढ़ जाता है। संवहनी दीवार के माध्यम से ल्यूकोसाइट्स का मार्ग इन कोशिकाओं में निहित स्थानांतरित करने की क्षमता का परिणाम है - अर्थात्। हरकतजो हेमट्रेक्टेंट्स द्वारा भी सक्रिय होता है। ल्यूकोसाइट्स के साइटोप्लाज्म के अंदर, कैल्शियम आयनों की एकाग्रता बढ़ जाती है। यह सूक्ष्मनलिका प्रणाली को सक्रिय करता है, जो कोशिका के आंतरिक कंकाल का निर्माण करता है, एक्टोमोसिन परिसरों को सक्रिय करता है, उनके दानेदार पदार्थों के न्युट्रोफिल का स्राव करता है, जिसमें रक्त वाहिकाओं के बेसल झिल्ली को भंग करने में सक्षम न्यूट्रोफिल प्रोटीज शामिल हैं। ल्यूकोसाइट्स के सतह रिसेप्टर्स के साथ हेमट्रेक्टेंट्स की बातचीत उन में विभिन्न एंजाइमों की सक्रियता के साथ होती है, जिसमें कैल्शियम-निर्भर फॉस्फोलिपेज़ ए 2, कैल्शियम-निर्भर प्रोटीन किनेसेस: प्रोटीन किनसे ए और प्रोटीन किनोसिन सी। फ्रंट पोल पर ल्यूकोसाइट में हेमट्रेक्टेंट्स के प्रभाव के तहत, कॉर्टिकल जेल सोल में बदल जाता है, अर्थात। अधिक तरल हो जाता है। इसके मध्य भाग के सोल को ल्यूकोसाइट के इस पतले हिस्से में डाला जाता है। ल्यूकोसाइट को पीछे की ओर छोटा और सामने की ओर लंबा किया जाता है। पूर्वकाल ध्रुव के कॉर्टिकल जेल के तरलीकृत हिस्से को बल के साथ वापस फेंक दिया जाता है और इस प्रकार ल्यूकोसाइट आगे बढ़ता है। न्यूट्रोफिलिक ल्यूकोसाइट्स में सबसे बड़ी कार्यात्मक गतिविधि है। पॉलीमॉर्फोन्यूक्लियर ल्यूकोसाइट्स सूजन के ध्यान में आने वाले पहले हैं क्योंकि वे अधिक संवेदनशील हैं, वे रक्त में बहुत अधिक हैं। उन्हें कोशिकाएं कहा जाता है। " आपातकालीन प्रतिक्रिया“और डिस्पोजेबल। मोनोसाइट्स 3 दिनों तक रक्त में होते हैं, ऊतक में जाते हैं और लगभग 10 दिनों तक उनमें होते हैं। उनमें से कुछ गतिहीन ऊतक मैक्रोफेज में विभेदित हैं, कुछ निष्क्रिय हैं और फिर से सक्रिय हो सकते हैं। इसलिए, मोनोसाइट्स को पुन: प्रयोज्य कोशिका कहा जाता है। पोत के बाहर रक्त कोशिकाओं की रिहाई के इस तरह के अनुक्रम की पहचान मेचनकोव द्वारा की गई है और इसे "उत्प्रवास का नियम" या "सूजन के दौरान सेलुलर प्रतिक्रिया का चरण" कहा जाता है: 1) बहुपद (न्यूट्रोफिल और ईोसिनोफिल) 2 दिन तक, 2) मोनोन्यूक्लियर (मोनोसाइट्स और लिम्फोसाइट्स) 5-6 दिनों तक, 3) फाइब्रोब्लास्टिक, सूजन के फोकस में हिस्टियोसाइट्स और फाइब्रोब्लास्ट के संचय की विशेषता है। सूजन के फोकस में ल्यूकोसाइट्स का सबसे महत्वपूर्ण कार्य फागोसाइटोसिस है - अर्थात। बैक्टीरिया को पकड़ने, मारने और पचाने के साथ-साथ शरीर के ऊतकों और कोशिकाओं के क्षय उत्पादों का पाचन होता है। फागोसाइटोसिस के दौरान, होते हैं 4 मंच : 1) ऑब्जेक्ट के लिए फैगोसाइट सन्निकटन का चरण; 2) ऑब्जेक्ट को फैगोसाइट के पालन का चरण; 3) ऑब्जेक्ट के फैगोसाइट अवशोषण का चरण; 4) अवशोषित वस्तु के इंट्रासेल्युलर परिवर्तनों का चरण। पहला चरण फिमोसाइट्स से लेकर केमोकोटैक्सिस की क्षमता द्वारा समझाया गया है। ऑप्सिन, एंटीबॉडी और टुकड़े, प्लाज्मा प्रोटीन और लाइसोजाइम के पूरक, किसी वस्तु के फैगोसाइट द्वारा चिपके और बाद में अवशोषण के तंत्र में एक बड़ी भूमिका निभाते हैं। यह स्थापित किया गया है कि ऑप्सोनिन अणुओं के कुछ हिस्से हमला किए गए सेल की सतह पर, और उसी अणु के अन्य भागों में बाँधते हैं - फैगोसाइट झिल्ली के साथ। अवशोषण का तंत्र चिपके से अलग नहीं होता है - धीरे-धीरे माइक्रोबियल सेल को फागोसाइट के साथ कवर करके किया जाता है, अर्थात। अनिवार्य रूप से माइक्रोब की सतह पर फैगोसाइट की सतह को चिपकाकर जब तक कि पूरी वस्तु को फागोसाइट झिल्ली से चिपकाया नहीं जाता है। एक परिणाम के रूप में, अवशोषित वस्तु फैगोसाइट के अंदर होती है, जो फागोसिटिक सेल के झिल्ली के हिस्से द्वारा गठित बैग में संलग्न होती है। इस बैग को फागोसोम कहा जाता है। फागोसोम गठन फागोसोम के अंदर अवशोषित वस्तु के इंट्रासेल्युलर परिवर्तनों के चरण को शुरू करता है, अर्थात। फैगोसाइट के आंतरिक वातावरण के बाहर। फैगोसाइटोसिस के दौरान अवशोषित एक वस्तु के इंट्रासेल्युलर परिवर्तनों का मुख्य हिस्सा गिरावट के साथ जुड़ा हुआ है - अर्थात्, फागोसाइट्स के साइटोप्लाज्मिक ग्रैन्यूल की सामग्री को फागोसोम में स्थानांतरित करना। इन कणिकाओं में, सभी विखंडित फागोसाइट्स में जैविक रूप से सक्रिय पदार्थों की एक बड़ी संख्या होती है, मुख्य रूप से एंजाइम होते हैं, जो रोगाणुओं और अन्य अवशोषित वस्तुओं को मारते हैं। न्यूट्रोफिल में, 2-3 प्रकार के दाने होते हैं जिनमें लाइसोजाइम होते हैं - माइक्रोबियल दीवार, लैक्टोफेरिन को भंग करना - एक प्रोटीन जो लोहे को बांधता है और इस तरह एक बैक्टीरियोस्टेटिक प्रभाव, मायलोपरोक्सीडेज, तटस्थ रोग, एसिड हाइड्रॉलिस, एक प्रोटीन होता है जो विटामिन बी 12 और अन्य को बांधता है। जैसे ही एक फागोसोम का गठन होता है, दाने इसे करीब से देखते हैं। ग्रैन्यूल्स की झिल्लियां फागोसोम झिल्ली के साथ विलीन हो जाती हैं और ग्रैन्यूल की सामग्री फेजोम के आंतरिक भाग में प्रवेश करती है। जैसा कि पहले ही उल्लेख किया गया है, न्युट्रोफिल सूजन के क्षेत्र में घुसपैठ करने वाले पहले ल्यूकोसाइट्स हैं। वे बैक्टीरिया और फंगल संक्रमण के खिलाफ प्रभावी सुरक्षा प्रदान करते हैं। यदि घाव संक्रमित नहीं है, तो इसमें न्युट्रोफिल की सामग्री जल्दी से कम हो जाती है और 2 दिनों के बाद मैक्रोफेज सूजन के फोकस में प्रबल होते हैं। न्यूट्रोफिल की तरह, भड़काऊ मैक्रोफेज मोटाइल कोशिकाएं होती हैं जो विभिन्न संक्रामक एजेंटों से फागोसिटोसिस द्वारा शरीर की रक्षा करती हैं। वे लाइसोसोमल एंजाइम और ऑक्सीजन कट्टरपंथी को भी सुरक्षित करने में सक्षम हैं, लेकिन न्यूट्रोफिल से कई गुण हैं जो तीव्र सूजन के बाद के चरणों में और घाव भरने के तंत्र में इन कोशिकाओं को विशेष रूप से महत्वपूर्ण बनाते हैं: 1. मैक्रोफेज बहुत लंबे समय तक रहते हैं (महीने, और न्यूट्रोफिल - एक सप्ताह)। 2. मैक्रोफेज न्यूट्रोफिल सहित अपने स्वयं के जीव की क्षतिग्रस्त और गैर-व्यवहार्य कोशिकाओं को अवशोषित करने और फिर पहचानने और नष्ट करने में सक्षम हैं। इससे संबंधित भड़काऊ एक्सयूडेट की "सफाई" में उनकी असाधारण भूमिका है। मैक्रोफेज सूजन के फोकस से क्षतिग्रस्त संयोजी ऊतक के विघटन और हटाने में शामिल मुख्य कोशिकाएं हैं, जो बाद के ऊतक पुनर्निर्माण के लिए आवश्यक हैं। वे तटस्थ प्रोटीज को संश्लेषित और स्रावित करते हैं: इलास्टेज, कोलेजनैज, प्लास्मिनोजेन एक्टिवेटर, संयोजी ऊतक के बाह्य कोलेजन और इलास्टिन फाइबर को नष्ट करते हैं। घाव भरने में मैक्रोफेज की प्रमुख भूमिका होती है। प्रयोग में जानवरों में, मोनोन्यूक्लियर कोशिकाओं से रहित, घाव ठीक नहीं होता है। यह इस तथ्य से समझाया गया है कि मैक्रोफेज फाइब्रोब्लास्ट्स और अन्य मेसेंकाईमल कोशिकाओं के लिए विकास कारकों को संश्लेषित करते हैं, फाइब्रोब्लास्ट्स द्वारा कोलेजन संश्लेषण को बढ़ाने वाले कारक उत्पन्न करते हैं, ऐसे कारकों के स्रोत हैं जो एंजियोजेनेसिस के विभिन्न चरणों को नियंत्रित करते हैं - क्षतिग्रस्त ऊतकों के पुनर्संयोजन, पॉलीपेप्टाइड हार्मोन का उत्पादन करते हैं जो तीव्र चरण प्रतिक्रिया को मध्यस्थता करते हैं - इंटरलेयूकिन। -1 और आईएल -6 और ट्यूमर नेक्रोसिस कारक। सूजन तीव्र और पुरानी में विभाजित है। तीव्रसूजन (इन्फ्लोमेटो एक्यूटा) अचानक क्षति के कारण विकसित होता है - जला, शीतदंश, यांत्रिक चोट, कुछ संक्रमण। इसकी अवधि आमतौर पर कई दिनों से अधिक नहीं होती है। तीव्र सूजन की विशेषता स्पष्ट एक्सयूडेटिव प्रतिक्रियाओं से होती है, जिसके दौरान पानी, प्रोटीन, रक्त कोशिकाएं (ज्यादातर ल्यूकोसाइट्स) रक्तप्रवाह को छोड़ देती हैं और क्षतिग्रस्त क्षेत्र में प्रवेश करती हैं। पुरानी सूजन (ज्वलनशीलता क्रोनिका) तब विकसित होती है जब हानिकारक एजेंट लंबे समय तक काम करता है। पुरानी सूजन सप्ताह, महीनों और वर्षों तक रहती है। फाइब्रोब्लास्ट्स और संवहनी एंडोथेलियम के प्रसार के साथ-साथ सूजन के फ़ोकस में विशेष कोशिकाओं के संचय द्वारा - मैक्रोफेज, लिम्फोसाइट्स, प्लाज्मा कोशिकाओं और फ़ाइब्रोब्लास्ट्स के रूप में यह बहुत अधिक नहीं है। सबसे गंभीर मानव रोगों में से एक पुरानी भड़काऊ प्रक्रिया की विशेषता है - कुष्ठ, संधिशोथ, तपेदिक, पुरानी पाइलोनफ्राइटिस, सिफलिस, यकृत सिरोसिस, और इसी तरह। जीर्ण सूजन आम तौर पर सामान्य पैरेन्काइमा को अपरिवर्तनीय क्षति के साथ होती है, जिसके दोष तंतुमय संयोजी ऊतक से भरे होते हैं जो प्रभावित अंगों को विकृत करते हैं। इष्टतम मामले में, हानिकारक एजेंट की कार्रवाई की समाप्ति भड़काऊ प्रतिक्रिया के क्षीणन और भड़काऊ प्रतिक्रियाओं के सभी परिणामों के पूर्ण उन्मूलन के साथ होती है - अर्थात्। "सूजन का पूर्ण संकल्प"। इसका मतलब है कि मध्यस्थों के गठन और क्षति क्षेत्र से उनके लापता होने, ल्यूकोसाइट्स के उत्प्रवास की समाप्ति, संवहनी पारगम्यता की बहाली, तरल पदार्थ, प्रोटीन, बैक्टीरिया और कोशिकाओं के टूटने वाले उत्पादों (न्यूट्रोफिल और मैक्रोफेज सहित) की समाप्ति। मध्यस्थों का गायब होना सूजन के स्रोत से उनके सहज प्रसार और आंशिक रूप से विभिन्न एंजाइमों द्वारा आंशिक रूप से निष्क्रियता के कारण होता है, निष्क्रियता प्रणाली के साथ ही सूजन के दौरान विकसित होती है। यदि संवहनी पारगम्यता में वृद्धि एंडोथेलियल कोशिकाओं को सकल क्षति से जुड़ी नहीं थी, तो मध्यस्थों के गायब होने के बाद पारगम्यता को सामान्य रूप से सामान्य किया जाता है। निडस में संचित अधिकांश सूजन लिम्फ प्रवाह के साथ हटा दी जाती है। फाइब्रिन जमा रक्त फाइब्रिनोलिटिक एंजाइम, भड़काऊ सेल एंजाइमों द्वारा भंग कर दिया जाता है और लसीका वाहिकाओं द्वारा भी हटा दिया जाता है। यह संभव है कि मैक्रोफेज भी लसीका वाहिकाओं को छोड़ दें। गैर विषैले अक्षुण्ण पदार्थों से लदे मैक्रोफेज का एक हिस्सा लंबे समय तक पूर्व सूजन के स्थान पर रह सकता है। सूजन का पूर्ण समाधान संरचना और क्षतिग्रस्त ऊतकों के कार्य की पूर्ण बहाली के लिए स्थितियां बनाता है। हालांकि, यह केवल अंगों और ऊतकों के अपेक्षाकृत छोटे घावों के साथ होता है, जो पुनर्जनन के लिए भी उच्च क्षमता रखते हैं - त्वचा, श्लेष्म झिल्ली और आंतरिक अंगों के पैरेन्काइमा। सूजन का अधूरा संकल्प इस तथ्य की ओर जाता है कि निशान के माध्यम से वसूली होती है। सामान्य प्रतिक्रिया शरीर का सूजन स्थान, कारण, अंग को नुकसान की डिग्री, अंग की अपर्याप्तता की घटना, शरीर की प्रतिक्रिया और प्रतिरोध, प्रतिरक्षा, अंतःस्रावी ग्रंथियों की स्थिति, पोषण, संविधान, लिंग, आयु, पिछली बीमारियों पर निर्भर करती है। सूजन का जैविक सार. द्वितीय 25 साल की (1882 से) मेचनकोव ने फागोसाइटोसिस की जांच की है। तुलनात्मक विकृति विज्ञान की उनकी पद्धति एक विकासवादी पहलू में प्रक्रिया का अध्ययन है। उन्होंने साबित किया कि जंतु जगत के सभी सदस्यों में सूजन होती है। एककोशिकीय संरक्षण और पोषण में समान हैं। निचले बहुकोशिकीय (स्पंज) में, सभी कोशिकाएं फागोसिटोज कर सकती हैं। रोगाणु परतों के गठन के दौरान, फागोसाइटोसिस मेसोडर्म से जुड़ा होता है। जब एक खुले प्रकार के संवहनी प्रणाली (क्रेफ़िश) का निर्माण होता है, तो फागोसाइट्स को भड़काऊ फ़ोकस पर आसानी से पहुंचाया जाता है और उच्चतर में, वाहिकाओं, तंत्रिका तंत्र और संयोजी ऊतक की प्रतिक्रिया फागोसाइटिक प्रतिक्रिया में शामिल हो जाती है। यह पूरे जीव की प्रतिक्रिया है, जो विकास की प्रक्रिया में विकसित हुई है, एक सुरक्षात्मक और अनुकूली मूल्य है - फागोसाइटोसिस संरक्षण का आधार है, बाकी सभी बस भड़काऊ प्रतिक्रिया का सामान है। सूजन का निदान - ऊतक के दृश्य क्षेत्रों पर, यह उपरोक्त लक्षणों से प्रकट होता है: लालिमा, बुखार, सूजन, दर्द और बिगड़ा हुआ कार्य। मूल्यांकन के तरीके फागोसाइट्स का कार्यात्मक मूल्यांकन: क) ल्यूकोसाइट्स की कार्यात्मक गतिविधि का निर्धारण: 1. फागोसिटोसिस का% प्रति 100 संभावित फागोसाइट्स में फैगोसाइटिक कोशिकाओं के% का एक व्यापक संकेतक है, 2. फागोसाइटिक संख्या इन 100 फागोसाइट्स द्वारा कब्जा की गई फागोसाइटोसिस वस्तुओं की संख्या है, 3. फैगोसाइटिक इंडेक्स - या अवशोषण की तीव्रता - फागोसाइटोसिस की कैप्चर की गई वस्तुओं की संख्या है, जो प्रत्येक फागोसाइटिक ल्यूकोसाइट के लिए जिम्मेदार है। 4. कुल अवशोषण तीव्रता 1 मिमी 3 में निहित फागोसाइट्स द्वारा कब्जा की गई फागोसाइटोसिस वस्तुओं की संख्या है, 5. फागोसाइटोसिस की पूर्णता, 6. समूहन सूचकांक - 15-20 मिनट में शिरापरक रक्त के बार-बार अध्ययन के बाद अंतःशिरा द्वारा प्रशासित होने पर रक्त से मोटे डाई के गायब होने की दर, 7. टीकाकरण की डिग्री का आकलन करने के लिए एंटीबॉडी टिटर निर्धारित करें, 8. एक्सयूडेट की सेलुलर संरचना की जांच की जाती है। 9. ल्यूकोसाइट्स और ल्यूकोसाइट सूत्र की कुल संख्या का निर्धारण। सामान्य स्थिति पर भड़काऊ प्रतिक्रिया की निर्भरता - प्रतिक्रियाशीलता और प्रतिरोध, जो सूजन की उपस्थिति, विकास, पाठ्यक्रम और परिणाम प्रदान करते हैं। सूजन हो सकती है: ● स्वच्छंद व्यक्ति - स्वस्थ व्यक्तियों में अच्छी प्रतिक्रिया के साथ, ● हाइपरर्जिक (बहुत तेजी से) - एलर्जी के मामले में या पित्त संबंधी व्यक्तियों में, सूजन- यह ऊतक क्षति के जवाब में उत्पन्न होने वाली एक फाइटोलैनेटिक सुरक्षात्मक रोग प्रक्रिया है, जिसमें विशिष्ट रूप से परिवर्तनकारी, माइक्रोकिरुलेटरी और प्रोलिफ़ेरेटिव परिवर्तन शामिल हैं, अंततः हानिकारक एजेंट, मृत ऊतक और अधिक या कम पूर्ण को अलग करने और समाप्त करने के उद्देश्य से अंग की रिकवरी। सेलस ने सूजन के 4 पुरस्कारों का वर्णन किया: लालिमा (रबोर), बुखार (कैलोर), सूजन (ट्यू-मोर), दर्द (डोलर)। गैलेन ने उन्हें पांचवां संकेत दिया - फ़ंक्शन का उल्लंघन (फंक्शनलियो लासा)। उपरोक्त के अलावा, निम्नलिखित हो सकता है सामान्य लक्षण सूजन: ल्यूकोसाइटोसिस, बुखार, प्रोटीन में परिवर्तन, रक्त की हार्मोनल और एंजाइमी संरचना, बढ़ा हुआ ईएसआर, आदि। भड़काऊ प्रक्रिया की गतिशीलता, इसके कारणों की परवाह किए बिना, हमेशा काफी मानक होती है। सूजन के 3 घटक हैं: एक्सयूलेशन और ल्यूकोसाइट इम्यूलेशन, प्रोलिफरेशन के साथ परिवर्तन, माइक्रोकैक्र्यूलेशन डिसऑर्डर और हेमोरहेओलॉजी। बदलने की शक्तिवाला(क्षति) कोशिकाओं के संरचनात्मक और कार्यात्मक संगठन और ऊतकों और अंगों के अंतरकोशिकीय पदार्थ का उल्लंघन है, जो उनकी महत्वपूर्ण गतिविधि के उल्लंघन के साथ है। यह प्राथमिक और माध्यमिक परिवर्तनों को भेद करने के लिए प्रथागत है। सूजन के कारण कारक के प्रत्यक्ष प्रभाव की प्रतिक्रिया में प्राथमिक परिवर्तन होता है। प्राथमिक परिवर्तन की प्रतिक्रियाएं मानो हानिकारक कारक की क्रिया को लम्बा खींचती हैं। कारक स्वयं शरीर के संपर्क में नहीं रह सकता है। द्वितीयक परिवर्तन सूजन पैदा करने वाले कारक और प्राथमिक परिवर्तन के कारकों दोनों के प्रभाव में होता है। हानिकारक कारक का प्रभाव मुख्य रूप से कोशिका झिल्ली पर प्रकट होता है, जिसमें लाइसोसोमल भी शामिल हैं। लाइसोसोम एंजाइम प्रतिक्रियाशील होते हैं। वे बाहर जाते हैं और सेल के सभी तत्वों को नुकसान पहुंचाते हैं। इस प्रकार, माध्यमिक परिवर्तन मुख्य रूप से आत्म-नुकसान है। एक ही समय में, माध्यमिक परिवर्तन सूजन का एक उचित और आवश्यक घटक है - एक सुरक्षात्मक और अनुकूली प्रक्रिया के रूप में। अतिरिक्त काउंटर क्षति का उद्देश्य एटियलॉजिकल कारक के प्रारंभिक स्थानीयकरण और इसके प्रभाव के तहत क्षतिग्रस्त शरीर के ऊतक है। क्षति की कीमत पर, कई अन्य महत्वपूर्ण सुरक्षात्मक घटनाएं प्राप्त की जाती हैं: चयापचय की सक्रियता, भड़काऊ और सेलुलर मध्यस्थों की भागीदारी, वृद्धि हुई फागोसाइटोसिस, आदि। मेटाबोलिक परिवर्तन सूजन की शुरुआत में मुख्य रूप से होता है कार्बोहाइड्रेट. प्रारंभ में, ऊतक एंजाइमों की सक्रियता के कारण, कार्बोहाइड्रेट और ग्लाइकोलाइसिस के दोनों ऑक्सीडेटिव फॉस्फोराइलेशन को बढ़ाया जाता है। इसके बाद, ग्लाइकोलाइसिस श्वसन से अधिक होने लगता है। इसका कारण यह है: 1. सूजन ऊतक द्वारा ऑक्सीजन की बढ़ती खपत। 2. रक्त संचार गड़बड़ा जाता है। रक्त में ऑक्सीजन की मात्रा कम हो जाती है। 3. ल्यूकोसाइट्स, लाइसोसोमल एंजाइमों के घाव में संचय, जो मुख्य रूप से एनारोबिक रूप से ग्लूकोज को तोड़ता है, बढ़ता है। 4. माइटोकॉन्ड्रिया की संख्या में कमी और कमी होती है। अंडर-ऑक्सीडाइज्ड कार्बोहाइड्रेट मेटाबॉलिज्म उत्पाद कपड़ों में जमा होते हैं: लैक्टिक और ट्राईकार्बोक्सिलिक एसिड। उल्लंघन वसा चयापचय इस तथ्य में निहित है कि मुख्य रूप से प्रकोप में लाइसोसोमल एंजाइम की कार्रवाई के तहत तीव्र सूजन वसा फैटी एसिड बनाने के लिए टूट जाते हैं। सूजन के प्रकोप में तेजी से परेशान प्रोटीन विनिमय और न्यूक्लिक एसिड। लाइसोसोमल और अन्य एंजाइमों की कार्रवाई के तहत, अमीनो एसिड, पॉलीपेप्टाइड्स, न्यूक्लियोटाइड्स, न्यूक्लियोसाइड (एडेनोसिन) प्रोटीन और न्यूक्लिक एसिड का टूटना होता है। कार्बोहाइड्रेट, वसा और प्रोटीन के चयापचय संबंधी विकारों के परिणामस्वरूप, अम्लीय चयापचय उत्पाद सूजन वाले ऊतक में जमा होते हैं और चयापचय को विकसित करते हैं एसिडोसिस। शुरुआत में, यह रक्त और ऊतक द्रव के क्षारीय भंडार द्वारा मुआवजा दिया जाता है। भविष्य में, क्षारीय भंडार के स्थानीय क्षय के साथ और ताजे रक्त के प्रवाह की कठिनाई के साथ, एसिडोसिस असंगत हो जाता है। तीव्र शुद्धता के साथ सूजन पीएच 5.4 तक पहुंच सकता है, और पुरानी में - 6.6। Aci-doses कुछ लाइसोसोमल एंजाइमों की कार्रवाई के लिए अनुकूल परिस्थितियों का निर्माण करते हैं, विशेष रूप से ग्लाइकोसिडेस में, जो संयोजी ऊतक के कार्बोहाइड्रेट घटकों को तोड़ते हैं। हाइड्रोजन आयनों की सांद्रता जितनी अधिक बढ़ जाती है, सूजन उतनी ही तीव्र होती है। केंद्र से परिधि की दिशा में, हाइड्रोजन आयनों की एकाग्रता धीरे-धीरे कम हो जाती है। एक अम्लीय वातावरण में, लवण का विघटन बढ़ता है। नतीजतन, के, ना, सीए आयनों की सामग्री सूजन फ़ोकस में बढ़ जाती है। यह भी कोशिकाओं के विनाश और इन लवणों की रिहाई के कारण है। मैक्रोर्जी के कम गठन के कारण, सेल में पोटेशियम-सोडियम संतुलन गड़बड़ा जाता है। पोटेशियम कोशिकाओं को छोड़ना शुरू कर देता है, इसके विपरीत, सोडियम, कोशिका में प्रवेश करता है। Hyperionium और di-zionia दिखाई देते हैं। उसी समय, आणविक एकाग्रता बढ़ जाती है, क्योंकि ऊतक के टूटने और बिगड़ा हुआ चयापचय की प्रक्रिया में, बड़े अणु कई छोटे लोगों में टूट जाते हैं। आयनिक और आणविक एकाग्रता में वृद्धि के कारण, हाइपरोस्मिया विकसित होता है। हाइपरकोनिया से हाइपरसोमिया होता है - सूजन फोकस में प्रोटीन एकाग्रता में वृद्धि। हाइपरकोनिया इसलिए होता है क्योंकि: 1) प्रोटीन रक्त से भड़काऊ फोकस में जारी किया जाता है, इस तथ्य के कारण कि एसिडोसिस और लाइसोसोमल एंजाइम प्रोटीन को संवहनी दीवार की पारगम्यता बढ़ाते हैं; 2) एसिडोसिस की शर्तों के तहत, मोटे प्रोटीन का ठीक करने के लिए विखंडन। भड़काऊ मध्यस्थों मध्यस्थों/ मध्यस्थ / सूजन - यह शारीरिक रूप से सक्रिय पदार्थों का एक जटिल है जो सूजन पैदा करने वाले कारकों की कार्रवाई की मध्यस्थता करता है और सूजन के विकास और परिणामों को निर्धारित करता है। सूजन के दौरान, वे बड़ी मात्रा में उत्सर्जित होते हैं और मध्यस्थ बन जाते हैं। क्योंकि वे भड़काऊ प्रक्रिया के प्रकटन को मजबूत करने या कमजोर करने में सक्षम हैं, जिन्हें वे न्यूनाधिक कहा जाता है। मध्यस्थता लिंक सूजन के रोगजनन में महत्वपूर्ण है। भड़काऊ मध्यस्थों के मुख्य समूह हैं: 1. बायोजेनिक अमाइन - हिस्टामाइन, सेरोटोनिन। हिस्टामाइन, सबसे महत्वपूर्ण मध्यस्थों में से एक, बेसोफिल्स और मस्तूल कोशिकाओं द्वारा स्रावित होता है और झिल्ली रिसेप्टर्स के माध्यम से अपनी कार्रवाई का एहसास करता है। हिस्टामाइन रिलीज नुकसान पहुंचाने वाली पहली ऊतक पुनः क्रियाओं में से एक है। हिस्टामाइन वासोडिलेशन का कारण बनता है, एंडोथेलियल कोशिकाओं के गोलाई के कारण संवहनी पारगम्यता को बढ़ाता है और इंटरसेलुलर संपर्कों को कमजोर करता है, प्रो-टैगलैंडिन ई 2 का उत्पादन बढ़ाता है, लाइसोसोमल एंजाइम, न्यूट्रोफिल की रिहाई को कम करता है। एक व्यक्ति दिखाई दिया खुजली वाली त्वचा, जलन और दर्द। रिलीज के बाद, हिस्टामाइन एंजाइम हिस्टामिन से बहुत तेजी से नष्ट हो जाता है। इसलिए, इसकी कार्रवाई जल्दी से बंद हो जाती है और अन्य मध्यस्थ, विशेष रूप से सेरोटोनिन में बदल जाते हैं। यह न्यूरो-ब्रेन, बेसोफिल्स, प्लेटलेट्स में निहित है। सूजन के फोकस में, मध्यम खुराक में सेरोटोनिन धमनी के फैलाव, शिराओं की दीवारों में मायोसाइट्स में कमी और शिरापरक जमाव का कारण बनता है। इसके अलावा, यह संवहनी दीवार की पारगम्यता बढ़ाता है, रक्त के थक्कों को बढ़ाता है, दर्द की भावना का कारण बनता है। बायोजेनिक एमाइन खुद और अन्य भड़काऊ मध्यस्थों के बीच बातचीत करते हैं। उदाहरण के लिए मध्यस्थों के 2 समूह: प्लाज्मा सिस्टम / किन, पूरक, घटक प्रणाली के घटक, रक्त जमावट कारक /। सबसे महत्वपूर्ण किनिन ब्रैडीकाइनिन और कैलिडिन हैं। किनिन प्रणाली की सक्रियता का प्रारंभिक बिंदु 12 जमावट कारक की सक्रियता है - ऊतक क्षति के मामले में हेजमैन कारक। यह कारक कल्लिक्रेनी में प्रीक्लेरिक्रेनी में बदल जाता है। प्लाज्मा प्रोटीन किनिनोजेन और प्लाज़्माक्विनिन पर बाद का कार्य इससे बनता है। वे धमनी के फैलाव का कारण बनते हैं और वेन्यूल्स की पारगम्यता को बढ़ाते हैं, नसों की चिकनी मांसपेशियों को कम करते हैं, और रक्तचाप को बढ़ाते हैं। किनिन्स न्यूट्रोफिल उत्प्रवास को रोकते हैं, लिम्फोसाइटों के प्रवास को उत्तेजित करते हैं, लिम्फोसाइट्स का स्राव करते हैं, और दर्द की भावना पैदा करते हैं। पूरक एक जटिल प्लाज्मा प्रणाली है जिसमें कम से कम 18 प्रोटीन होते हैं। यह विदेशी और देशी बदल कोशिकाओं के lysis प्रदान करता है। पूरक टुकड़े संवहनी पारगम्यता को बढ़ा सकते हैं, लाइसोसोमल हाइड्रॉलिसिस को छोड़ सकते हैं, ल्यूकोट्राइसेस के गठन में भाग ले सकते हैं। हेमोस्टेसिस और फाइब्रिनोलिसिस की प्रणाली घनास्त्रता और फाइब्रिनोपेप्टाइड के गठन को बढ़ावा देती है। वे रक्त वाहिकाओं की पारगम्यता को बढ़ाते हैं, परिजनों के गठन को उत्तेजित करते हैं। मध्यस्थों के तीसरे समूह में एराकिडोनिक एसिड के उत्पाद हैं - प्रोस्टाग्लैंडीन और ल्यूकोट्रिएनेस। पीजी लगभग सभी प्रकार की परमाणु कोशिकाओं द्वारा निर्मित होते हैं, लेकिन मुख्य रूप से ल्यूकोसाइट्स द्वारा। पीजी अन्य मध्यस्थों की कार्रवाई को बढ़ाते हैं या कमजोर करते हैं, प्लेटलेट एकत्रीकरण को रोकते या बढ़ाते हैं, रक्त वाहिकाओं को पतला या पतला करते हैं, और शरीर के तापमान को बढ़ाते हैं। ल्यूकोट्रिएन प्लेटलेट्स, बेसोफिल, एंडोथेलियल कोशिकाओं के झिल्ली में बनते हैं। वे ल्यूकोसाइट एकत्रीकरण, माइक्रोवस्कुलर ऐंठन, वृद्धि की पारगम्यता, ब्रोन्कोस्पास्म का कारण बनते हैं। मध्यस्थों के 4 वें समूह - ऑक्सीजन कट्टरपंथी और लिपिड हाइड्रोपरॉक्साइड्स। कोशिकाओं के माइटोकॉन्ड्रिया में, ऑक्सीजन के कट्टरपंथी जैसे कि हाइड्रोजन पेरोक्साइड, हाइड्रॉक्सिल रेडिकल, आदि बनते हैं। माइटोकॉन्ड्रिया के क्षतिग्रस्त होने पर, अम्लीय मूलक निकल जाते हैं, झिल्ली के लिपिड के साथ संपर्क करते हैं, जिससे लिपिड हाइड्रोक्लॉक्साइड बनते हैं। ऑक्सीजन रेडिकल और लिपिड हाइड्रोपरॉक्साइड की पीढ़ी के लिए प्रक्रियाओं का पूरा परिसर "ऑक्सीडेटिव सिस्टम" कहलाता है। सूजन के फोकस में, मुक्त कट्टरपंथी प्रक्रियाओं को सक्रिय किया जाता है और माइक्रोबियल और स्वयं की कोशिकाओं के झिल्ली को नुकसान पहुंचाता है। एक तथाकथित "ऑक्सीडेटिव विस्फोट" उत्पन्न होता है। यह फागोसाइट्स की जीवाणुनाशक गतिविधि का आधार है। इसके अलावा, कट्टरपंथी microvessels की पारगम्यता में वृद्धि करते हैं, प्रसार को उत्तेजित कर सकते हैं। मध्यस्थों का 5 वाँ समूह पॉलिमॉर्फोन्यूक्लियर ल्यूकोसाइट्स / पीएमएन / मोनोसाइट्स और लिम्फोसाइटों का मध्यस्थ है। पीएमएन अत्यधिक सक्रिय मध्यस्थों के एक समूह का उत्सर्जन करता है जो भड़काऊ फोकस में विभिन्न प्रतिक्रियाओं का कारण बनता है, इसकी अभिव्यक्तियों का निर्माण करता है। प्रतिनिधियों में से एक प्लेटलेट सक्रिय कारक / पीएएफ / है। यह वाहिकाओं की पारगम्यता को बढ़ाता है, प्लेटलेट एकत्रीकरण, ल्यूकोसाइट उत्सर्जन का कारण बनता है। इसके अलावा, ल्यूकोसाइट्स प्रोस्टाग्लान ई 2, ल्यूकोट्रिएनेस, थ्रोम्बोक्सेन ए 2 (रक्त के थक्के को बढ़ाता है, कोरोनरी वाहिकाओं को बढ़ाता है), प्रोस्टाइक्लिन (रक्त वाहिकाओं का विस्तार और रक्त के थक्के को कम करता है) जैसे मध्यस्थों का स्राव करता है। भड़काऊ दर्द की उत्पत्ति में प्रोस्ट्रोसाइक्लिन और ल्यूकोट्रियन महत्वपूर्ण हैं। मोनो-साइटेस और लिम्फोसाइट्स मोनोकिन्स और लिम्फोसाइट्स का स्राव करते हैं। उदाहरण के लिए, लिम्फोसाइट्स एक कारक को सिकोड़ते हैं जो मैक्रोफेज, मैक्रोफेज-उत्तेजक कारक को रोकता है। लिम्फोकेन्स सामान्य रूप से भड़काऊ प्रतिक्रिया को विनियमित करते हुए, न्युट्रोफेज, माइक्रोफेज और लिम्फोसाइटों की बातचीत का समन्वय करते हैं। सूजन के एंटीमेडिएटर्स सूजन के सभी चरणों में, पदार्थ जो मध्यस्थों के अत्यधिक संचय को रोकते हैं या मध्यस्थों के प्रभाव को रोकते हैं, जारी किए जाते हैं और कार्य करते हैं। ये मुख्य रूप से एंजाइम हैं: हिस्टामिन्स, कारबॉक्सपेप्टिडेस किनिन अवरोधक, पूरक अंश के एस्टरेज़ अवरोधक। इओसिनोफिल्स भड़काऊ फोकस के लिए विरोधी दवाओं के गठन और वितरण में एक महत्वपूर्ण भूमिका निभाते हैं। विनोदी विरोधी मध्यस्थों में, अल्फा-1-एंटीट्रिप्सिन द्वारा एक महत्वपूर्ण भूमिका निभाई जाती है, जो हेपेटोसाइट्स में बनती है। यह एक प्रोटीज अवरोधक है। परिभाषा से इस प्रकार है सूजन का दूसरा घटक सूजन के फोकस में माइक्रोकैरियुलेशन और हेमोरेहोलॉजी का उल्लंघन है। संचार विकारों के निम्नलिखित चरण प्रतिष्ठित हैं: 1. धमनी हाइपरमिया का गठन। 2. शिरापरक हाइपरिमिया का चरण, जो मिश्रित से गुजरता है। 3. अगला रक्त ठहराव आ सकता है। जल्दी से बनने वाली हिस्टामाइन, किनिन्स, प्रोस्टाग्लैंडिंस और अन्य भड़काऊ मध्यस्थ धमनियों, धमनियों को पतला करते हैं और धमनी हाइपरमिया के गठन को सुनिश्चित करते हैं। धमनी हाइपरिमिया के विकास में एक महत्वपूर्ण भूमिका और इसके रखरखाव के लिए पूर्व-खुराक की स्थिति में वाहिकाओं के अल्फा-एड्रेनोसेप्टर्स की संवेदनशीलता में परिवर्तन होता है। नतीजतन, एड्रेनालिन और सहानुभूति प्रभावों के लिए वाहिकाओं की प्रतिक्रिया में कमी होती है, जो धमनी और प्रीक्पिलरी स्फिंक्टर्स के विस्तार में योगदान करती है। एसिडोसिस के कारण सूजन के फोकस में, डिसियोनिया (ऊतक द्रव में K + आयनों की एकाग्रता में वृद्धि), प्रीस्किलर स्फिंक्टर्स का वासोकोनस्ट्रिक्टिव प्रभाव भी कम हो जाता है। ये सभी कारक धमनी हाइपरिमिया के गठन की ओर ले जाते हैं। धमनी हाइपरमिया को रक्त प्रवाह की मात्रा और रैखिक वेग में वृद्धि, कार्यशील केशिकाओं की संख्या की विशेषता है। ऑक्सीजन से भरपूर रक्त के प्रवाह में वृद्धि रेडॉक्स प्रक्रियाओं और गर्मी निर्माण की वृद्धि में योगदान करती है। इसलिए, धमनी हाइपरमिया के चरण में, ओकुलर सूजन में तापमान में वृद्धि सब्जेक्टली और ऑब्जेक्टिवली दर्ज की जाती है। जब सूजन रक्त वाहिकाओं की पारगम्यता को बढ़ाती है, जो सूजन के फोकस में प्रोटीन और पानी की रिहाई में योगदान करती है। सबसे पहले, एल्ब्यूमिन होते हैं, जिसके संबंध में रक्त में ग्लोब्युलिन और फाइब्रोजेन की मात्रा बढ़ जाती है। इससे चिपचिपाहट और रक्त की एकाग्रता में वृद्धि होती है, इसका परिणाम रक्त प्रवाह का धीमा होना और लाल रक्त कोशिकाओं के समुच्चय का बनना है। तरल पदार्थ के संचय के परिणामस्वरूप, और बाद में ऊतक में गठित तत्व, लसीका और रक्त वाहिकाएं संकुचित होती हैं, जिससे रक्त और लसीका के लिए बाहर निकलना मुश्किल हो जाता है। समान तत्वों का एकत्रीकरण, उनके चिपकाने और कीचड़ का निर्माण जहाजों में विकसित होता है। मिठाई के लिए, सिक्का स्तंभों के रूप में एरिथ्रोसाइट एकत्रीकरण विशेषता है। एक मीठा के साथ, एरिथ्रोसाइट झिल्ली टूट नहीं जाती है, इसलिए कीचड़ टूट सकता है। इसके समानांतर में, रक्त के थक्कों और थ्रोम्बोम्बोलिज़्म के गठन के साथ रक्त जमावट प्रणाली सक्रिय होती है। ये सभी परिवर्तन रक्त की गतिशील चिपचिपाहट को बढ़ाने और इसके rheological गुणों की गिरावट में योगदान करते हैं। इसके अलावा, माइक्रोथ्रोमबस गठन और रक्तस्राव का कारण संवहनी दीवार को सीधा नुकसान होता है, एक कारक जिसके कारण सूजन होती है, हेजमैन कारक की सक्रियता, मध्यस्थों की कार्रवाई / लाइसोसोमल एंजाइम, ब्रैडीकाइनिन, कैलिडिन /। रेड ब्लड सेल्स वाहिकाओं को इंटरेंडोथेलियल स्पेस के जरिए छोड़ते हैं। इस प्रकार, धमनी हाइपरमिया बहुत जल्दी शिरापरक में शामिल हो जाता है, जिनमें से अभिव्यक्तियां उत्तरोत्तर बढ़ती हैं। शिरापरक हाइपरिमिया के चरण में, सूजन के स्रोत से रक्त का बहिर्वाह परेशान होता है, रक्त प्रवाह के रैखिक और वॉल्यूमेट्रिक वेग में कमी आती है, हाइड्रोस्टेटिक दबाव बढ़ता है, और जॉग के आकार और पीडुलम जैसी रक्त प्रवाह विकसित होता है। सूजन और शिरापरक हाइपरिमिया के विकास के साथ, रक्त प्रवाह का एक और, प्रगतिशील धीमा हो जाता है। यह इसके कारण होता है: ए) केशिकाओं के अधिकतम फैलाव और नसों के खुलने के कारण संवहनी पृष्ठीय के पार-अनुभागीय क्षेत्र में अत्यधिक वृद्धि, बी) सूजन के फोकस से रक्त और लसीका के बहिर्वाह के लिए एक यांत्रिक बाधा, मुख्य रूप से शिरापरक और लसीका वाहिकाओं के संपीड़न के कारण होता है। ) इसका पालन करने वाले ल्यूकोसाइट्स की छोटी वाहिकाओं की आंतरिक दीवार की खुरदरापन के साथ-साथ एंडोथेलियल कोशिकाओं की सूजन के कारण रक्त के प्रवाह के प्रतिरोध में वृद्धि; डी) रक्त के और अधिक मोटा होना और बढ़ने के कारण इसकी चिपचिपाहट बढ़ जाती है; ऊतक में वाहिकाओं से तरल पदार्थ निकलने के बारे में। अंत में, रक्त आंदोलन का एक पड़ाव है - ठहराव। स्टैसिस को प्रारंभिक रूप से अलग केशिकाओं और वेन्यूल्स में दर्ज किया जाता है, बाद में यह अधिक से अधिक वाहिकाओं को कवर करता है। आखिरकार, ऐटेरियस में स्टैसिस विकसित होता है। सूजन की गंभीरता के आधार पर, ठहराव अल्पकालिक हो सकता है, घंटों तक बना रह सकता है या अपरिवर्तनीय हो सकता है। स्टैसिस का परिणाम रक्त कोशिकाओं और ऊतकों में अपरिवर्तनीय परिवर्तन हो सकता है। रसकर बहना रसकर बहना - यह सूजन के फोकस में रक्त के तरल भाग से बाहर निकलता है। इसे 3 तरीकों से किया जाता है: 1. इंटरेंडोथेलियल स्लिट्स के माध्यम से, जिसका आकार माइक्रोफाइबर एंडोथेलियल कोशिकाओं की कमी के कारण बढ़ता है। 2. विशेष चैनलों के माध्यम से एंडोथेलियल कोशिकाओं के शरीर के माध्यम से। 3. सेल शरीर के माध्यम से सबसे छोटी बूंदों को सक्रिय रूप से संचालित करने के रूप में माइक्रोप्रोसाइटोसिस मार्ग। भड़काऊ फ़ोकस में संवहनी दीवार की पारगम्यता बढ़ाने के दो चरणों की पहचान की गई है: 1. वैसोएक्टिव पदार्थों की कार्रवाई के कारण तुरंत संवहनी पारगम्यता बढ़ रही है। 2. पीएमएन-ल्यूकोसाइट्स की कार्रवाई से जुड़ी देर (देरी, लंबी)। ल्यूकोसाइट ग्रैन्यूल में जैविक रूप से सक्रिय पदार्थ होते हैं जो कि क्षरण और फैगोसाइटोसिस के दौरान जारी होते हैं। पीएमएन-ल्यूकोसाइट्स के संचय और उनके क्षरण की प्रक्रिया एक लंबी प्रक्रिया है। यही कारण है कि वे पारगम्यता बढ़ाने का दूसरा चरण प्रदान करते हैं। संवहनी पारगम्यता में वृद्धि निम्नलिखित कारकों के कारण होती है: 1. कारक की प्रत्यक्ष कार्रवाई (पशु जहर, बैक्टीरिया विषाक्त पदार्थों, आदि)। 2. एक बास (हिस्टामाइन, सेरोटोनिन, किनिन्स, आदि) की क्रिया 3. एसिडोसिस। यह कोलाइड के द्रवीकरण और इंटरेंडोथेलियल कनेक्शन को कमजोर करने की ओर जाता है। वाहिकाओं की बढ़ी हुई पारगम्यता में सूजन वाले क्षेत्र में प्रोटीन और रक्त तत्वों की रिहाई होती है। पानी और उसमें घुले पदार्थों का निकलना निम्न कारण है: 1. निस्पंदन क्षेत्र में वृद्धि और प्रसार। 2. केशिकाओं और venules में रक्तचाप में वृद्धि। 3. सूजन वाले ऊतक में आसमाटिक दबाव में वृद्धि। 4. लसीका शोफ। फुलाया हुआ ऊतक में जाने वाले द्रव को कहा जाता है ekssu- ल्युइगी डेटोम। इसमें बड़ी मात्रा में प्रोटीन (30-50 ग्राम / लीटर), रक्त कणिकाएं, क्षतिग्रस्त ऊतक की कोशिकाएं होती हैं। Noninflammatory exudate - transudate में बहुत कम प्रोटीन, रक्त कणिकाएं, क्षतिग्रस्त ऊतक की कोशिकाएं होती हैं। सूजन के दौरान प्रोटीन और पानी की रिहाई के समानांतर, ल्यूकोसाइट उत्सर्जन की प्रक्रिया आगे बढ़ती है। ल्यूकोसाइट उत्सर्जन ल्यूकोसाइट्स का निकास दीवार की गति और उनके खड़े होने से पहले होता है, जो विशेष रूप से शिरापरक हाइपरिमिया के चरण में स्पष्ट रूप से मनाया जाता है। इस घटना को ल्यूकोसाइट्स, निकट-दीवार माइक्रोकैग्यूलेशन के नकारात्मक चार्ज में कमी के द्वारा समझाया गया है, जिसके परिणामस्वरूप माइक्रोफ़िबर्स ल्यूकोसाइट्स के संचलन को रोकते हैं और उनके निकट-दीवार खड़े होने में योगदान करते हैं। अधिक II.Mechnikov ने उल्लेख किया कि पीएमएन-ल्यूकोसाइट्स सूजन में पहले दिखाई देते हैं, फिर मोनोसाइट्स और आखिरी लिम्फोसाइट्स। ल्यूकोसाइट्स दो तरीकों से निकलते हैं: पीएमएन-ल्यूकोसाइट्स इंटरेंडोथेलियल अंतराल के माध्यम से बाहर निकलते हैं, और एंडोथेलियल कोशिकाओं के शरीर के माध्यम से मोनोन्यूक्लियर कोशिकाएं। बाद की प्रक्रिया सबसे अधिक समय लेने वाली है और यह बताती है कि मोनोन्यूक्लियर कोशिकाएं बाद में सूजन वाले क्षेत्र में क्यों दिखाई देती हैं। रक्त तत्वों के तहखाने झिल्ली को कोलाइडल समाधान (थिक्सोट्रॉपी), यानी की चिपचिपाहट में एक आइसोथर्मल प्रतिवर्ती कमी के आधार पर दूर किया जाता है। जब ल्यूकोसाइट झिल्ली से जुड़ा होता है, तो जेल का सोल में संक्रमण। ल्यूकोसाइट, आसानी से सोल पर काबू पाने, पोत के बाहर हो जाता है, और झिल्ली फिर से एक जेल में बदल जाती है। इस प्रक्रिया में, एंजाइम शामिल होते हैं, और सभी कोलाज-नाज़ा के ऊपर। उत्प्रवास के अनुक्रम पर एक निश्चित प्रभाव में सूजन के स्रोत का पीएच है। पीएच 7.4-7.2 पर, पीएमएन-ल्यूकोसाइट्स जमा होता है, पीएच 7.0-6.8, मोनोन्यूक्लियर सेल, और पीएच 6.7 पर, सभी ल्यूकोसाइट्स मवाद के रूप में सूजन के निडस में मर जाते हैं। ल्यूकोसाइट्स के उत्प्रवास में महत्वपूर्ण रसायनोत-सिसु का है। यह पूरक की भागीदारी के साथ बनता है। पूरक के अवरोधकों का उपयोग जहाजों को नुकसान और ल्यूकोसाइट्स की रिहाई को रोकता है। केमोटैक्सिस को स्ट्रेप्टोकिनेस द्वारा उत्तेजित किया जाता है। जब चेमोटॉक्सिन दिखाई देते हैं यांत्रिक क्षति ऊतक, एंडोटॉक्सिन की कार्रवाई के कारण संक्रामक सूजन के साथ। गामा ग्लोब्युलिन के टूटने के दौरान लिम्फोसाइटों द्वारा केमोटोक्सिन भी बनते हैं। चेमोटैक्सिस ऊतकों, बैक्टीरिया, वायरस, और कैलिकेरिन प्रणाली के चयापचय उत्पादों से प्रेरित होता है। ल्यूकोसाइट्स के उत्प्रवास में एक निश्चित भूमिका तथाकथित सर्फेक्टेंट द्वारा निभाई जाती है, जो सतह के तनाव को कम कर सकती है। उदाहरण के लिए: कार्बनिक अम्ल। एक ल्युकोसैट की सतह के तनाव को बदलकर, वे बाद में साइटोप्लाज्मिक प्रोट्रूशियन्स विकसित करने और स्यूडोपोडिया का निर्माण करते हैं। धीरे-धीरे, पूरे ल्यूकोसाइट में चला जाता है, पूरी तरह से पोत से परे जा रहा है। वाहिकाओं से जारी ल्यूकोसाइट्स का भाग्य उस वातावरण पर निर्भर करता है जिसमें वे गिरते हैं। यदि सूजन प्रकृति में सड़न रोकनेवाला है, तो उत्सर्जित ल्यूकोसाइट्स जल्दी से मर जाते हैं 3-5 दिन। यदि सूजन में एक सेप्टिक चरित्र है, तो भड़काऊ फोकस में ल्यूकोसाइट्स की संख्या उत्तरोत्तर बढ़ रही है। दमन शुरू होता है। भड़काऊ फोकस के केंद्र में स्थित कुछ ल्यूकोसाइट्स मर जाते हैं। भाग फागोसाइटिक गतिविधि को दर्शाता है। एंजाइम गतिविधि बढ़ रही है: माइलोपरोक्सीडेज, एसिड हाइड्रॉलिस जो अतिरिक्त रूप से स्थित जीवाणुओं को नष्ट करते हैं। इस तथ्य के बावजूद कि बैक्टीरियल पट्टिका सूजन पीरियडोंटल रोगों के विकास का प्राथमिक कारण है, केवल इसका प्रभाव पीरियडोंटल विनाश की गंभीरता को स्पष्ट नहीं कर सकता है। शरीर की प्रतिक्रिया विकास में महत्वपूर्ण भूमिका निभाती है periodontal रोग। मानव शरीर में अन्योन्याश्रित सुरक्षात्मक तंत्र का एक जटिल समूह है, जिसका उद्देश्य सूक्ष्मजीवों को खत्म करना, चिकित्सा प्राप्त करना और एक स्वस्थ अवस्था बनाए रखना है। विरोधाभासी रूप से, एक ही प्रणाली, जिसे शरीर की रक्षा और चंगा करने के लिए डिज़ाइन किया गया है, पीरियडोंटल रोगों में ऊतक क्षति की ओर जाता है। इम्यूनोलॉजी एक अत्यंत जटिल विषय है। इसके अलावा, भड़काऊ और प्रतिरक्षा प्रतिक्रिया के रूप में ऐसी धारणाओं को अलग करना मुश्किल है, क्योंकि कई स्थितियों में उनकी कार्रवाई एक-दूसरे को ओवरलैप करती है। यह अध्याय भड़काऊ और प्रतिरक्षा प्रतिक्रिया की अभिव्यक्तियों का एक सिंहावलोकन प्रदान करता है, साथ ही साथ पीरियडोंटल बीमारी के उपचार और विनाश में उनकी भूमिका। निम्नलिखित विषयों को कवर किया जाएगा:
सूजन सूजन उन घटनाओं का एक स्पष्ट अनुक्रम है जो किसी भी क्षति या संक्रमण के जवाब में विकसित होती हैं, इस प्रकार, "गैर-विशिष्ट" चरित्र होता है। सूजन एक प्राथमिक प्रतिक्रिया है जो प्रतिरक्षा प्रणाली की सक्रियता से पहले होती है। सूजन की प्रक्रिया तीन चरणों की विशेषता है:
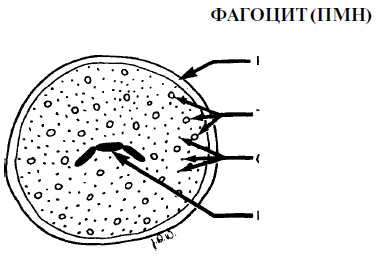
इससे पहले कि हम स्वयं इस प्रक्रिया पर चर्चा करना शुरू करें, हम सूजन के मुख्य सेलुलर और आणविक तत्वों को प्रस्तुत करते हैं। सूजन के सेलुलर तत्व सूजन के लिए जिम्मेदार मुख्य कोशिकाएं ल्यूकोसाइट्स (पीएमएन) हैं, जो एक ही स्टेम सेल से मोनोसाइट्स के रूप में अस्थि मज्जा में बनती हैं। कोशिका की सतह के विशिष्ट मार्कर यह निर्धारित करते हैं कि मैक्रोफेज या पीएमएन के गठन के मार्ग के साथ-साथ कौन से पथ प्रोमीलोसाइट्स के विकास को बढ़ावा देगा। ये मार्कर विभेदन के पूरा होने के बाद गायब हो जाते हैं। संलग्न उपकला में कई पीएमएन की उपस्थिति को सामान्य माना जाता है। उनकी संख्या में वृद्धि जीव की प्रतिक्रिया की दीक्षा का संकेत है। पीएमएन फागोसाइट्स हैं और ल्यूकोसाइट्स की कुल संख्या का 70% बनाते हैं। पीएमएन के साइटोप्लाज्म में ऐसे तत्व होते हैं जो किमोटैक्सिस सक्रियण के दौरान कोशिकाओं की गति के लिए जिम्मेदार होते हैं, साथ ही लाइसोसोम भी होते हैं जो बैक्टीरिया को नष्ट करते हैं। इन कोशिकाओं द्वारा बैक्टीरिया का विनाश आमतौर पर, लेकिन हमेशा नहीं होता है, क्योंकि सूक्ष्मजीव पीएमएन (यानी, फागोसाइटोसिस के बाद) द्वारा अवशोषित होते हैं। भड़काऊ प्रतिक्रिया में शामिल अगली कोशिकाएं मैक्रोफेज हैं, जो परिसंचारी मोनोसाइट्स से बनती हैं, और पीएमएन के बाद सूजन के क्षेत्र में दिखाई देती हैं। मैक्रोफेज बड़ी कोशिकाएं होती हैं, जिनमें पीएनजी के समान फागोसिटिक क्षमता होती है। इसके अलावा, मैक्रोफेज प्रतिरक्षा प्रतिक्रिया में एक महत्वपूर्ण भूमिका निभाते हैं। लिम्फोसाइट्स सूजन के क्षेत्र में अंतिम रूप से प्रवेश करते हैं और मुख्य रूप से जुड़े होते हैं पुरानी सूजन। इसके अलावा, लिम्फोसाइट्स प्रतिरक्षा प्रणाली की मुख्य कोशिकाएं हैं। मास्ट कोशिकाएं बेसोफिल के घूमने के समान होती हैं। वे हिस्टामाइन, प्लेटलेट सक्रिय करने वाले कारक (पीएएफ), प्रोस्टाग्लैंडीन ई 2 और ल्यूकोट्रिएन (एलटीबी 4 और लिमिटेड 4) को छोड़ते हैं, इनमें से प्रत्येक तत्व का एक भड़काऊ प्रभाव है। प्लेटलेट्स सेरोटोनिन (सूजन का एक महत्वपूर्ण मध्यस्थ) जारी करते हैं। सूजन के आणविक घटक हिस्टामाइन रक्त वाहिका की दीवारों की पारगम्यता को बढ़ाता है, इस प्रकार प्रभावित क्षेत्र में भड़काऊ कोशिकाओं की पहुंच को सुविधाजनक बनाता है। हिस्टामाइन को मस्तूल कोशिकाओं और बेसोफिल द्वारा जारी किया जाता है। सेरोटोनिन (5-हाइड्रोक्सी-ट्रिप्टामाइन) भी संवहनी पारगम्यता को बढ़ाता है। बेसोफिल, न्युट्रोफिल और मैक्रोफेज प्लेटलेट सक्रिय करने वाले कारक (पीएएफ) को छोड़ते हैं। पीएएफ प्लेटलेट्स से सेरोटोनिन की रिहाई को बढ़ाता है। न्युट्रोफिल केमोटैक्सिस फैक्टर (NCF) मस्तूल कोशिकाओं से मुक्त होता है और PMN केमोटैक्सिस को नियंत्रित करता है। ल्यूकोसाइट्स द्वारा केमोकिंस जारी किए जाते हैं। वे साइटोकिन्स के एक बड़े समूह का गठन करते हैं जो मस्तूल सेल गिरावट और पीएमएन केमोटैक्सिस का कारण बनते हैं। चेतावनी: शब्दावली भ्रामक लग सकती है। सभी अणु जो प्रतिरक्षा या भड़काऊ प्रतिक्रिया को प्रभावित करते हैं, साइटोकिन्स कहलाते हैं। इसके अनुरूप, सभी केमोकिंस साइटोकिन्स होते हैं, लेकिन बड़ी संख्या में साइटोकिन्स होते हैं जो कि केमोकाइन नहीं होते हैं। सक्रिय पूरक SZ मस्तूल सेल गिरावट का कारण बनता है। सक्रिय पूरक C5a मस्तूल सेल की गिरावट, फैगोसाइट कैमोटेक्सिस, पीएमएन सक्रियण और केशिका पारगम्यता में वृद्धि की ओर जाता है। ब्रैडीकिनिन (किनिन प्रणाली का एक तत्व) वासोडिलेशन का कारण बनता है और संवहनी पारगम्यता को बढ़ाता है। फाइब्रिनोपेप्टाइड्स जमावट तंत्र के उत्पाद हैं और पीएमएन और मैक्रोफेज के केमोटैक्सिस को प्रभावित करते हैं। प्रोस्टाग्लैंडीन E2 (PGE2) साइक्लोऑक्सीजिनेज का एक उत्पाद है और हिस्टामाइन और ब्रैडीकाइनिन की कार्रवाई के तहत संवहनी पारगम्यता में वृद्धि के साथ-साथ वासोडिलेशन का कारण बनता है। ल्यूकोट्रिएन बी 4 (एलटीबी 4) का निर्माण लाइपोक्सिनेज चक्र के दौरान होता है। यह PMN केमोटैक्सिस को उत्तेजित करता है और PGE2 के साथ सहक्रियाशील रूप से संवहनी दीवार की पारगम्यता में वृद्धि की ओर जाता है। Leukotriene D4 (LTD4), जो कि लाइपोक्सिनेज चक्र के दौरान भी बनता है, संवहनी पारगम्यता को बढ़ाता है। न्यूट्रोफिल केमोटैक्सिस फैक्टर (NCF) बेसोफिल द्वारा जारी किया जाता है। Selectins तीन अणुओं का एक समूह है जो संवहनी दीवार के माध्यम से PMN और मैक्रोफेज के प्रवास को सुविधाजनक बनाता है। Selectin E और Selectins P PMN के लिए विशिष्ट हैं, और Selectin L मैक्रोफेज के लिए है। चयनकर्ता कोशिकाओं की गति को धीमा कर देते हैं, जो बाद की पोत की दीवार के आसंजन में योगदान देता है। आईसीएएमएस के रूप में जाना जाने वाले समूह सहित तीन समूहों में कम से कम 12 अणु शामिल हैं जो समान कार्य करते हैं। पीरियडोंटल रोगों में तीव्र सूजन जैसा कि ऊपर उल्लेख किया गया है, तीव्र सूजन की प्रक्रिया में तीन चरण शामिल हैं। जैसे कि बैक्टीरिया का फलक नाली में जम जाता है, निम्नलिखित घटनाएं घटित होती हैं। प्रभावित क्षेत्र में रक्त वाहिकाओं के विस्तार के कारण रक्त की आपूर्ति बढ़ जाती है। कुछ मध्यस्थ वासोडिलेशन का कारण बनते हैं, उदाहरण के लिए हिस्टामाइन और PGE2। सेरोटोनिन, C5a, ब्रैडीकाइनिन, फाइब्रिनोपेप्टाइड्स, PGE2, LTB2 और LTD2 संवहनी दीवार की पारगम्यता को बढ़ाते हैं और एंडोथेलियल कोशिकाओं के बीच स्थान को बढ़ाते हैं। चयनकर्ताओं और आईसीएएमएस ने पीएमएन के आंदोलन को धीमा कर दिया, जिससे उत्तरार्द्ध में प्रवेश करने की अनुमति मिली संयोजी ऊतक। PMN के प्रवासन और फागोसिटिक फ़ंक्शन को NCF जैसे किमोटैक्टिक कारकों द्वारा नियंत्रित किया जाता है। केमोकाइन्स, C5a, फाइब्रिनोपेप्टाइड्स और LTB4 भी न्युट्रोफिल फैगोसाइटोसिस और केमियाक्सिस में योगदान करते हैं। संक्रामक आक्रमण के लिए शरीर की प्रतिक्रिया में शामिल होने वाली मुख्य फैगोसाइटिक कोशिकाएं पॉलीमोर्फोन्यूक्लियर न्यूट्रोफिल और मैक्रोफेज हैं। सूक्ष्मजीवों का विनाश, आमतौर पर, लेकिन हमेशा नहीं, कोशिकाओं द्वारा उनके अवशोषण के बाद होता है। कुछ कोशिका झिल्ली को नुकसान उन कारकों के गठन और रिलीज को जन्म दे सकता है जो सूजन के नैदानिक लक्षणों की शुरुआत की ओर ले जाते हैं।
ग्यारह शास्त्रीय प्रोटीन
कणिकाओं को लाइसोसोम या "आत्मघाती पैकेट भी कहा जाता है।" जीवाणु कोशिकाओं और शरीर की कोशिकाओं को नष्ट करने वाले एंजाइम फ़ैगोसाइट ऑक्सीजन-स्वतंत्र फागोसाइटोसिस यह प्रक्रिया बड़ी संख्या में विनाशकारी पदार्थों की कार्रवाई के परिणामस्वरूप होती है जो ऑर्गेनेल में निहित हैं जो फागोसाइट्स के साइटोप्लाज्म में स्थित हैं। ऐसे जीवों को ग्रैन्यूल या लाइसोसोम कहा जाता है। एंजाइमों की विनाशकारी गतिविधि ग्रैन्यूल्स और अन्य कारकों की सामग्री की रिहाई की ओर ले जाती है जो कि cationic प्रोटीन, तटस्थ प्रोटीज, एसिड हाइड्रॉलिसिस के साथ-साथ अन्य पदार्थों, जैसे लैक्टोफेरिन के समूह से संबंधित हैं। फागोसाइट्स द्वारा अवशोषित होने के बाद एंजाइम बैक्टीरिया को नष्ट कर देते हैं। हालांकि, फ़ैगोसाइटोसिस की प्रक्रिया में, कुछ एंजाइम फ़ैगोसाइट से "रिसाव" कर सकते हैं और सेल के आसपास की संरचनाओं के साथ बातचीत कर सकते हैं। संभवतः, इस घटना का एक खांचे या जेब के तरल पदार्थ में बहुत महत्व है, जहां बैक्टीरिया का विनाश बिना पूर्व अवशोषण के शुरू होता है, जो पीरियडोंटल ऊतकों की सुरक्षा में योगदान देता है। इसके अलावा, लाइसोसोमल एंजाइम बैक्टीरिया द्वारा संश्लेषित और जारी किए गए विनाशकारी एंजाइमों और विषाक्त पदार्थों की कार्रवाई को बेअसर करने में एक महत्वपूर्ण भूमिका निभा सकते हैं, भले ही इन एंजाइमों और विषाक्त पदार्थों को पहले फागोसाइट्स द्वारा अवशोषित किया गया था। ऑक्सीजन पर निर्भर फागोसाइटोसिस यह प्रक्रिया कोशिका अंग के अंदर स्थित जीवाणुओं के विनाश की ओर ले जाती है, जिसे फैगोलिसोसोम कहा जाता है। इसके दौरान, ऑक्सीजन ऑक्सीडेंट और लाइसोसोमल एंजाइम मायलोपरोक्सीडेज से विषाक्त ऑक्सीडेंट और हाइड्रोजन पेरोक्साइड निकलते हैं, जो बैक्टीरिया की कोशिकाओं को बड़े पैमाने पर उनकी कोशिका दीवार को नुकसान पहुंचाते हैं। कई अध्ययनों के दौरान, पॉलीमॉर्फोन्यूक्लियर न्यूट्रोफिल (पीएमएन) और पेरियोडोंटल ऊतकों की स्थिति के बीच संबंध का अध्ययन किया गया है। पीरियोडॉन्टल रोग मनुष्यों या जानवरों में न्यूट्रोफिल की उपस्थिति में अधिक सामान्य और अधिक गंभीर होते हैं, जैसे कि एग्रानुलोसाइटोसिस या ल्यूकोसाइट आसंजन विफलता। पीएमएन की संख्या में कमी या जन्मजात अपर्याप्तता वाले जानवरों में, तीव्र पीरियडोंटल विनाश और दांतों का नुकसान हुआ। बड़ी संख्या में रोगियों को शामिल नैदानिक अध्ययनों से पता चला है कि मरीजों में पीएमएन के कार्यात्मक अपर्याप्तता की उपस्थिति पीरियडोंटल ऊतकों के विनाश के लिए एक उच्च जोखिम कारक है। 1996 में, इंटरनेशनल कांग्रेस ऑफ पैरोडोन्टोलॉजी में, ऑफ़ेंबैकर ने सुझाव दिया कि सामान्य पीएमएन वाले रोगियों में बैक्टीरिया के भार की डिग्री की परवाह किए बिना, मसूड़े की सूजन होने की संभावना है, लेकिन पीरियंडोंटाइटिस नहीं। दूसरी ओर, ज्यादातर मामलों में पीएमएन के कार्यात्मक अपर्याप्तता की उपस्थिति अनुलग्नक के नुकसान के साथ होती है। इन अध्ययनों के निष्कर्ष बताते हैं कि पीएमएन एक स्वस्थ पीरियडोंटल स्थिति को सुनिश्चित करने में महत्वपूर्ण भूमिका निभाता है, लेकिन पीरियडोंटल ऊतकों के विनाश का कारण बन सकता है। शरीर के ऊतकों का विनाश यह सर्वविदित है कि पीरियडोंटल रोगों के विकास के दौरान शरीर अपने स्वयं के ऊतकों का एक महत्वपूर्ण विनाश होता है। इस तरह की क्षति को क्रोनिक की उपस्थिति में एक रोग संबंधी प्रतिक्रिया के रूप में माना जा सकता है सूजन की बीमारी। निम्नलिखित पदार्थों में बैक्टीरिया और उनके चयापचय उत्पादों के खिलाफ शरीर की रक्षात्मक प्रतिक्रिया की प्रक्रिया में पीरियडोंटल ऊतकों को नष्ट करने की क्षमता होती है।
सीरम पूरक प्रणाली सीरम पूरक प्रणाली में 20 से अधिक मट्ठा प्रोटीन होते हैं, जो सक्रिय होने पर जैविक गतिविधि के अधिकारी होते हैं। यह प्रणाली भड़काऊ और प्रतिरक्षा प्रतिक्रिया में एक अत्यंत महत्वपूर्ण भूमिका निभाती है। पूरक प्रणाली के प्रोटीन के सक्रियण के दो मुख्य तंत्र हैं। जीवाणु की दीवार की सतह पर एंटीबॉडी बांधने के बाद पहला क्लासिक तंत्र सक्रिय होता है। दूसरे वैकल्पिक तंत्र को कुछ ग्राम-नकारात्मक जीवाणुओं की दीवार के घटकों द्वारा सीधे सक्रिय किया जा सकता है। ऐसे घटकों को एंडोटॉक्सिन कहा जाता है। नीचे कई सीरम पूरक सक्रियण कारकों में से कुछ हैं जो दोनों तंत्रों में शामिल हैं।
सीरम पूरक प्रणाली में जैविक रूप से सक्रिय कारक पीरियोडॉन्टल ऊतकों के माइक्रोबियल आक्रमण के खिलाफ शरीर की रक्षा करने में महत्वपूर्ण भूमिका निभाने की संभावना रखते हैं, क्योंकि वे बैक्टीरिया के विनाश और अन्य रक्षा तंत्रों की शुरूआत करते हैं जो सूक्ष्मजीवों की एकाग्रता को कम करते हैं। जैसा कि सभी सुरक्षात्मक तंत्रों के साथ होता है जब पूरक सक्रिय होता है, तो पीरियडोंटल ऊतकों को नुकसान होने की संभावना होती है। इस अध्याय के अंत में पूरक द्वारा प्रेरित एंटीबॉडी और फागोसाइट्स द्वारा पेरियोडोंटल ऊतकों को नुकसान की ख़ासियत की चर्चा होगी। हालांकि, इसके अलावा, पूरक प्रणाली की सक्रियता के कारण, शरीर की अपनी कोशिकाओं, विशेष रूप से लाल रक्त कोशिकाओं के झिल्ली का विनाश हो सकता है। पूरक के सक्रियण से पीरियडोंटल ऊतकों का विनाश हो सकता है, जो रोग के नैदानिक लक्षणों को निर्धारित करता है। इम्मुनोलोगि परंपरागत रूप से, हम प्रतिरक्षा प्रणाली के दो हिस्सों पर विचार करते हैं: सेलुलर प्रतिरक्षा और हास्य प्रतिरक्षा। इस तरह के अलगाव की शीघ्रता के बावजूद, प्रतिरक्षाविज्ञानी वर्तमान में चिह्नित करने की कोशिश कर रहे हैं प्रतिरक्षा प्रणाली ऐसे तत्वों द्वारा जो सेलुलर एंटीजन को पहचानते हैं, और ऐसे तत्व जो फ्री एंटीजन को पहचानते हैं। प्रतिरक्षा प्रणाली के सेलुलर तत्व
साइटोकिन्स और अन्य आणविक तत्व साइटोकिन्स गैर-एंटीबॉडी अणु होते हैं जो प्रतिरक्षा और भड़काऊ प्रतिक्रिया के कई घटकों को प्रभावित करने की क्षमता रखते हैं, जैसे कि तारीफ कैस्केड, ब्रैडीकाइनिन, जमावट प्रक्रिया और एराकिडोनिक एसिड कैस्केड। सबसे महत्वपूर्ण साइटोकिन्स में शामिल हैं:
इम्युनोग्लोबुलिन (एंटीबॉडी)
पीरियडोंटल बीमारी में प्रतिरक्षा प्रतिक्रिया नाली के क्षेत्र में जीवाणु पट्टिका के संचय के साथ, समय की एक छोटी अवधि (आमतौर पर कई दिन) गुजरती है, जिसके दौरान एंटीबॉडी का पता नहीं लगाया जाता है। कुछ दिनों के बाद, शरीर बैक्टीरिया और उनके चयापचय उत्पादों की उपस्थिति पर प्रतिक्रिया करना शुरू कर देता है। फाइब्रोब्लास्ट्स, मैक्रोफेज और लिम्फोसाइट्स IL-1, IL-2, IL-6 और IL-8 छोड़ते हैं। सेलेक्टिन्स और 1C AM का सक्रियण होता है, जो डायफेडिसिस (संवहनी दीवार के माध्यम से छिद्र), पॉलीमोर्फोन्यूक्लियर ल्यूकोसाइट्स का माइग्रेशन और कीमोआटैक्सिस की शुरुआत करता है। डायापीसिस की प्रक्रिया में तेजी आती है, और PMN के बाद मैक्रोफेज होता है। दोनों सेल प्रकार साइटोकिन्स द्वारा सक्रिय होते हैं। नैदानिक रूप से, यह मसूड़े की सूजन के साथ प्राथमिक लाली द्वारा प्रकट होता है। एंटीजन को टी हेल्पर कोशिकाओं का उपयोग करके बी कोशिकाओं और मोनोसाइट्स को "वितरित" किया जाता है। अंत में, साइटोकिन्स जारी किए जाते हैं। यह बी कोशिकाओं के उत्पादन की ओर जाता है, जो प्रत्येक एंटीजन के लिए विशिष्ट एंटीबॉडी बनाते हैं। एंटीजन ओप्सोनेशन और फागोसाइटोसिस से गुजरते हैं, जिसके परिणामस्वरूप पदार्थों की रिहाई होती है जो कोलेजन और मुख्य पदार्थ को नुकसान पहुंचाते हैं। SZa और C5a मस्तूल कोशिकाओं द्वारा हिस्टामाइन की रिहाई का नेतृत्व करते हैं, यह वासोडिलेशन का कारण बनता है और बड़ी संख्या में सुरक्षात्मक कोशिकाओं के इच्छुक क्षेत्र में प्रवास की सुविधा प्रदान करता है। अंत में, खांचे के उपकला में अल्सर होता है, जो बैक्टीरियल एंटीजन के एक भी तेजी से प्रवेश में योगदान देता है। इस बिंदु पर, मसूड़े सूज जाते हैं, खून बहता है और थोड़ा दर्द हो सकता है। फाइब्रोब्लास्ट्स, पीएमएन और अन्य कोशिकाओं द्वारा उत्पादित साइटोकिन्स एक सुरक्षात्मक और हानिकारक भूमिका निभा सकते हैं। प्रभावित क्षेत्र में लिम्फोसाइटों और प्लाज्मा कोशिकाओं के साथ घुसपैठ की जाती है। उपचार की अनुपस्थिति में या रक्षा तंत्र की अपर्याप्तता के मामले में, बैक्टीरिया की कार्रवाई के परिणामस्वरूप लगाव का नुकसान होता है, और एक जीवाणु अड़चन के लिए शरीर की प्रतिक्रिया के परिणामस्वरूप। निष्कर्ष शरीर के बैक्टीरिया और रक्षा तंत्र के बीच स्वास्थ्य की स्थिति में संतुलन होता है। रोग के विकास के साथ यह संतुलन गड़बड़ा जाता है, बैक्टीरिया और शरीर के बैक्टीरिया को नष्ट करने और इलाज के प्रयासों से, पीरियडोंटल ऊतकों के विनाश का कारण बनता है। इस तरह के असंतुलन के कारण हो सकता है कि वायरल कारकों, रक्षा तंत्र या बाहरी कारकों की कार्रवाई, उदाहरण के लिए, तंबाकू धूम्रपान के प्रभाव में। पीरियोडॉन्टल अल्फाबेट |
| पढ़ें: |
|---|
सबसे लोकप्रिय:
बिर्च लटका या मस्सा
|
नई
- सौंदर्य प्रसाधनों की छाल पर त्वचा के गहन मॉइस्चराइजिंग का कार्यक्रम
- आपको ऐक्रेलिक पाउडर की क्या आवश्यकता है
- उल्लू शुभंकर का क्या अर्थ है
- अग्नाशयशोथ के लिए विश्लेषण: क्या शोध किया जाना चाहिए और क्या संकेतक दिखाते हैं
- उल्लू - धन और अच्छी किस्मत को आकर्षित करने के लिए एक ताबीज
- बिल्ली के बच्चे की आवाज़ से रात में कौन सा पक्षी चिल्लाता है?
- कोलेस्ट्रॉल और तनाव
- घर पर मैनीक्योर
- प्रभावी चेहरे
- टूटे पैर के बाद एक आदमी क्या है?