Sezioni del sito
Scelta dell'editore:
- Macchie bianche sulle unghie, motivi per cosa fare, macchie bianche sulle unghie e segni popolari
- Metodi disponibili per aumentare rapidamente i leucociti del sangue
- Il fungo del chiodo e della pelle non resisterà ai fondi di caffè
- Mostra di mobili Crocus. Mostre di mobili
- Tatuaggio del gufo sul valore del braccio
- I più grandi membri del mondo
- Fratture delle falangi della foto del piede
- Che cos'è il colesterolo "cattivo" e "buono"
- Cosa fare se la pelle intorno alle unghie si asciuga
- La più sicura lista di vernici naturali
pubblicità
| Ruolo patogenetico della risposta infiammatoria. Mediatori infiammatori: classificazione |
|
La comparsa di processi infiammatori in risposta all'azione di un fattore patologico è una risposta adeguata del corpo. L'infiammazione è un processo complesso che si sviluppa a livello locale o generale, che si manifesta in risposta all'azione di agenti stranieri. Il compito principale dello sviluppo risposta infiammatoria mira ad eliminare gli effetti patologici e ripristinare il corpo. I mediatori infiammatori sono mediatori direttamente coinvolti in questi processi. Brevemente sui principi delle reazioni infiammatorieIl sistema immunitario è il guardiano della salute umana. Quando necessario, entra in battaglia e distrugge batteri, virus e funghi. Tuttavia, con l'intensificazione intensificata del lavoro, il processo di lotta contro i microrganismi può essere visto visivamente o sentire l'aspetto del quadro clinico. È in questi casi che l'infiammazione si sviluppa come risposta protettiva del corpo. C'è un processo acuto di reazione infiammatoria e il suo corso cronico. Il primo si verifica a causa dell'azione improvvisa di un irritante (trauma, ferita, effetti allergici, infezione). L'infiammazione cronica ha una natura protratta e segni clinici meno pronunciati. Nel caso di una risposta locale del sistema immunitario nella zona di ferita o lesione, compaiono i seguenti segni di una reazione infiammatoria:
Stadio di sviluppo dell'infiammazioneIl processo di infiammazione si basa sull'interazione simultanea di fattori protettivi della pelle, del sangue e delle cellule immunitarie. Immediatamente dopo il contatto con un agente estraneo, il corpo risponde con un'espansione locale dei vasi sanguigni nella zona del trauma diretto. C'è un aumento della permeabilità delle loro pareti e un aumento della microcircolazione locale. Insieme alle cellule del flusso sanguigno di protezione umorale, vieni qui. Nel secondo stadio, le cellule immunitarie iniziano a combattere contro i microrganismi che si trovano nel luogo della lesione. Inizia il processo chiamato fagocitosi. Le cellule di neutrofili cambiano forma e assorbono agenti patologici. Successivamente, ci sono sostanze speciali volte alla distruzione di batteri e virus. In parallelo con i microrganismi, i neutrofili distruggono le vecchie cellule morte situate nella zona di infiammazione. Quindi, inizia lo sviluppo della terza fase della reazione dell'organismo. Il punto focale dell'infiammazione è come se fosse protetto da tutto il corpo. A volte in questo luogo si può sentire una pulsazione. I mediatori infiammatori cellulari cominciano a essere prodotti. mastocitiche consente di pulire l'area lesa da tossine, scorie e altre sostanze.
Concetti generali sui mediatoriI mediatori infiammatori sono sostanze attive di origine biologica, il cui rilascio è accompagnato dalle principali fasi di alterazione. Sono responsabili per il verificarsi di reazioni infiammatorie. Ad esempio, aumento della permeabilità delle pareti dei vasi o un aumento locale della temperatura nell'area del trauma. I principali mediatori dell'infiammazione si distinguono non solo per lo sviluppo del processo patologico. La loro produzione avviene costantemente. Ha lo scopo di regolare le funzioni del corpo a livello cellulare e cellulare. A seconda della direzione di azione, i modulatori hanno l'effetto:
Con l'apparenza di danni o nel luogo di azione dei microrganismi, il link del mediatore controlla i processi di interazione degli effettori infiammatori e il cambiamento delle fasi caratteristiche del processo. Tipi di mediatori dell'infiammazioneTutti i modulatori infiammatori sono divisi in due grandi gruppi, a seconda della loro origine:
I mediatori dell'infiammazione umorale si trovano nel corpo umano prima dell'esposizione a un fattore patologico, cioè il corpo ha una scorta di queste sostanze. La loro deposizione avviene nelle cellule in una forma inattiva. Ammine vasoattivo, neuropeptidi e fattori lisosomiali sono anche modulatori preesistenti. Le restanti sostanze appartenenti al gruppo di mediatori cellulari vengono prodotte direttamente durante lo sviluppo della risposta infiammatoria.
Derivati complementariI mediatori dell'infiammazione sono derivati del complimento. Questo gruppo di sostanze biologicamente attive è considerato il più importante tra i modulatori umorali. I derivati comprendono 22 diverse proteine, la cui formazione si verifica quando viene attivato il complemento (la formazione di un immunocomplesso o di immunoglobuline).
Questo gruppo di mediatori è prodotto da fluido plasmatico e tissutale. A causa dell'ingresso nella zona patologica, si verificano processi di essudazione. Con l'aiuto di derivati del complemento vengono rilasciati interleuchina, neurotrasmettitori, leucotrieni, prostaglandine e fattori attivanti piastrinici. chinineQuesto gruppo di sostanze è un vasodilatatore. Si formano nel tessuto fluido e plasma da specifiche globuline. I principali rappresentanti del gruppo sono bradykinin e kallidin, il cui effetto si manifesta come segue:
L'azione della bradichinina è finalizzata ad aprire l'accesso del plasma sanguigno al sito di infiammazione. Le kinin sono mediatori del dolore dell'infiammazione. Irritano i recettori locali, causando disagio, sensazione dolorosaPrurito. prostaglandineI mediatori cellulari dell'infiammazione sono le prostaglandine. Questo gruppo di sostanze appartiene ai derivati dell'acido arachidonico. Le fonti di prostaglandine sono macrofagi, piastrine, granulociti e monociti.
Le prostaglandine sono mediatori infiammatori che esibiscono la seguente attività:
leucotrieniRelativo ai mediatori appena formati. Cioè, nel corpo in uno stato di riposo del sistema immunitario, il loro numero non è sufficiente per una risposta immediata a un fattore fastidioso. I leucotrieni provocano un aumento della permeabilità della parete vascolare e l'accesso aperto ai globuli bianchi nell'area della patologia. La materia nella genesi del dolore infiammatorio. Le sostanze possono essere sintetizzate in tutte le cellule del sangue, ad eccezione dei globuli rossi, così come nell'avventizia delle cellule polmonari, dei vasi sanguigni e dei mastociti. In caso di sviluppo processo infiammatorio in risposta a batteri, virus o fattori allergici, i leucotrieni causano broncospasmo, innescando lo sviluppo di edema. L'effetto è simile all'azione dell'istamina, ma più lungo. L'organo bersaglio per le sostanze attive è il cuore. Distinguendosi in gran numero, agiscono sul muscolo cardiaco, rallentano il flusso sanguigno coronarico e aumentano il livello della risposta infiammatoria. trombossaniQuesto gruppo di modulatori attivi si forma nei tessuti della milza, delle cellule cerebrali, dei polmoni e delle cellule del sangue nelle piastrine. Hanno un effetto spastico sui vasi, aumentano i processi di trombosi durante l'ischemia cardiaca, contribuiscono ai processi di aggregazione e adesione delle piastrine. Ammine biogenicheMediatori infiammatori primari - istamina e serotonina. Le sostanze sono provocatori dei disordini iniziali del microcircolo nell'area della patologia. La serotonina è un neurotrasmettitore che viene prodotto nei mastociti, negli enterocromi e nelle piastrine. L'azione della serotonina varia con il suo livello nel corpo. In condizioni normali, quando la quantità del mediatore è fisiologica, aumenta lo spasmo dei vasi e aumenta il loro tono. Con lo sviluppo di reazioni infiammatorie, il numero aumenta drammaticamente. La serotonina diventa un vasodilatatore, aumentando la permeabilità della parete vascolare e espandendo i vasi sanguigni. Inoltre, la sua azione è cento volte più efficace del secondo neurotrasmettitore di ammine biogeniche.
L'istamina è un mediatore dell'infiammazione che ha un effetto diverso sui vasi sanguigni e sulle cellule. Agendo su un gruppo di recettori sensibili all'istamina, la sostanza dilata le arterie e inibisce il movimento dei leucociti. Quando esposto a un altro, si restringe le vene, provoca un aumento della pressione intra-capellare e, al contrario, stimola il movimento dei globuli bianchi. Agendo sui recettori dei neutrofili, l'istamina limita la loro funzionalità, sui recettori dei monociti - stimola il secondo. Pertanto, il neurotrasmettitore può avere contemporaneamente un effetto antinfiammatorio infiammatorio. L'effetto vasodilatatore dell'istamina viene potenziato sotto l'influenza di un complesso con acetilcolina, bradichinina e serotonina. Enzimi lisosomialiI mediatori dell'infiammazione immunitaria sono prodotti da monociti e granulociti nel sito del processo patologico durante la stimolazione, l'emigrazione, la fagocitosi, il danno cellulare e la morte. Proteinasi, che sono il componente principale degli enzimi lisosomiali, hanno un'azione antimicrobica, lisando microrganismi patogeni estranei. Inoltre, i principi attivi aiutano ad aumentare la permeabilità delle pareti vascolari, modulano l'infiltrazione dei leucociti. A seconda del numero di enzimi isolati, possono migliorare o indebolire la migrazione delle cellule leucocitarie. La reazione infiammatoria si sviluppa e persiste a lungo a causa del fatto che gli enzimi lisosomiali attivano il sistema del complemento, rilasciano citochine e lymokine, attivano la coagulazione e la fibrinolisi.
Proteine cationicheI mediatori dell'infiammazione includono proteine contenute in granuli di neutrofili e aventi alti microbicidi. Queste sostanze agiscono direttamente sulla cellula estranea, rompendone la membrana strutturale. Ciò causa la morte dell'agente patologico. Successivamente, il processo di distruzione e scissione da proteinasi lisosomiale. Le proteine cationiche promuovono il rilascio dell'istamina del neurotrasmettitore, aumentano la permeabilità vascolare, accelerano l'adesione e la migrazione delle cellule dei leucociti. citochineQuesti sono mediatori cellulari dell'infiammazione prodotta dalle seguenti cellule:
Agendo sui neutrofili, le citochine aumentano la permeabilità della parete vascolare. Stimolano inoltre le cellule dei leucociti per uccidere, assorbire e distruggere i microrganismi colonizzati dagli alieni e migliorare il processo della fagocitosi. Dopo aver ucciso agenti patologici, le citochine stimolano la rigenerazione e la proliferazione di nuove cellule. Le sostanze interagiscono con i rappresentanti del loro gruppo di mediatori, prostaglandine, neuropeptidi. Metaboliti attivi di ossigenoUn gruppo di radicali liberi che, grazie alla presenza di elettroni spaiati, sono in grado di interagire con altre molecole, prendendo parte direttamente allo sviluppo del processo infiammatorio. I metaboliti dell'ossigeno che fanno parte dei mediatori includono:
La fonte di questi principi attivi è lo strato esterno dell'acido arachidonico, l'esplosione della fagocitosi durante la loro stimolazione, così come l'ossidazione di piccole molecole.
I metaboliti dell'ossigeno aumentano la capacità delle cellule di fagocitosi di distruggere agenti estranei, causare l'ossidazione dei grassi, danni agli amminoacidi, acidi nucleici, carboidrati, che aumenta la permeabilità vascolare. Come modulatori, i metaboliti sono in grado di aumentare l'infiammazione o avere un effetto anti-infiammatorio. Di grande importanza nello sviluppo di malattie croniche. neuropeptidiQuesto gruppo include calcitonina, neurokinina A e sostanza R. Questi sono i modulatori più noti dei neuropeptidi. L'effetto della sostanza si basa sui seguenti processi:
Oltre a tutto quanto sopra, acetilcolina, adrenalina e norepinefrina sono anche mediatori attivi. L'acetilcolina è coinvolta nella formazione dell'iperemia arteriosa, dilata i vasi sanguigni nella patologia. La norepinefrina e l'adrenalina agiscono come modulatori dell'infiammazione, inibendo la crescita della permeabilità vascolare. Lo sviluppo della risposta infiammatoria non è una violazione del corpo. Al contrario, questo è un indicatore che il sistema immunitario affronta i suoi compiti. Fisiopatologia dell'infiammazione (Conferenza n. IX) Parte 1. 1. Il concetto di infiammazione. 2. Danno primario e secondario. 3. Disturbi metabolici nell'infiammazione. 4. Mediatori dell'infiammazione. 5. fasi della reazione vascolare nell'infiammazione 6. Exudate, i suoi tipi e funzioni. infiammazione (infiammazione) è una complessa risposta protettiva-adattativa locale del tessuto connettivo, dei vasi e del sistema nervoso dell'intero organismo, sviluppata nel processo di evoluzione da creature altamente organizzate in risposta al danno, è finalizzata ad isolare e rimuovere l'agente dannoso ed eliminare le conseguenze del danno. Questo è un tipico processo patologico con cambiamenti nel metabolismo e nella circolazione del sangue, la fagocitosi e la proliferazione. La base di qualsiasi infiammazione è: 1) danno e 2) reazioni protettive. La capacità di resistere al danno, la capacità di guarire le ferite, di ripristinare almeno alcuni dei tessuti persi è la proprietà più importante degli organismi viventi. E queste proprietà sono determinate dal fatto che un corpo sano risponde immediatamente al danno da una serie di reazioni generali e locali. Reazioni generali causato da cambiamenti più o meno pronunciati nello stato funzionale del sistema nervoso, endocrino e immunitario del corpo. Sono accompagnati da cambiamenti nella reattività dell'intero organismo. Le reazioni locali che si verificano nella zona del danno e nelle sue immediate vicinanze, caratterizzano un processo chiamato infiammazione. Significato biologico l'infiammazione è di limitare, ritardare, fermare lo sviluppo del danno e inoltre, se riesce, eliminare la zona di danno dai prodotti di decadimento e dai tessuti distrutti, preparando così il terreno per i processi di restauro effettivi. Nel XVIII secolo, Celso descrisse 4 principali segni clinici di infiammazione: rossore (rubor), gonfiore (tumore), dolore (dolor) e febbre (calorico). Galeno ha aggiunto il quinto segno - disfunzione (functio laesa). Rubor, tumore, dolor, calor et functio laesa sintomata inflammationis sunt. Cause di infiammazione : a) fattori fisici, b) fattori chimici, c) fattori biologici, d) disturbi circolatori, e) crescita tumorale, e) risposte immunitarie. differire 4 fasi: 1. alterazione (alterazione), 2. essudazione (exsudatio) 3. emigrazione (emigrazione) 4. proliferazione (proliferazione). alterativa- questo è il collegamento principale, in effetti - il meccanismo di innesco. L'alterazione può essere primaria o secondaria. primario l'alterazione si sviluppa immediatamente dopo l'impatto del fattore dannoso e si forma a livello dell'elemento funzionale dell'organo. L'alterazione primaria può manifestarsi come cambiamenti specifici, così come cambiamenti non specifici che si sviluppano stereotipicamente indipendentemente dalle proprietà e dalle caratteristiche del fattore patogeno. Queste modifiche sono correlate: 1) con danni alle strutture a membrana, 2) con danno alla membrana mitocondriale, 3) con danno ai lisosomi. Interruzione della struttura della membrana cellulare porta alla rottura delle pompe cellulari. Quindi, la capacità della cellula di reagire adeguatamente modificando il proprio metabolismo ai cambiamenti nell'omeostasi ambientale viene persa, i sistemi enzimatici e il cambiamento dei mitocondri. Nella cellula si accumulano metaboliti ossidati: acidi piruvico, lattico e succinico. Inizialmente, questi cambiamenti sono reversibili e possono scomparire se il fattore eziologico è cessato. La cellula recupera completamente la sua funzione. Se il danno continua e i lisosomi sono coinvolti nel processo, i cambiamenti sono irreversibili. Pertanto, i lisosomi sono chiamati "siti di lancio infiammatori" e da loro inizia la formazione di alterazioni secondarie. Alterazione secondaria a causa dell'effetto dannoso degli enzimi lisosomiali. La glicolisi, la lipolisi e la proteolisi sono migliorate. Come risultato della rottura delle proteine nei tessuti, aumenta il numero di polipeptidi e amminoacidi; Gli acidi grassi aumentano con la ripartizione dei grassi; interruzione del metabolismo dei carboidrati porta all'accumulo di acido lattico. Tutto ciò causa disordini fisici e chimici nei tessuti e l'iperosmia si sviluppa con un aumento della concentrazione di ioni K +, Na +, Ca 2+, Cl; iperkonia: aumento del numero di molecole proteiche dovute alla scissione di grandi dimensioni in quelle più piccole; Iperionium H + - a causa della dissociazione di una grande quantità di acidi con il rilascio di ioni idrogeno. E come risultato di tutto ciò, l'acidosi metabolica si sviluppa a causa di un aumento dei prodotti metabolici acidi. Tutti i componenti del tessuto sono coinvolti nel processo e l'alterazione è irreversibile, il cui risultato è l'autolisi delle cellule. La formazione di sostanze che non solo possono rafforzare, ma anche indebolire l'alterazione, influenzando i vari componenti dell'infiammazione, vale a dire regolazione della microcircolazione, essudazione, emigrazione dei leucociti e proliferazione delle cellule del tessuto connettivo. Queste sostanze biologicamente attive sono chiamate mediatori o modulatori infiammatori. I mediatori dell'infiammazione differiscono ● in tempo la loro attività: presto e tardi; ● per punto di applicazione: colpisce vasi o cellule e ● per origine: humoral (plasma) e cellulare. Fonti di mediatori dell'infiammazione possono essere proteine del sangue e fluido extracellulare, tutte le cellule del sangue, cellule del tessuto connettivo, cellule nervose, elementi non cellulari del tessuto connettivo. Ci sono preformato e appena formato mediatori. I mediatori preformati vengono continuamente sintetizzati senza alcun danno, si accumulano in appositi magazzini e vengono rilasciati immediatamente dopo il danno (ad esempio l'istamina). La sintesi di altri mediatori inizia dopo il danno, come misura di risposta. Tali mediatori sono chiamati di recente formazione (ad esempio prostaglandine). Il danno al tessuto è accompagnato dall'attivazione di speciali sistemi di sangue proteolitico, che portano alla comparsa nel centro di infiammazione di vari peptidi che fungono da mediatori dell'infiammazione. Le chinasi vasoattive si formano anche quando il sistema fibrinolitico viene attivato dal fattore Hageman attivato, che trasforma il plasminogeno inattivo che circola nel sangue in un enzima attivo plasmina. La plasmina fende la fibrina (e la digestione tempestiva della fibrina è necessaria per la guarigione delle ferite). Allo stesso tempo si formano peptidi in grado di dilatare i vasi sanguigni e mantenere una maggiore permeabilità vascolare. La plasmina attiva il sistema del complemento. Il sistema del complemento, che comprende circa 20 diverse proteine, viene attivato in aggiunta al fattore Hageman in due altri modi: il classico è il complesso antigene-anticorpo e l'alternativa è i lipopolisaccaridi delle cellule microbiche. I componenti C 3a e C 5a del complemento sono coinvolti nell'infiammazione, che opsonizza e lecca batteri, virus e cellule patologicamente modificate; contribuire alla degranulazione di mastociti e basofili con il rilascio di mediatori. I componenti del complemento causano anche l'adesione, l'aggregazione e la degranulazione delle cellule del sangue, il rilascio di enzimi lisosomiali, la formazione di radicali liberi, IL-1, la chemiotassi, la leucopoiesi e la sintesi di immunoglobuline. I mediatori del plasma e dell'origine cellulare sono correlati e agiscono sul principio della reazione autocatalitica con feedback e amplificazione reciproca. Disturbo della microcircolazione nel fuoco dell'infiammazione è caratterizzato da un cambiamento nel tono dei vasi microcircolatori, corrente potenziata della parte liquida del sangue all'esterno della nave (cioè, essudazione) e uscita elementi uniformi sangue (cioè emigrazione). per risposta vascolare caratteristica 4 palcoscenico : 1) vasospasmo a breve termine, 2) iperemia arteriosa, 3) iperemia venosa, spasmo i vasi si presentano sotto l'azione di un agente dannoso sul tessuto ed è associato al fatto che i vasocostrittori sono eccitati per primi perché sono più sensibili dei vasodilatatori. Lo spasmo dura fino a 40 secondi e viene rapidamente sostituito dall'iperemia arteriosa. Iperemia arteriosa formato nei seguenti tre modi: ● a causa della paralisi dei vasocostrittori; ● a seguito di esposizione a mediatori con attività vasodilatatrice; ● a seguito dell'implementazione del riflesso assonale. Gli sfinteri precapillari si rilassano, il numero di capillari funzionanti aumenta e il flusso sanguigno attraverso i vasi dell'area danneggiata può essere dieci volte maggiore di quello del tessuto intatto. L'espansione dei vasi microcircolatori, un aumento del numero di capillari funzionanti e un aumento dell'afflusso di sangue all'organismo determinano il primo segno macroscopico di infiammazione - rossore. Se l'infiammazione si sviluppa nella pelle, la cui temperatura è inferiore alla temperatura del sangue che scorre, la temperatura dell'area infiammata aumenta - c'è la febbre. Poiché la prima volta dopo l'infortunio, la velocità del flusso sanguigno lineare e volumetrico nell'area dell'infiammazione è sufficientemente ampia, il sangue che scorre dalla fonte di infiammazione contiene più ossigeno e meno emoglobina recuperata e quindi ha un colore rosso brillante. L'iperemia arteriosa durante l'infiammazione non dura a lungo (da 15 minuti a un'ora) e si trasforma sempre in iperemia venosa, in cui l'aumento dell'afflusso di sangue al corpo è combinato con il rallentamento e persino la completa cessazione del flusso sanguigno capillare. Iperemia venosa inizia con la massima espansione degli sfinteri precapillari, che diventano insensibili agli stimoli vasocostrittori e il deflusso venoso è ostacolato. Successivamente, il flusso sanguigno nei capillari e nelle arteriole viene rallentato. La ragione principale dello sviluppo dell'iperemia venosa è l'essudazione: l'uscita della parte liquida del sangue dalla microvascolarizzazione nel tessuto circostante. L'essudazione è accompagnata da un aumento della viscosità del sangue, una resistenza periferica all'aumento del flusso sanguigno, la velocità del flusso sanguigno diminuisce. Inoltre, l'essudato comprime i vasi venosi, il che complica il deflusso venoso e aumenta anche l'iperemia venosa. Lo sviluppo dell'iperemia venosa è favorito dal gonfiore nell'ambiente acido dei corpuscoli sanguigni, dall'ispessimento del sangue, dal disturbo dei desmosomi, dalla posizione marginale dei leucociti, dalla formazione di microtrombi. Il flusso sanguigno rallenta gradualmente e acquisisce nuove caratteristiche qualitative a causa di un aumento della pressione idrostatica nei vasi: il sangue inizia a muoversi a scatti quando il sangue si muove in avanti al momento della sistole del cuore, e al momento della diastole il sangue si ferma. Con un ulteriore aumento della pressione idrostatica, il sangue nella sistole si muove in avanti, e al momento della diastole ritorna - cioè, sorge il movimento simile a un pendolo. Il movimento di spinta e pendolo del sangue determina l'insorgenza di dolore pulsante. A poco a poco essudazione provoca lo sviluppo di stasi - un fenomeno comune nell'infiammazione. Di regola stasi si verifica in singoli vasi della parte venosa del letto microcircolatorio a causa di un forte aumento della sua permeabilità. Allo stesso tempo, la parte liquida del sangue passa rapidamente nello spazio extravascolare e il vaso rimane pieno di una massa di cellule del sangue strettamente correlate l'una all'altra. L'alta viscosità di tale massa rende impossibile spostarlo attraverso i vasi e si verifica la stasi. I globuli rossi formano "colonne di monete", i confini tra di loro vengono gradualmente cancellati e una massa solida si forma nel lume della nave - fango (dall'inglese Sludge - Tina, dirt). Meccanismi di essudazione: l'essudazione dovuta all'infiammazione è dovuta principalmente all'aumentata permeabilità della microvascolarizzazione delle proteine a seguito di un cambiamento significativo nell'endotelio vascolare. I cambiamenti nelle proprietà delle cellule endoteliali dei vasi microcircolatori sono la principale, ma non la sola causa di essudazione durante l'infiammazione. La formazione di vari essudati contribuisce alla crescita della pressione idrostatica all'interno dei vasi microcircolatori, associata all'espansione delle arteriole portatrici, un aumento della pressione osmotica del fluido interstiziale, dovuto all'accumulo di prodotti di degradazione tissutale osmoticamente attivi nello spazio extravascolare. Più significativamente, il processo di essudazione è espresso nelle venule e nei capillari. L'essudazione forma il quarto segno di infiammazione - gonfiore (tumore). Composizione essudato (exsudatum) è la parte liquida del sangue, gli elementi formati del sangue e i tessuti distrutti. La composizione dell'essudato emette 5 tipi di infiammazione: ● sieroso; ● catarrale (mucosa); ● fibrinoso; ● emorragico; ● purulento; ● ichorous. Funzioni di essudato - come risultato di essudazione, la concentrazione di batteri e altre tossine viene diluita e distrutta da enzimi proteolitici provenienti dal plasma sanguigno. Durante l'essudazione, gli anticorpi sierici entrano nel fuoco dell'infiammazione, che neutralizzano le tossine batteriche e opsonizzano i batteri. L'iperemia infiammatoria fornisce una transizione al fuoco dell'infiammazione dei leucociti del sangue, promuove la fagocitosi. L'essudato di fibrinogeno si trasforma in fibrina, i cui fili creano una struttura che facilita la transizione dei leucociti nella ferita. La fibrina svolge un ruolo importante nel processo di guarigione delle ferite. Tuttavia, anche l'essudazione ha conseguenze negative: il gonfiore dei tessuti può portare a soffocamento o un aumento della pressione intracranica che minaccia la vita. Disturbi della microcircolazione possono causare danni al tessuto ischemico. L'eccessiva deposizione di fibrina può impedire la successiva riparazione del tessuto danneggiato e contribuire all'eccessiva proliferazione del tessuto connettivo. Pertanto, il medico dovrebbe esercitare un controllo efficace sullo sviluppo di essudazione. Fisiopatologia dell'infiammazione (Lezione n. X) parte 2. 1. Emigrazione dei leucociti al centro dell'infiammazione. 2. Funzioni dei leucociti nel fuoco dell'infiammazione. 3. Infiammazione acuta e cronica. 4. L'essenza biologica dell'infiammazione. 5. Diagnosi di infiammazione. Quando l'iperemia arteriosa passa nei leucociti venosi, si spostano gradualmente dallo strato assiale allo strato periferico-parietale e iniziano ad aderire alla superficie dell'endotelio. Il leucocita deve superare due barriere: l'endotelio e la membrana basale. Lo strato di endotelio dei leucociti passa, schiacciamento tra le cellule endoteliali e la membrana basale viene temporaneamente dissolta dalle sue proteasi. L'intero processo di transizione del leucocita attraverso la parete del vaso dura da 2 a 12 minuti e non provoca danni alla parete del vaso. Il posto principale dell'emigrazione dei leucociti è il venule postcapillare. Nell'infiammazione acuta, i neutrofili emigrano prima di tutto e, molto più tardi, i monociti. Eosinofili, basofili e linfociti sono anche in grado di emigrare. L'emigrazione dei leucociti è associata all'emergere di emittenti speciali di mediatori nel focolaio infiammatorio. I hemattaractants più forti sono lipopolisaccaridi, che fanno parte delle endotossine batteriche. L'emattr attivo endogeno più potente include frammenti del complemento attivato durante l'infiammazione, in particolare C5a, leucotriene B4, fattore attivante piastrinico e calicreina. L'emigrazione dei leucociti nel centro di infiammazione inizia con la loro adesione all'endotelio vascolare della microvascolarizzazione. L'adesività aumenta a causa della maggiore formazione di cellule endoteliali di speciali molecole di RNA e della loro corrispondente proteina. Il passaggio dei leucociti attraverso la parete vascolare è il risultato della capacità di muoversi inerente a queste cellule - cioè. locomozioneche è anche attivato da emattragenti. All'interno del citoplasma dei leucociti aumenta la concentrazione di ioni di calcio. Questo attiva il sistema dei microtubuli, che forma lo scheletro interno della cellula, attiva i complessi di actomicosina, la secrezione dei neutrofili del loro contenuto granulare, incluse le proteasi neutrofili in grado di dissolvere la membrana basale dei vasi sanguigni, viene potenziata. L'interazione di emattrattivi con i recettori di superficie dei leucociti è accompagnata dall'attivazione di vari enzimi in essi, inclusa fosfolipasi calcio-dipendente A2, chinasi di proteine calcio-dipendenti: proteina chinasi A e proteina chinasi C. Sotto l'influenza di emattrenti nel leucocita al polo anteriore, il gel corticale si trasforma in un sol, cioè. diventa più liquido Il sol della sua parte centrale viene versato in questa parte diluita dei leucociti. Il leucocita è accorciato nella parte posteriore e allungato nella parte anteriore. La parte liquefatta del gel corticale del polo anteriore viene rigettata con forza e quindi il leucocita avanza. I leucociti neutrofili hanno la massima attività funzionale. I leucociti polimorfonucleati sono i primi a venire al centro dell'infiammazione perché sono più sensibili, sono molto più nel sangue. Si chiamano cellule. " risposta di emergenza"e usa e getta. I monociti sono nel sangue fino a 3 giorni, vanno al tessuto e sono in loro per circa 10 giorni. Alcuni di essi sono differenziati in macrofagi dei tessuti sedentari, alcuni sono inattivi e possono essere riattivati. Pertanto, i monociti sono chiamati celle riutilizzabili. Tale sequenza di rilascio di cellule ematiche al di fuori della nave è stata identificata da Mechnikov e viene chiamata "legge dell'emigrazione" o "stadio della reazione cellulare durante l'infiammazione": 1) polinucleare (neutrofili ed eosinofili) fino a 2 giorni, 2) mononuclea (monociti e linfociti) fino a 5-6 giorni, 3) fibroblastico, caratterizzato dall'accumulo di istiociti e fibroblasti al centro dell'infiammazione. La funzione più importante dei leucociti al centro dell'infiammazione è la fagocitosi, vale a dire catturare, uccidere e digerire i batteri, così come la digestione dei prodotti di decomposizione di tessuti e cellule del corpo. Durante la fagocitosi, ci sono 4 palcoscenico : 1) lo stadio dell'approssimazione dei fagociti all'oggetto; 2) lo stadio di aderenza del fagocita all'oggetto; 3) lo stadio dell'assorbimento dei fagociti dell'oggetto; 4) lo stadio delle trasformazioni intracellulari dell'oggetto assorbito. Il primo stadio è spiegato dall'abilità dei fagociti alla chemiotassi. Opsonine, anticorpi e frammenti del complemento, proteine del plasma e lisozima, giocano un ruolo importante nei meccanismi di adesione e successivo assorbimento da parte del fagocita di un oggetto. È stato stabilito che alcune parti delle molecole di opsonina si legano alla superficie della cellula attaccata e ad altre parti della stessa molecola - con la membrana del fagocita. Il meccanismo di assorbimento non differisce dall'appiccare - la cattura viene effettuata avvolgendo gradualmente la cellula microbica con un fagocita, vale a dire essenzialmente attaccando progressivamente la superficie del fagocita alla superficie del microbo fino a quando l'intero oggetto non è incollato alla membrana del fagocita. Di conseguenza, l'oggetto assorbito si trova all'interno del fagocita, racchiuso in un sacchetto formato da una parte della membrana della cellula fagocitica. Questa borsa è chiamata fagosoma. La formazione del fagosoma inizia lo stadio delle trasformazioni intracellulari dell'oggetto assorbito all'interno del fagosoma, vale a dire al di fuori dell'ambiente interno del fagocita. La parte principale delle trasformazioni intracellulari di un oggetto assorbito durante la fagocitosi è associata alla degranulazione - cioè il trasferimento del contenuto dei granuli citoplasmatici dei fagociti nel fagosoma. In questi granuli, tutti i fagociti obbligati contengono un gran numero di sostanze biologicamente attive, principalmente enzimi, che uccidono e quindi digeriscono i microbi e altri oggetti assorbiti. Nei neutrofili ci sono 2-3 tipi di granuli che contengono lisozima - dissolvendo la parete microbica, lattoferrina - una proteina che lega il ferro e quindi ha un effetto batteriostatico, mieloperossidasi, proteasi neutre, idrolasi acide, una proteina che lega vitamina B 12 e altre. Non appena si forma un fagosoma, i granuli si avvicinano strettamente. Le membrane dei granuli si fondono con la membrana del fagosoma e il contenuto dei granuli entra all'interno del fagosoma. Come già accennato, i neutrofili sono i primi leucociti che si infiltrano nell'area dell'infiammazione. Offrono una protezione efficace contro le infezioni batteriche e fungine. Se la ferita non è infetta, il contenuto di neutrofili diminuisce rapidamente e dopo 2 giorni i macrofagi predominano nel fuoco dell'infiammazione. Come i neutrofili, i macrofagi infiammatori sono cellule mobili che proteggono il corpo dalla fagocitosi da vari agenti infettivi. Sono anche in grado di secernere enzimi lisosomiali e radicali dell'ossigeno, ma differiscono dai neutrofili per una serie di qualità che rendono queste cellule particolarmente importanti negli stadi successivi dell'infiammazione acuta e nei meccanismi di guarigione delle ferite: 1. I macrofagi vivono molto più a lungo (mesi e neutrofili - una settimana). 2. I macrofagi sono in grado di riconoscere e quindi assorbire e distruggere le cellule danneggiate e non vitali del proprio organismo, compresi i neutrofili. Relativo a questo è il loro ruolo straordinario nella "pulizia" dell'essudato infiammatorio. I macrofagi sono le principali cellule coinvolte nella dissoluzione e nella rimozione del tessuto connettivo danneggiato dal centro dell'infiammazione, che è necessario per la successiva ricostruzione tissutale. Sintetizzano e secernono proteasi neutre: elastasi, collagenasi, attivatore del plasminogeno, distruggendo le fibre extracellulari di collagene ed elastina del tessuto connettivo. I macrofagi svolgono un ruolo chiave nella guarigione delle ferite. Negli animali nell'esperimento, privo di cellule mononucleate, le ferite non guariscono. Ciò è spiegato dal fatto che i macrofagi sintetizzano fattori di crescita per fibroblasti e altre cellule mesenchimali, producono fattori che aumentano la sintesi del collagene da parte dei fibroblasti, sono fonti di fattori che controllano vari stadi dell'angiogenesi - rivascolarizzazione del tessuto danneggiato, producono ormoni polipeptidici che mediano la risposta in fase acuta - interleuchina -1 e IL-6 e fattore di necrosi tumorale. L'infiammazione è divisa in acuta e cronica. acutoinfiammazione (infiammatio acuta) si sviluppa a causa di danni improvvisi - ustioni, congelamento, lesioni meccaniche, alcune infezioni. La sua durata di solito non supera diversi giorni. L'infiammazione acuta è caratterizzata da pronunciate reazioni essudative, durante le quali l'acqua, le proteine, le cellule del sangue (principalmente i leucociti) lasciano il flusso sanguigno ed entrano nella zona danneggiata. Infiammazione cronica (infiammatio chronica) si sviluppa quando l'agente dannoso agisce per lungo tempo. L'infiammazione cronica dura settimane, mesi e anni. È caratterizzato non tanto dall'essudazione come dalla proliferazione dei fibroblasti e dell'endotelio vascolare, così come dall'accumulo di cellule speciali nel fuoco dell'infiammazione - macrofagi, linfociti, plasmacellule e fibroblasti. La maggior parte delle più gravi malattie umane sono caratterizzate da un processo infiammatorio cronico - lebbra, artrite reumatoide, tubercolosi, pielonefrite cronica, sifilide, cirrosi epatica e così via. L'infiammazione cronica è solitamente accompagnata da danni irreversibili al parenchima normale, i cui difetti sono riempiti con tessuto connettivo fibroso che deforma gli organi colpiti. Nel caso ottimale, la cessazione dell'azione dell'agente dannoso è accompagnata dall'attenuazione della risposta infiammatoria e dalla completa eliminazione di tutte le conseguenze delle reazioni infiammatorie stesse - es. "risoluzione completa dell'infiammazione". Ciò significa la cessazione della formazione dei mediatori e la loro scomparsa dalla zona di danno, la cessazione dell'emigrazione dei leucociti, il ripristino della permeabilità vascolare, la rimozione di liquidi, proteine, prodotti di degradazione di batteri e cellule (compresi neutrofili e macrofagi). La scomparsa dei mediatori è dovuta in parte alla loro diffusione spontanea dalla fonte di infiammazione e parzialmente inattivazione da parte di vari enzimi, con il sistema di inattivazione che si sviluppa durante il corso dell'infiammazione stessa. Se l'aumento della permeabilità vascolare non era associato a un grave danno alle cellule endoteliali, allora la permeabilità è rapidamente normalizzata dopo la scomparsa dei mediatori. La maggior parte dell'infiammazione accumulata nel nidus viene rimossa con il flusso linfatico. I depositi di fibrina vengono sciolti da enzimi fibrinolitici del sangue, enzimi delle cellule infiammatorie e vengono anche rimossi dai vasi linfatici. È possibile che anche i macrofagi lascino i vasi linfatici. Una parte dei macrofagi caricati con sostanze intatte non tossiche può rimanere a lungo al posto della precedente infiammazione. La piena risoluzione dell'infiammazione crea le condizioni per il completo ripristino della struttura e della funzione dei tessuti danneggiati. Tuttavia, questo accade solo con ferite relativamente piccole di organi e tessuti che hanno anche un'alta capacità di rigenerazione - la pelle, le mucose e il parenchima degli organi interni. La risoluzione incompleta dell'infiammazione porta al fatto che il recupero avviene attraverso cicatrici. Reazione generale del corpo l'infiammazione dipende dalla posizione, causa, grado di danno all'organo, insorgenza di insufficienza dell'organo, reattività e resistenza del corpo, immunità, stato delle ghiandole endocrine, nutrizione, costituzione, sesso, età, precedenti malattie. L'essenza biologica dell'infiammazione. II Mechnikov, 25 anni (dal 1882), ha studiato la fagocitosi. Il suo metodo di patologia comparativa è lo studio del processo in un aspetto evolutivo. Ha dimostrato che l'infiammazione si verifica in tutti i membri del mondo animale. In protezione unicellulare e nutrizione sono la stessa cosa. Nel multicellulare inferiore (spugna), tutte le cellule possono fagocitare. Durante la formazione di strati germinali, la fagocitosi è attaccata al mesoderma. Quando si forma un sistema vascolare di tipo aperto (gambero), i fagociti vengono più facilmente inviati al fuoco infiammatorio e, in quelli più alti, la reazione dei vasi, del sistema nervoso e del tessuto connettivo si unisce alla reazione fagocitaria. Questa è una reazione di tutto l'organismo, sviluppata nel processo di evoluzione, ha un valore protettivo e adattativo - la fagocitosi è la base della protezione, tutto il resto è solo un accessorio della reazione infiammatoria. Diagnosi di infiammazione - sulle aree visibili del tessuto, si manifesta con i suddetti sintomi: arrossamento, febbre, gonfiore, dolore e funzione alterata. Metodi di valutazione valutazione funzionale dei fagociti: a) determinazione dell'attività funzionale dei leucociti: L'1% della fagocitosi è un indicatore esteso del% di cellule fagocitiche per 100 fagociti potenziali, 2. Il numero fagocitico è il numero di oggetti di fagocitosi catturati da questi 100 fagociti, 3. indice fagocitico - o l'intensità di assorbimento - è il numero di oggetti catturati di fagocitosi, che rappresenta per ciascun leucocita fagocitico, 4. l'intensità di assorbimento totale è il numero di oggetti di fagocitosi catturati dai fagociti contenuti in 1 mm 3, 5. completezza della fagocitosi, 6. Indice del conglomerato: il tasso di scomparsa del colorante grezzo dal sangue quando somministrato per via endovenosa dopo ripetuti studi sul sangue venoso in 15-20 minuti, 7. per valutare il grado di vaccinazione determinare il titolo anticorpale, 8. Viene studiata la composizione cellulare dell'essudato. 9. Determinazione del numero totale di leucociti e formula dei leucociti. La dipendenza della reazione infiammatoria sulla condizione generale - reattività e resistenza, che forniscono l'aspetto, lo sviluppo, il decorso e l'esito dell'infiammazione. L'infiammazione può essere: ● normergico - con buona reattività in individui sani, ● Iperergico (molto rapido) - in caso di allergie o in individui collerici, infiammazione- è un processo patologico protettivo filogenetico che si manifesta in risposta al danno tissutale, che include alterazioni caratteristiche, microcircolatorie e proliferative, finalizzate in ultima analisi a isolare ed eliminare l'agente dannoso, i tessuti morti e più o meno completo recupero di organi. Celso ha descritto 4 premi di infiammazione: rossore (rubor), febbre (calorico), gonfiore (tu-mor), dolore (dolor). Galeno aggiunse loro il quinto segno - la violazione della funzione (functio laesa). In aggiunta a quanto sopra, il seguente può sintomi comuni infiammazioni: leucocitosi, febbre, alterazioni delle proteine, composizione ormonale ed enzimatica del sangue, aumento della VES, ecc. La dinamica del processo infiammatorio, indipendentemente dalle ragioni che lo causano, è sempre abbastanza standard. Ci sono 3 componenti di infiammazione: alterazione, disturbo del microcircolo ed emoreologia con essudazione e emigrazione dei leucociti, proliferazione. alterativa(danno) è una violazione dell'organizzazione strutturale e funzionale delle cellule e della sostanza intercellulare di tessuti e organi, che è accompagnata da una violazione della loro attività vitale. È consuetudine distinguere le alterazioni primarie e secondarie. L'alterazione primaria si verifica in risposta all'effetto diretto del fattore che causa l'infiammazione. Le reazioni dell'alterazione primaria come se prolungassero l'azione del fattore dannoso. Il fattore stesso potrebbe non essere più in contatto con il corpo. L'alterazione secondaria avviene sotto l'influenza sia del fattore che causa l'infiammazione che dei fattori di alterazione primaria. L'effetto del fattore dannoso si manifesta principalmente sulle membrane cellulari, comprese quelle lisosomali. Gli enzimi del lisosoma sono reattivi. Vanno fuori e danneggiano tutti gli elementi della cellula. Quindi, l'alterazione secondaria è principalmente autolesionismo. Allo stesso tempo, l'alterazione secondaria è una componente piuttosto ragionevole e necessaria dell'infiammazione - come processo protettivo e adattativo. Il danno contrattuale aggiuntivo è finalizzato alla localizzazione precoce del fattore eziologico e al tessuto del corpo danneggiato dalla sua influenza. Al prezzo del danno si ottengono molti altri importanti fenomeni protettivi: attivazione del metabolismo, coinvolgimento di mediatori infiammatori e cellulari, aumento della fagocitosi, ecc. Cambiamento metabolico All'inizio dell'infiammazione si verifica prevalentemente a causa di carboidrati. Inizialmente, a causa dell'attivazione degli enzimi tissutali, sono aumentate sia la fosforilazione ossidativa dei carboidrati che la glicolisi. Successivamente, la glicolisi inizia a predominare sulla respirazione. Questo perché: 1. Aumento del consumo di ossigeno da parte del tessuto infiammato. 2. La circolazione del sangue è disturbata. Il sangue diminuisce il contenuto di ossigeno. 3. L'accumulo nella lesione dei leucociti, gli enzimi lisosomiali, che abbattono il glucosio principalmente in modo anaerobico, aumenta. 4. Si verificano danni e riduzione del numero di mitocondri. Il metabolismo dei carboidrati sotto-ossidato si accumula nei tessuti: acido lattico e tricarbossilico. violazione metabolismo dei grassi si trova nel fatto che sotto l'azione di enzimi principalmente lisosomiale nel focolaio infiammazione acuta I grassi si rompono per formare acidi grassi. Nello scoppio di un'infiammazione bruscamente disturbato scambio di proteine e acidi nucleici. Sotto l'azione di lisosomiale e di altri enzimi, si verifica la rottura di proteine e acidi nucleici in aminoacidi, polipeptidi, nucleotidi, nucleosidi (adenosina). A causa di disordini metabolici di carboidrati, grassi e proteine, i prodotti metabolici acidi si accumulano nel tessuto infiammato e si sviluppano metabolicamente acidosi. All'inizio, è compensato da riserve alcaline di sangue e fluido tissutale. In futuro, con l'esaurimento locale delle riserve alcaline e con la difficoltà di afflusso di sangue fresco, l'acidosi non viene compensata. Con purulento acuto il pH di infiammazione può raggiungere 5,4, e in cronico - 6,6. Le Aci-dosi creano condizioni favorevoli all'azione di alcuni enzimi lisosomiali, in particolare le glicosidasi, che scompongono i componenti carboidrati del tessuto connettivo. Più la concentrazione di ioni di idrogeno aumenta, più intensa è l'infiammazione. Nella direzione dal centro alla periferia, la concentrazione di ioni idrogeno diminuisce gradualmente. In un ambiente acido, la dissociazione dei sali aumenta. Di conseguenza, il contenuto di ioni K, Na, Ca aumenta nel fuoco dell'infiammazione. Ciò è anche dovuto alla distruzione delle cellule e al rilascio di questi sali. A causa della ridotta formazione di macroerg, l'equilibrio potassio-sodio nella cellula è disturbato. Il potassio inizia a lasciare le cellule, il sodio, al contrario, entra nella cellula. Appaiono iperionio e di-zionia. Allo stesso tempo, la concentrazione molecolare aumenta, come nel processo di disgregazione dei tessuti e di metabolismo compromesso, le grandi molecole si scompongono in molte piccole. A causa di un aumento della concentrazione ionica e molecolare, si sviluppa iperosmia. L'iperkonia porta all'iperosmia - un aumento della concentrazione di proteine nel fuoco dell'infiammazione. L'iperconia si verifica perché: 1) la proteina viene rilasciata dal sangue al fuoco infiammatorio, a causa del fatto che l'acidosi e gli enzimi lisosomiali aumentano la permeabilità della parete vascolare alla proteina; 2) nelle condizioni di acidosi, la fissione di proteine grossolane a fini. Mediatori infiammatori mediatori/ intermediari / infiammazione - è un complesso di sostanze fisiologicamente attive che mediano l'azione di fattori che causano l'infiammazione e determinano lo sviluppo e gli esiti dell'infiammazione. Durante l'infiammazione, vengono escreti in grandi quantità e diventano mediatori. perché sono in grado di rafforzare o indebolire la manifestazione del processo infiammatorio, sono chiamati modulatori. Il legame del mediatore è importante nella patogenesi dell'infiammazione. I principali gruppi di mediatori dell'infiammazione sono: 1. Ammine biogeniche - istamina, serotonina. L'istamina, uno dei mediatori più importanti, è secreta dai basofili e dai mastociti e realizza la sua azione attraverso i recettori di membrana. Il rilascio di istamina è una delle prime azioni di riparazione dei tessuti da danneggiare. L'istamina causa vasodilatazione, aumenta la permeabilità vascolare a causa dell'arrotondamento delle cellule endoteliali e l'indebolimento dei contatti intercellulari, aumenta la produzione di pro-taglandina E 2, riduce il rilascio di enzimi lisosomiali, neutrofili. Fai apparire una persona prurito della pelle, bruciore e dolore. Dopo il rilascio, l'istamina viene rapidamente distrutta dall'enzima istaminasi. Pertanto, la sua azione si arresta rapidamente e altri mediatori, in particolare la serotonina, vengono attivati. È contenuto nel neuro-cervello, nei basofili, nelle piastrine. Nel campo dell'infiammazione, la serotonina in dosi moderate causa la dilatazione delle arteriole, la riduzione dei miociti nelle pareti delle venule e la congestione venosa. Inoltre, aumenta la permeabilità della parete vascolare, aumenta i coaguli di sangue, provoca una sensazione di dolore. Le amine biogeniche interagiscono tra loro e altri mediatori dell'infiammazione. Per esempio 2 ° gruppo di mediatori: sistemi plasma / chinina, complemento, componenti del sistema componente, fattori di coagulazione del sangue /. Le chinine più importanti sono bradykinin e kallidin. Il punto di partenza dell'attivazione del sistema kinin è l'attivazione di 12 fattori di coagulazione - fattore Hageman in caso di danno tissutale. Questo fattore trasforma prekallikreiny in kallikreiny. Quest'ultimo atto sulla proteina plasmatica chininogeno e plasmochinine si formano da esso. Causano la dilatazione delle arteriole e aumentano la permeabilità delle venule, riducono la muscolatura liscia delle vene e aumentano la pressione sanguigna. Le kinine inibiscono l'emigrazione dei neutrofili, stimolano la migrazione dei linfociti, la secrezione delle linfochine e causano una sensazione di dolore. Il complemento è un complesso sistema plasmatico comprendente almeno 18 proteine. Fornisce lisi di cellule alterate native e native. Frammenti di complemento possono aumentare la permeabilità vascolare, rilasciare idrolasi lisosomiali, partecipare alla formazione dei leucotrieni. Il sistema di emostasi e fibrinolisi promuove la trombosi e la formazione di fibrinopeptidi. Aumentano la permeabilità dei vasi sanguigni, stimolano la formazione di chinine. Il terzo gruppo di mediatori sono prodotti dell'acido arachidonico - prostaglandine e leucotrieni. I PG sono prodotti da quasi tutti i tipi di cellule nucleari, ma prevalentemente da leucociti. Le PG aumentano o indeboliscono l'azione di altri mediatori, inibiscono o aumentano l'aggregazione piastrinica, diluiscono o diluiscono i vasi sanguigni e aumentano la temperatura corporea. I leucotrieni si formano nelle membrane delle piastrine, dei basofili, delle cellule endoteliali. Causano aggregazione dei leucociti, spasmo microvascolare, aumento della permeabilità, broncospasmo. Il 4o gruppo di mediatori - radicali di ossigeno e idroperossidi lipidici. Nei mitocondri delle cellule si formano radicali dell'ossigeno come perossido di idrogeno, radicale idrossile, ecc .. Quando i mitocondri vengono danneggiati, i radicali acidi vengono rilasciati interagendo con i lipidi della membrana formando idroperossidi lipidici. L'intero complesso di processi per la generazione di radicali dell'ossigeno e idroperossidi lipidici è chiamato "sistema ossidativo". Al centro dell'infiammazione, i processi dei radicali liberi vengono attivati e danneggiano le membrane delle cellule microbiche e proprie. Si origina una cosiddetta "esplosione ossidativa". È la base dell'attività battericida dei fagociti. Inoltre, i radicali aumentano la permeabilità dei microvasi, possono stimolare la proliferazione. Il quinto gruppo di mediatori è un mediatore di leucociti polimorfonucleati / PMN / monociti e linfociti. I PMN emettono un gruppo di mediatori altamente attivi che causano varie reazioni nel fuoco infiammatorio, formando le sue manifestazioni. Uno dei rappresentanti è il fattore di attivazione piastrinica / PAF /. Aumenta la permeabilità delle navi, causa l'aggregazione piastrinica, l'emigrazione dei leucociti. Inoltre, i leucociti secernono mediatori come la prostaglan E 2, i leucotrieni, il trombossano A 2 (aumenta la coagulazione del sangue, restringe i vasi coronarici), la prostaciclina (espande i vasi sanguigni e riduce la coagulazione del sangue). Le prostate e i leucotrieni sono importanti nell'origine del dolore infiammatorio. I monociti e i linfociti secernono monokines e linfochine. Ad esempio, i linfociti secernono un fattore che inibisce i macrofagi, fattore di stimolazione dei macrofagi. Le linfochine coordinano l'interazione di neutrofagi, microfaghe e linfociti, regolando la risposta infiammatoria in generale. Antimediatori di infiammazione In tutte le fasi dell'infiammazione, le sostanze che impediscono l'accumulo eccessivo di mediatori o arrestano l'influenza dei mediatori vengono rilasciate e agiscono. Questi sono principalmente enzimi: istaminasi, inibitori della chinina della carbossipeptidasi, inibitori esterasi della frazione del complemento. Gli eosinofili svolgono un ruolo importante nella formazione e nella somministrazione di farmaci anti-infiammatori al fuoco infiammatorio. Di anti-mediatori umorali, un ruolo importante è svolto da alfa-1-antitripsina, che si forma negli epatociti. È un inibitore della proteasi. Come segue dalla definizione Il 2 ° componente dell'infiammazione è una violazione del microcircolo e dell'ematologia nel fuoco dell'infiammazione. Si distinguono le seguenti fasi dei disturbi circolatori: 1. Formazione di iperemia arteriosa. 2. Stadio di iperemia venosa, che passa attraverso il misto. 3. Successivamente può venire la stasi del sangue. Istamina, chinine, prostaglandine e altri mediatori dell'infiammazione formano rapidamente arterie, arteriole e assicurano la formazione di iperemia arteriosa. Un ruolo importante nello sviluppo dell'iperemia arteriosa e il suo mantenimento appartengono al cambiamento della sensibilità degli alfa-adrenorecettori dei vasi in condizioni di dose acuta. Di conseguenza, c'è una diminuzione della reazione dei vasi ad adrenalina e influenze simpatiche, che contribuisce all'espansione dell'arteriola e degli sfinteri precapillari. Al centro dell'infiammazione dovuta all'acidosi, alla disionia (aumento della concentrazione di ioni K + nel fluido tissutale), diminuisce anche l'effetto vasocostrittore degli sfinteri precapillari. Tutti questi fattori portano alla formazione di iperemia arteriosa. L'iperemia arteriosa è caratterizzata da un aumento del volume e della velocità lineare del flusso sanguigno, il numero di capillari funzionanti. Un aumento del flusso di sangue ricco di ossigeno contribuisce al miglioramento dei processi redox e della generazione di calore. Pertanto, nella fase di iperemia arteriosa, un aumento della temperatura nell'infiammazione oculare è soggettivamente e oggettivamente registrato. Quando l'infiammazione aumenta la permeabilità dei vasi sanguigni, che contribuisce al rilascio di proteine e acqua nel fuoco dell'infiammazione. Prima di tutto, ci sono albumina, in relazione alla quale aumenta la quantità di globuline e di fibriogen nel sangue. Ciò comporta un aumento della viscosità e della concentrazione del sangue, il risultato è un rallentamento del flusso sanguigno e la formazione di aggregati di globuli rossi. Come risultato dell'accumulo di fluido, e in seguito degli elementi formati nel tessuto, i vasi sanguigni e linfatici vengono compressi, il che rende difficile il flusso di sangue e linfa. L'aggregazione di elementi uniformi, la loro formazione di impasti e fanghi si sviluppa nei vasi. Per i dolci, l'aggregazione degli eritrociti sotto forma di colonne di monete è caratteristica. Con un dolce, la membrana dell'eritrocito non si rompe, quindi il fango si può rompere. Parallelamente, il sistema di coagulazione del sangue viene attivato con la formazione di coaguli di sangue e tromboembolismo. Tutti questi cambiamenti contribuiscono all'aumento della viscosità dinamica del sangue e al deterioramento delle sue proprietà reologiche. Inoltre, la causa della formazione di microtrociti e dell'emorragia è un danno diretto alla parete vascolare, un fattore che causa infiammazione, attivazione del fattore Hageman, azione dei mediatori / enzimi lisosomiali, bradichinina, kallidina /. I globuli rossi lasciano i vasi attraverso gli spazi interendoteliali. Così, l'iperemia arteriosa si unisce molto rapidamente al venoso, le cui manifestazioni aumentano progressivamente. Nella fase di iperemia venosa, il flusso di sangue proveniente dalla fonte dell'infiammazione viene disturbato, la velocità lineare e volumetrica del flusso sanguigno diminuisce, la pressione idrostatica aumenta e si sviluppa il flusso sanguigno a forma di giunco e pendolo. Con lo sviluppo dell'infiammazione e dell'iperemia venosa si verifica un ulteriore rallentamento progressivo del flusso sanguigno. È causato da: a) un eccessivo aumento dell'area della sezione trasversale del dorso vascolare a causa della massima dilatazione dei capillari e dell'apertura delle vene, b) un ostacolo meccanico all'uscita di sangue e linfa dal centro dell'infiammazione, principalmente a causa della compressione dei vasi venosi e linfatici, ) un aumento della resistenza al flusso sanguigno a causa della rugosità della parete interna dei piccoli vasi dai leucociti adesi ad esso, così come il rigonfiamento delle cellule endoteliali; d) ulteriore ispessimento del sangue e aumento della sua viscosità a causa di aumento sul rilascio di fluido dai vasi nel tessuto. Alla fine, c'è una fermata del movimento del sangue - stasi. La stasi viene inizialmente registrata in capillari e venule separati, in seguito copre sempre più vasi. Dopo tutto, la stasi si sviluppa in aterioli. A seconda della gravità dell'infiammazione, la stasi può essere di breve durata, persistere per ore o essere irreversibile. La conseguenza della stasi può essere un cambiamento irreversibile delle cellule del sangue e dei tessuti. essudazione essudazione - questa è l'uscita della parte liquida del sangue nel fuoco dell'infiammazione. Viene effettuato in 3 modi: 1. Attraverso le fenditure interendoteliali, la cui dimensione aumenta a causa della riduzione delle cellule endoteliali dei microfibrelli. 2. Attraverso il corpo delle cellule endoteliali attraverso canali specializzati. 3. Percorso di micropinocitosi nella forma di condurre attivamente le più piccole gocce attraverso il corpo cellulare. Sono state identificate due fasi per aumentare la permeabilità della parete vascolare nel fuoco infiammatorio: 1. Aumentare istantaneamente la permeabilità vascolare a causa dell'azione delle sostanze vasoattive. 2. Ritardo (ritardato, lungo) associato all'azione dei leucociti PMN. I granuli di leucociti contengono sostanze biologicamente attive che vengono rilasciate durante la degranulazione e la fagocitosi. Il processo di accumulo di leucociti PMN e la loro degranulazione è un processo lungo. Ecco perché forniscono la seconda fase del miglioramento della permeabilità. L'aumento della permeabilità vascolare è dovuto ai seguenti fattori: 1. L'azione diretta del fattore (veleni animali, tossine batteriche, ecc.). 2. L'azione di un BAS (istamina, serotonina, kinins, ecc.) 3. Acidosi. Porta alla liquefazione dei colloidi e all'indebolimento delle connessioni interendoteliali. L'aumentata permeabilità delle navi porta al rilascio di proteine ed elementi ematici nell'area infiammata. Il rilascio di acqua e sostanze disciolte in esso è dovuto a: 1. Un aumento dell'area di filtrazione e diffusione. 2. Aumento della pressione sanguigna nei capillari e nelle venule. 3. Aumento della pressione osmotica nel tessuto infiammato. 4. edema linfatico Viene chiamato il fluido che entra nel tessuto infiammato ekssu- luigi Datome. Contiene una grande quantità di proteine (30-50 g / l), corpuscoli di sangue, cellule di tessuto danneggiato. Essudato non infiammatorio - trasudato, contiene molto meno proteine, corpuscoli di sangue, cellule di tessuto danneggiato. In parallelo con il rilascio di proteine e acqua durante l'infiammazione, il processo di emigrazione dei leucociti procede. Emigrazione dei leucociti L'uscita dei leucociti è preceduta dal movimento del muro e dalla loro posizione, che è osservata particolarmente chiaramente nella fase di iperemia venosa. Questo fenomeno è spiegato da una diminuzione della carica negativa dei leucociti, microcoagulazione vicino alla parete, a seguito della quale le microfibre inibiscono il movimento dei leucociti e contribuiscono alla loro posizione vicino alla parete. Di più I.I.Mechnikov ha notato che i leucociti PMN appaiono prima nell'infiammazione, quindi nei monociti e negli ultimi linfociti. I leucociti emigrano in due modi: i leucociti PMN escono attraverso gli spazi interendoteliali e le cellule mononucleate attraverso il corpo delle cellule endoteliali. Quest'ultimo processo richiede più tempo e questo spiega perché le cellule mononucleate appaiono più tardi nell'area infiammata. La membrana basale degli elementi del sangue viene superata sulla base di una diminuzione reversibile isotermica della viscosità di una soluzione colloidale (tixotropia), vale a dire transizione del gel al sol quando i leucociti sono attaccati alla membrana. Il leucocita, superando facilmente il sol, risulta essere fuori dalla nave, e la membrana si trasforma nuovamente in un gel. In questo processo, sono coinvolti gli enzimi e, soprattutto, il collage Naza. Una certa influenza sulla sequenza di emigrazione ha il pH della fonte di infiammazione. A pH 7,4-7,2, i leucociti PMN si accumulano, a pH 7,0-6,8, le cellule mononucleate ea pH 6,7, tutti i leucociti muoiono nel nido dell'infiammazione per formare pus. Importante nell'emigrazione dei leucociti appartiene chemotak-sisu. È formato con la partecipazione del complemento. L'uso di inibitori del complemento previene danni alle navi e il rilascio di leucociti. La chemiotassi è stimolata dalla streptochinasi. Le chemotossine compaiono quando danno meccanico tessuto, con infiammazione infettiva dovuta all'azione delle endotossine. Le chemotossine sono anche formate dai linfociti durante la degradazione delle gammaglobuline. La chemiotassi è stimolata dai prodotti metabolici di tessuti, batteri, virus e il sistema della callicreina. Un certo ruolo nell'emigrazione dei leucociti è svolto dai cosiddetti tensioattivi, che possono abbassare la tensione superficiale. Ad esempio: acidi organici. Alterando la tensione superficiale di un leucocita, questi ultimi causano lo sviluppo di protrusioni citoplasmatiche e formano pseudopodi. A poco a poco, l'intero leucocita si muove in esso, andando completamente al di là della nave. Il destino dei leucociti rilasciati dalle navi dipende dall'ambiente in cui cadono. Se l'infiammazione è di natura asettica, allora i leucociti emigrati muoiono rapidamente durante 3-5 giorni. Se l'infiammazione ha un carattere settico, il numero di leucociti nel fuoco infiammatorio aumenta progressivamente. Inizia la suppurazione. Alcuni leucociti situati al centro del fuoco infiammatorio muoiono. La parte mostra l'attività fagocitaria. L'attività enzimatica è in aumento: mieloperossidasi, idrolasi acide che distruggono i batteri extracellulari. Nonostante il fatto che la placca batterica sia la causa primaria dello sviluppo di malattie parodontali infiammatorie, solo il suo effetto non può spiegare la gravità della distruzione parodontale. La reazione del corpo svolge un ruolo cruciale nello sviluppo malattia parodontale. Il corpo umano ha una serie complessa di meccanismi di protezione interdipendenti volti ad eliminare i microrganismi, raggiungere la guarigione e mantenere uno stato sano. Paradossalmente, lo stesso sistema, progettato per proteggere e curare il corpo, porta a danni ai tessuti nelle malattie parodontali. L'immunologia è un argomento estremamente complesso. Inoltre, è piuttosto difficile separare tali nozioni come risposta infiammatoria e immunitaria, poiché in molte situazioni la loro azione si sovrappone a vicenda. Questo capitolo fornisce una panoramica delle manifestazioni della risposta infiammatoria e immunitaria, nonché il loro ruolo nella guarigione e nella distruzione della malattia parodontale. Verranno trattati i seguenti argomenti:
infiammazione L'infiammazione è una chiara sequenza di eventi che si sviluppano in risposta a qualsiasi danno o infezione, quindi, ha un carattere "non specifico". L'infiammazione è la risposta primaria che si verifica prima dell'attivazione del sistema immunitario. Il processo di infiammazione è caratterizzato da tre fasi:
Prima di iniziare a discutere del processo stesso, presentiamo i principali elementi cellulari e molecolari dell'infiammazione. Elementi cellulari di infiammazione Le principali cellule responsabili dell'infiammazione sono leucociti (PMN), che si formano nel midollo osseo dalle stesse cellule staminali dei monociti. I marcatori specifici della superficie cellulare determinano quale percorso porterà allo sviluppo dei promielociti - lungo il percorso di formazione dei macrofagi o del PMN. Questi indicatori scompaiono dopo il completamento della differenziazione. La presenza di diversi PMN nell'epitelio attaccato è considerata normale. L'aumento del loro numero è un segno dell'inizio della reazione dell'organismo. I PMN sono fagociti e costituiscono il 70% del numero totale di leucociti. Il citoplasma del PMN contiene elementi responsabili del movimento delle cellule durante l'attivazione della chemiotassi, così come i lisosomi che distruggono i batteri. La distruzione dei batteri da parte di queste cellule solitamente, ma non sempre, avviene dopo che i microrganismi sono stati assorbiti dal PMN (cioè dopo la fagocitosi). Le cellule successive coinvolte nella risposta infiammatoria sono macrofagi, che sono formati da monociti circolanti, e compaiono nell'area di infiammazione dopo PMN. I macrofagi sono grandi cellule con le stesse abilità fagocitiche del PMN. Inoltre, i macrofagi svolgono un ruolo importante nella risposta immunitaria. I linfociti penetrano la regione dell'infiammazione per ultimi e sono associati principalmente a infiammazione cronica. Inoltre, i linfociti sono le principali cellule del sistema immunitario. I mastociti sono gli stessi dei basofili circolanti. Rilasciano istamina, fattore piastrinico attivante (PAF), prostaglandina E2 e leucotrieni (LTB4 e LTD4), ciascuno di questi elementi ha un pronunciato effetto infiammatorio. Le piastrine rilasciano serotonina (un importante mediatore dell'infiammazione). Componenti molecolari dell'infiammazione L'istamina aumenta la permeabilità delle pareti dei vasi sanguigni, facilitando così l'accesso delle cellule infiammatorie alla zona interessata. L'istamina è rilasciata da mastociti e basofili. La serotonina (5-idrossi-triptamina) aumenta anche la permeabilità vascolare. Basofili, neutrofili e macrofagi rilasciano il fattore attivante piastrinico (PAF). Il PAF aumenta il rilascio di serotonina dalle piastrine. Il fattore chemiotassi dei neutrofili (NCF) viene rilasciato dai mastociti e regola la chemiotassi del PMN. Le chemochine vengono rilasciate dai leucociti. Costituiscono un ampio gruppo di citochine che provocano la degranulazione dei mastociti e la chemiotassi del PMN. Avvertenza: la terminologia potrebbe sembrare piuttosto confusa. Tutte le molecole che influenzano la risposta immunitaria o infiammatoria sono chiamate citochine. In linea con questo, tutte le chemochine sono citochine, ma ci sono un gran numero di citochine che non sono chemochine. Il complemento attivato SZ causa la degranulazione dei mastociti. Il complemento attivato C5a porta alla degranulazione dei mastociti, alla chemiotassi dei fagociti, all'attivazione di PMN e ad un aumento della permeabilità capillare. La bradichinina (un elemento del sistema kinin) provoca vasodilatazione e aumenta la permeabilità vascolare. I fibrinopeptidi sono prodotti dal meccanismo di coagulazione e influenzano la chemiotassi del PMN e dei macrofagi. La prostaglandina E2 (PGE2) è un prodotto della cicloossigenasi e provoca vasodilatazione, contemporaneamente ad un aumento della permeabilità vascolare sotto l'azione dell'istamina e della bradichinina. Il leucotriene B4 (LTB4) si forma durante il ciclo della lipossigenasi. Stimola la chemiotassi del PMN e sinergicamente con PGE2 porta ad un aumento della permeabilità della parete vascolare. Il leucotriene D4 (LTD4), che si forma anche durante il ciclo della lipossigenasi, aumenta la permeabilità vascolare. Il fattore chemiotassi dei neutrofili (NCF) è rilasciato dai basofili. Le selectine sono un gruppo di tre molecole che facilitano la migrazione di PMN e macrofagi attraverso la parete vascolare. Selectins E e selectins P sono specifici per PMN e selectin L è per macrofagi. Le selezioni rallentano il movimento delle cellule, il che contribuisce all'adesione di queste ultime alla parete del vaso. I tre gruppi, incluso il gruppo noto come ICAMS, includono almeno 12 molecole che svolgono funzioni simili. Infiammazione acuta nelle malattie parodontali Come accennato in precedenza, il processo di infiammazione acuta comprende tre fasi. Mentre la placca batterica si accumula nella scanalatura, si verificano i seguenti eventi. L'apporto di sangue aumenta a causa dell'espansione dei vasi sanguigni nell'area colpita. Alcuni mediatori causano vasodilatazione, ad esempio istamina e PGE2. Serotonina, C5a, bradichinina, fibrinopeptidi, PGE2, LTB2 e LTD2 aumentano la permeabilità della parete vascolare e aumentano lo spazio tra le cellule endoteliali. Selectins e ICAMS rallentano il movimento del PMN, permettendo a quest'ultimo di penetrare tessuto connettivo. La migrazione e la funzione fagocitaria del PMN sono regolate da fattori chemiotattici, come NCF. Chemiochine, C5a, fibrinopeptidi e LTB4 contribuiscono anche alla fagocitosi e alla chemiotassi dei neutrofili. Le principali cellule fagocitiche coinvolte nella risposta del corpo all'invasione infettiva sono neutrofili e macrofagi polimorfonucleati. La distruzione di microrganismi, di solito, ma non sempre, si verifica dopo il loro assorbimento da parte delle cellule. Il danneggiamento di alcune membrane cellulari può portare alla formazione e al rilascio di fattori che portano alla comparsa dei sintomi clinici dell'infiammazione.
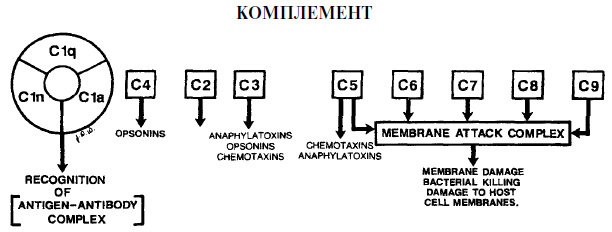
Undici proteine classiche
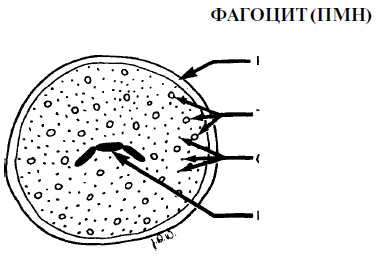
I granuli sono anche chiamati lisosomi o "pacchetti suicidi". enzimi che distruggono le cellule batteriche e le cellule del corpo fagociti Fagocitosi indipendente dall'ossigeno Questo processo si verifica a seguito dell'azione di un gran numero di sostanze distruttive contenute negli organelli che si trovano nel citoplasma dei fagociti. Tali organelli sono chiamati granuli o lisosomi. L'attività distruttiva degli enzimi porta al rilascio di contenuto di granuli e di altri fattori che appartengono ai gruppi di proteine cationiche, alle proteasi neutre, alle idrolasi acide e ad altre sostanze, come la lattoferrina. Gli enzimi distruggono i batteri dopo essere stati assorbiti dai fagociti. Tuttavia, nel processo della fagocitosi, alcuni enzimi possono "fuoriuscire" dal fagocita e interagire con le strutture che circondano la cellula. Probabilmente, questo fenomeno è di grande importanza in un solco o in un fluido tascabile, dove la distruzione dei batteri inizia senza un precedente assorbimento, che contribuisce alla protezione dei tessuti parodontali. Inoltre, gli enzimi lisosomali possono svolgere un ruolo importante nel neutralizzare l'azione degli enzimi distruttivi e delle tossine sintetizzate e rilasciate dai batteri, indipendentemente dal fatto che questi enzimi e le tossine siano stati precedentemente assorbiti dai fagociti. Fagocitosi dipendente dall'ossigeno Questo processo porta alla distruzione dei batteri situati all'interno degli organelli cellulari, chiamati fagolisosomi. Durante questo processo, ossidanti tossici e perossido di idrogeno vengono rilasciati dai radicali dell'ossigeno e dall'enzima lisosomiale mieloperossidasi, che porta alla morte massiccia di cellule batteriche a seguito di danni alla parete cellulare. Nel corso di numerosi studi, è stata studiata la relazione tra i neutrofili polimorfonucleati (PMN) e lo stato dei tessuti parodontali. Le malattie parodontali sono più comuni e più gravi in presenza di neutrofili nell'uomo o negli animali, come l'agranulocitosi o l'insufficienza di adesione dei leucociti. Negli animali con una diminuzione del numero o dell'insufficienza congenita del PMN, si è verificata una rapida distruzione parodontale e perdita di denti. Studi clinici condotti su un gran numero di pazienti hanno dimostrato che la presenza di insufficienza funzionale del PMN nei pazienti è un fattore di rischio elevato di distruzione del tessuto parodontale. Nel 1996, al Congresso Internazionale di Parodontologia, Offenbacker suggerì che i pazienti con PMN normale sviluppavano probabilmente gengiviti, ma non parodontite, indipendentemente dal grado di carica batterica. D'altra parte, la presenza di insufficienza funzionale del PMN nella maggior parte dei casi è accompagnata da una perdita di attaccamento. I risultati di questi studi suggeriscono che i PMN svolgono un ruolo cruciale nel garantire una condizione parodontale sana, ma possono portare alla distruzione dei tessuti parodontali. Distruzione dei tessuti corporei È noto che il corpo stesso determina una significativa distruzione dei suoi stessi tessuti durante lo sviluppo delle malattie parodontali. Tale danno può essere considerato come una reazione patologica in presenza di cronica malattia infiammatoria. Le seguenti sostanze hanno la capacità di distruggere i tessuti parodontali nel processo di reazione difensiva del corpo contro i batteri e i loro prodotti metabolici.
Sistema di complemento del siero Il sistema di complemento del siero consiste di oltre 20 proteine del siero di latte che, se attivate, possiedono attività biologica. Questo sistema svolge un ruolo estremamente importante nella risposta infiammatoria e immunitaria. Esistono due meccanismi principali di attivazione delle proteine del sistema del complemento. Il primo meccanismo classico viene attivato dopo che l'anticorpo si lega alla superficie della parete del batterio. Il secondo meccanismo alternativo può essere attivato direttamente dai componenti della parete di alcuni batteri gram-negativi. Tali componenti sono chiamati endotossine. Di seguito sono riportati solo alcuni dei numerosi fattori di attivazione del complemento sierico coinvolti in entrambi i meccanismi.
È probabile che i fattori biologicamente attivi formati nel sistema del complemento sierico svolgano un ruolo importante nella protezione del corpo dall'invasione microbica nei tessuti parodontali, poiché portano alla distruzione dei batteri e all'introduzione di altri meccanismi di difesa che riducono la concentrazione microbica. Come nel caso di tutti i meccanismi protettivi quando il complemento è attivato, esiste la possibilità di danneggiare i tessuti parodontali. Alla fine di questo capitolo ci sarà una discussione sulle peculiarità del danno ai tessuti parodontali da parte degli anticorpi e dei fagociti indotti dal complemento. Tuttavia, inoltre, a causa dell'attivazione del sistema del complemento, le membrane delle cellule del corpo, in particolare i globuli rossi, possono essere distrutte. L'attivazione del complemento può portare alla distruzione dei tessuti parodontali, che determina i sintomi clinici della malattia. IMMUNOLOGIA Tradizionalmente, consideriamo due parti del sistema immunitario: l'immunità cellulare e l'immunità umorale. Nonostante l'opportunità di tale separazione, gli immunologi stanno attualmente cercando di caratterizzarlo sistema immunitario da elementi che riconoscono gli antigeni cellulari e da elementi che riconoscono antigeni liberi. Elementi cellulari del sistema immunitario
Citochine e altri elementi molecolari Le citochine sono molecole non anticorpali che hanno la capacità di influenzare molti componenti della risposta immunitaria e infiammatoria, come la cascata di complimenti, la bradichinina, il processo di coagulazione e la cascata dell'acido arachidonico. Le citochine più importanti includono:
Immunoglobuline (anticorpi)
Risposta immunitaria nella malattia parodontale Con l'accumulo di placca batterica nell'area del solco, passa un breve periodo di tempo (di solito alcuni giorni) durante il quale non vengono rilevati gli anticorpi. Dopo alcuni giorni, il corpo inizia a reagire alla presenza di batteri e dei loro prodotti metabolici. Fibroblasti, macrofagi e linfociti rilasciano IL-1, IL-2, IL-6 e IL-8. Si verifica l'attivazione di selectine e 1C AM, che avvia diapedesis (percolazione attraverso la parete vascolare), migrazione e chemiotassi dei leucociti polimorfonucleati. Il processo della diapedesi viene accelerato e il PMN è seguito dai macrofagi. Entrambi i tipi di cellule sono attivati dalle citochine. Clinicamente, questo si manifesta con rossore primario con gengivite. Gli antigeni vengono "consegnati" alle cellule B e ai monociti usando le cellule T helper. Alla fine, vengono rilasciate le citochine. Ciò porta alla produzione di cellule B, che formano anticorpi specifici per ciascun antigene. Gli antigeni subiscono opsonizzazione e fagocitosi, con conseguente rilascio di sostanze che danneggiano il collagene e la sostanza principale. SZa e C5a portano al rilascio di istamina da mastociti, questo causa vasodilatazione e facilita la migrazione nell'area interessata di un numero maggiore di cellule protettive. In definitiva, l'epitelio dei solchi ulcerati, che contribuisce ad una penetrazione ancora più rapida degli antigeni batterici. A questo punto, le gengive si gonfiano, sanguinano e possono essere un po 'dolorose. Le citochine prodotte da fibroblasti, PMN e altre cellule, possono svolgere un ruolo sia protettivo che dannoso. L'area interessata è infiltrata con linfociti e plasmacellule. In assenza di trattamento o in caso di insufficienza dei meccanismi di difesa, la perdita dell'attaccamento si verifica a causa dell'azione dei batteri e come conseguenza della risposta del corpo a una sostanza irritante batterica. conclusione In uno stato di salute tra i batteri e i meccanismi di difesa del corpo c'è un equilibrio. Con lo sviluppo della malattia questo equilibrio viene disturbato, i batteri e gli sforzi del corpo per distruggere i batteri e curare, portano alla distruzione dei tessuti parodontali. Tale squilibrio può verificarsi a seguito dell'azione di fattori di virulenza, meccanismi di difesa o fattori esterni, ad esempio, sotto l'influenza del tabagismo. Alfabeto parodontale |
| Leggi: |
|---|
Più popolari:
Betulla appesa o verrucosa
|
nuovo
- Il programma di idratazione intensiva della pelle sulla corteccia dei cosmetici
- Cosa ti serve per la polvere acrilica
- Cosa significa mascotte del gufo
- Analisi per pancreatite: quali ricerche dovrebbero essere fatte e quali indicatori mostrare
- Gufo: un talismano per attirare denaro e buona fortuna
- Quale uccello urla di notte con la voce di un gattino?
- Colesterolo e stress
- Manicure a casa
- Viso efficace
- Cos'è un uomo dopo una gamba rotta?