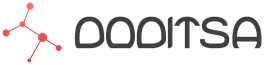Secțiuni de site
Alegerea editorului:
- Pete albe pe unghii, motive pentru ce să facă, pete albe pe unghii și semne populare
- Metode disponibile pentru creșterea rapidă a leucocitelor din sânge
- Unghiile de ciocolata si pielea nu vor rezista zonei de cafea
- Expozitie de mobilier Crocus. Expozitii de mobilier
- Owl tatuaj pe valoarea brațului
- Cei mai mari membri ai lumii
- Fracturile falangelor degetelor de la picioare ale fotografiei
- Ce este colesterolul "rău" și "bun"
- Ce trebuie să faceți dacă pielea din jurul unghiilor se usucă
- Lista celor mai sigure lacuri naturale
publicitate
| Rolul patogenetic al răspunsului inflamator. Mediatorii inflamatorii: clasificare |
|
Apariția proceselor inflamatorii ca răspuns la acțiunea unui factor patologic este un răspuns adecvat al organismului. Inflamația este un proces complex care se dezvoltă la nivel local sau general, care apare ca răspuns la acțiunea agenților străini. Sarcina principală de dezvoltare răspunsul inflamator are ca scop eliminarea efectelor patologice și refacerea corpului. Mediatorii inflamatorii sunt mediatori implicați direct în aceste procese. Pe scurt despre principiile reacțiilor inflamatoriiSistemul imunitar este gardian al sănătății umane. Când este necesar, intră în luptă și distruge bacteriile, virușii, ciupercile. Cu toate acestea, cu intensificarea intensificării muncii, procesul de combatere a microorganismelor poate fi observat vizual sau se poate simți aspectul imaginii clinice. În astfel de cazuri, inflamația se dezvoltă ca răspuns protector al organismului. Există un proces acut de reacție inflamatorie și cursul său cronic. Primul apare ca urmare a acțiunii bruște a unui iritant (traumă, rănire, efecte alergice, infecție). Inflamația cronică are o natură prelungită și semne clinice mai puțin pronunțate. În cazul unui răspuns local al sistemului imunitar în zona de rănire sau rănire, apar următoarele semne ale unei reacții inflamatorii:
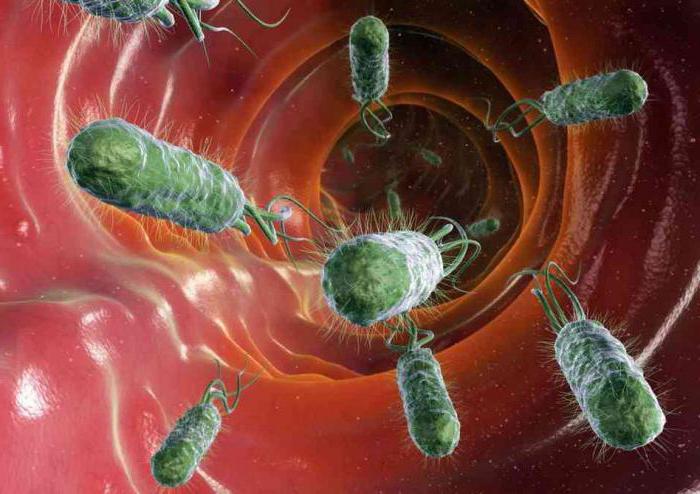
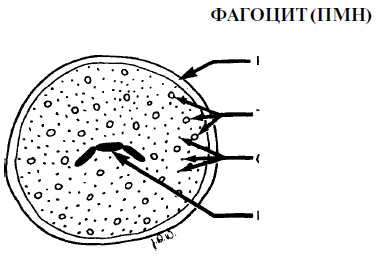
Etapa de dezvoltare a inflamațieiProcesul de inflamație se bazează pe interacțiunea simultană a factorilor de protecție ai pielii, sângelui și celulelor imune. Imediat după contactarea cu un agent străin, organismul răspunde cu o expansiune locală a vaselor de sânge în zona de traume directe. Există o creștere a permeabilității pereților lor și o microcirculare locală crescută. Împreună cu celulele de flux sanguin de protecție umorală vin aici. În a doua etapă, celulele imune încep să lupte împotriva microorganismelor care se află în locul leziunii. Se incepe procesul numit fagocitoza. Celulele neutrofile își schimbă forma și absorb agenții patologici. Apoi, există substanțe speciale destinate distrugerii bacteriilor și a virușilor. În paralel cu microorganismele, neutrofilele distrug vechile celule moarte situate în zona inflamației. Astfel începe dezvoltarea celei de-a treia faze a reacției organismului. Focalizarea inflamației ca și cum ar fi protejată de întregul corp. Uneori în acest loc se simte o pulsație. Mediatoarele inflamatorii mediterare încep să fie produse. mastocitelecare vă permite să curățați zona rănită de toxine, zguri și alte substanțe.
Concepte generale despre mediatoriMediatorii inflamatorii sunt substanțe active de origine biologică, a căror eliberare este însoțită de principalele faze ale modificării. Ele sunt responsabile de apariția reacțiilor inflamatorii. De exemplu, permeabilitatea crescută a pereților vaselor sau o creștere locală a temperaturii în zona traumatismelor. Principalii mediatori inflamatori se remarcă nu numai prin dezvoltarea procesului patologic. Producția lor are loc în mod constant. Acesta vizează reglarea funcțiilor corpului la nivelul țesuturilor și celular. În funcție de direcția de acțiune, modulatorii au efectul:
Odată cu apariția daunelor sau în locul acțiunii microorganismelor, legătura mediatorului controlează procesele de interacțiune a efectorilor inflamatori și schimbarea fazelor caracteristice ale procesului. Tipuri de mediatori inflamatoriToți modulatorii inflamatori sunt împărțiți în două grupe mari, în funcție de originea lor:
Umorali mediatori inflamatorii sunt în organismul uman înainte de expunerea la un factor patologic, adică, organismul are o aprovizionare cu aceste substanțe. Depunerea lor apare în celule într-o formă inactivă. Aminele vasoactive, neuropeptidele și factorii lizozomali sunt, de asemenea, modulatori preexistenți. Substanțele rămase aparținând grupului de mediatori celulari sunt produși direct în timpul dezvoltării răspunsului inflamator.
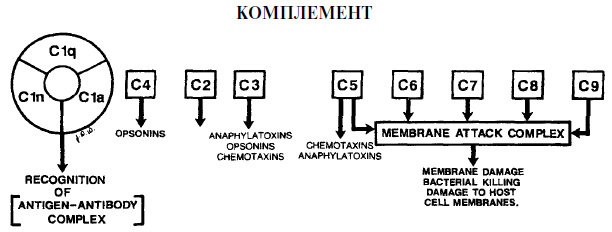
Derivații complecșiMediatorii inflamației sunt derivați ai complimentului. Acest grup de substanțe biologic active este considerat cel mai important dintre modulatorii umorali. Derivații includ 22 de proteine diferite, formarea cărora apare atunci când complementul este activat (formarea unui complex imun sau imunoglobuline).
Acest grup de mediatori este produs din plasmă și din țesutul lichid. Datorită intrării în zona patologică apar procese de exudare. Cu ajutorul derivaților complementului, se eliberează interleukină, neurotransmițători, leucotrieni, prostaglandine și factori de activare a trombocitelor. kinineleAcest grup de substanțe este un vasodilatator. Acestea se formează în țesuturi și plasme din globulele specifice. Principalii reprezentanți ai grupului sunt bradikinina și kallidina, efectul cărora se manifestă după cum urmează:
Acțiunea bradikininei vizează deschiderea accesului plasmei sanguine la locul inflamației. Kininele sunt mediatori ai durerii inflamației. Ei irită receptorii locali, provocând disconfort, dureroasă senzațiePruritul. prostaglandineMediatorii celulari ai inflamației sunt prostaglandinele. Acest grup de substanțe aparține derivatelor de acid arahidonic. Sursele de prostaglandine sunt macrofagele, trombocitele, granulocitele și monocitele.
Prostaglandinele sunt mediatori inflamatori care prezintă următoarea activitate:
leucotrieneLegat de mediatorii nou formați. Adică, în organism, într-o stare de repaus a sistemului imunitar, numărul lor nu este suficient pentru un răspuns imediat la un factor enervant. Leukotrienele provoacă o permeabilitate crescută a peretelui vascular și accesul deschis la celulele albe din sânge în zona patologică. În materie de geneză a durerii inflamatorii. Substanțele pot fi sintetizate în toate celulele sanguine, cu excepția celulelor roșii din sânge, precum și în adventiția celulelor plămânului, vaselor de sânge și a mastocitelor. În cazul dezvoltării proces inflamator ca răspuns la bacterii, viruși sau factori alergici, leucotrienele provoacă bronhospasm, declanșând dezvoltarea edemului. Efectul este similar cu acțiunea histaminei, dar mai mult. Organul țintă pentru substanțele active este inima. Stând în număr mare, ele acționează asupra mușchiului inimii, încetinesc fluxul sanguin coronarian și măresc nivelul răspunsului inflamator. tromboxaniAcest grup de modulatori activi se formează în țesuturile splinei, celulele creierului, plămânii și celulele sanguine din trombocite. Acestea au un efect spastic asupra vaselor, cresc procesele de tromboză în timpul ischemiei cardiace, contribuie la procesele de agregare și aderare a trombocitelor. Amine biogeneMediatori inflamatorii primari - histamina și serotonina. Substanțele sunt provocate de tulburări inițiale de microcirculare în domeniul patologiei. Serotonina este un neurotransmițător care este produs în celulele mastocite, enterochromasfinele și trombocitele. Acțiunea serotoninei variază în funcție de nivelul acesteia în organism. În condiții normale, când cantitatea de mediator este fiziologică, crește spasmul vaselor și crește tonul acestora. Odată cu dezvoltarea reacțiilor inflamatorii, numărul crește dramatic. Serotonina devine vasodilatator, mărind permeabilitatea peretelui vascular și extinderea vaselor de sânge. În plus, acțiunea sa este de o sută de ori mai eficace decât cel de-al doilea neurotransmițător al aminelor biogene.
Histamina este un mediator al inflamației care are un efect diferit asupra vaselor de sânge și a celulelor. Acționând pe un grup de receptori sensibili la histamină, substanța dilată arterele și inhibă mișcarea leucocitelor. Când este expus la altul, îngustă venele, determină o creștere a presiunii intracelare și, dimpotrivă, stimulează mișcarea celulelor albe din sânge. Acționând pe receptorii neutrofile, histamina limitează funcționalitatea lor, la receptorii monocitelor - stimulează aceasta din urmă. Astfel, neurotransmitatorul poate avea simultan un efect inflamator inflamator. Efectul vasodilatator al histaminei este crescut sub influența unui complex cu acetilcolină, bradikinină și serotonină. Lizozomale enzimeMediatorii inflamatori imuni sunt produși de monocite și granulocite la locul procesului patologic în timpul stimulării, emigrației, fagocitozelor, leziunilor celulare și morții. Proteinazele, care sunt principala componentă a enzimelor lizozomale, au o acțiune antimicrobiană, lizând microorganisme patologice străine. În plus, substanțele active ajută la creșterea permeabilității pereților vasculari, modulând infiltrarea leucocitelor. În funcție de numărul de enzime izolate, ele pot spori sau pot slăbi migrarea celulelor leucocitare. Reacția inflamatorie se dezvoltă și persistă mult timp datorită faptului că enzimele lizozomale activează sistemul de complement, eliberează citokine și limokine, activează coagularea și fibrinoliza.
Proteine cationiceMediatorii inflamatori includ proteine conținute în granule neutrofile și având microbicide ridicate. Aceste substanțe acționează direct asupra celulei străine, rupând membrana sa structurală. Aceasta provoacă moartea agentului patologic. În continuare, procesul de distrugere și scindare de către proteinazele lizozomale. Proteinele cationice promovează eliberarea histaminei neurotransmițătoare, sporesc permeabilitatea vasculară, accelerează aderarea și migrarea celulelor leucocitare. citokineAceștia sunt mediatori celulari ai inflamației produse de următoarele celule:
Acționând pe neutrofile, citokinele cresc permeabilitatea peretelui vascular. De asemenea, ele stimulează celulele leucocitare să ucidă, să absoarbă și să distrugă microorganismele colonizate străine și să sporească procesul de fagocitoză. După uciderea agenților patologici, citokinele stimulează regenerarea și proliferarea celulelor noi. Substanțele interacționează cu reprezentanți din grupul lor de mediatori, prostaglandine, neuropeptide. Metaboliții activi ai oxigenuluiUn grup de radicali liberi care, datorită prezenței electronilor neparticipați, sunt capabili să interacționeze cu alte molecule, luând un rol direct în dezvoltarea procesului inflamator. Metaboliții de oxigen care fac parte din mediatori includ:
Sursa acestor substanțe active este stratul exterior al acidului arahidonic, explozia fagocitoză în timpul stimulării lor, precum și oxidarea moleculelor mici.
Metabolitul oxigenului mărește capacitatea celulelor de fagocitoză de a distruge agenții străini, provoacă oxidarea grăsimilor, deteriorarea aminoacizilor, acizilor nucleici, carbohidrații, care mărește permeabilitatea vasculară. Ca modulatori, metaboliții sunt capabili să crească inflamația sau să aibă un efect antiinflamator. De mare importanță în dezvoltarea bolilor cronice. neuropeptideAcest grup include calcitonina, neurokinina A și substanța R. Acestea sunt cei mai cunoscuți modulatori ai neuropeptidelor. Efectul substanței se bazează pe următoarele procese:
În plus față de toate cele de mai sus, acetilcolina, epinefrina și norepinefrina sunt, de asemenea, mediatori activi. Acetilcolina este implicată în formarea hiperemiei arteriale, dilasează vasele de sânge în patologie. Norepinefrina și adrenalina acționează ca modulatori ai inflamației, inhibând creșterea permeabilității vasculare. Dezvoltarea răspunsului inflamator nu reprezintă o încălcare a corpului. Dimpotrivă, acesta este un indicator al faptului că sistemul imunitar se descurcă cu sarcinile sale. Patofiziologia inflamației (Cursul nr. IX) Partea 1. 1. Conceptul de inflamație. 2. Daune primare și secundare. 3. Tulburări metabolice în inflamație. 4. Mediatori de inflamație. 5. Etapele reacției vasculare în inflamație. 6. Exudatul, tipurile și funcțiile acestuia. inflamație (inflammatio) este un răspuns complex de protecție-adaptivă locală a țesutului conjunctiv, a vaselor și a sistemului nervos al întregului organism, dezvoltat în procesul de evoluție de la creaturi foarte organizate ca răspuns la daune, are ca scop izolarea și înlăturarea agentului dăunător și eliminarea consecințelor daunelor. Acesta este un proces patologic tipic cu schimbări în metabolism și circulație sanguină, fagocitoză și proliferare. Baza oricăror inflamații este: 1) leziuni și 2) reacții de protecție. Capacitatea de a rezista daunelor, capacitatea de a vindeca răni, de a restabili cel puțin o parte din țesuturile pierdute este cea mai importantă proprietate a organismelor vii. Iar aceste proprietăți sunt determinate de faptul că un organism sănătos răspunde imediat la daune printr-o serie de reacții generale și locale. Reacții generale cauzate de schimbări mai mult sau mai puțin pronunțate în starea funcțională a sistemului nervos, endocrin și imun al organismului. Acestea sunt însoțite de modificări ale reactivității întregului organism. Reacțiile locale care apar în zona de distrugere și în vecinătatea sa imediată, caracterizează un proces numit inflamare. Sensul biologic inflamația este limitarea, întârzierea, oprirea dezvoltării daunelor și, în cazul în care reușesc, curățarea zonei de deteriorare a produselor de dezintegrare și a țesuturilor distruse, pregătindu-se astfel terenul pentru procesele reale de restaurare. În secolul al XVIII-lea, Celsus a descris patru semne clinice principale ale inflamației: roșeață, umflare (tumoare), durere (dolor) și febră (calor). Galen a adăugat al cincilea semn - disfuncție (functio laesa). Rubrica, tumora, dolor, calor et functio laesa simptomata inflamatia sunt. Cauze ale inflamației : a) factorii fizici, b) factorii chimici, c) factorii biologici, d) tulburările circulatorii, e) creșterea tumorilor, e) răspunsurile imune. diferi 4 etape: 1. modificarea (alteratio), 2. exudație (exsudație) 3. emigrația (emigrația) 4. proliferarea (proliferatio). care schimbă- acesta este principalul link, de fapt, mecanismul de declanșare. Modificarea poate fi primară sau secundară. primar modificarea se produce imediat după impactul factorului dăunător și se formează la nivelul elementului funcțional al organului. Modificarea primară se poate manifesta ca schimbări specifice, precum și schimbări nespecifice care se dezvoltă în mod stereotip, indiferent de proprietățile și caracteristicile factorului patogen. Aceste modificări sunt legate: 1) cu deteriorarea structurilor membranare, 2) cu afectarea membranei mitocondriale, 3) cu afectarea lizozomilor. Perturbarea structurii membranei celulare duce la întreruperea pompelor celulare. Prin urmare, capacitatea celulei de a reacționa în mod adecvat prin schimbarea propriului metabolism la schimbările de homeostază de mediu este pierdută, sistemele enzimatice și schimbările mitocondriilor. În celulă se acumulează metaboliți oxidați: acizi piruvi, lactici și succinici. Inițial, aceste modificări sunt reversibile și pot să dispară dacă factorul etiologic a încetat. Celula își recuperează complet funcția. Dacă daunele persistă și lizozomii sunt implicați în proces, atunci schimbările sunt ireversibile. Prin urmare, lizozomii se numesc "locurile de lansare inflamatorie" și de la acestea începe formarea alterării secundare. Alterări secundare datorită efectului dăunător al enzimelor lizozomale. Glicoliza, lipoliza și proteoliza sunt îmbunătățite. Ca rezultat al descompunerii proteinelor în țesuturi, crește numărul de polipeptide și aminoacizi; Acizii grași cresc odată cu defalcarea grăsimilor; întreruperea metabolismului carbohidraților duce la acumularea de acid lactic. Toate acestea cauzează tulburări fizice și chimice în țesuturi, iar hiperosmia se dezvoltă cu o creștere a concentrației de ioni K +, Na +, Ca 2+, Cl; hiperconia - o creștere a numărului de molecule de proteine datorită defalcării substanțelor mari în cele mai mici; Hyperionium H + - datorită disocierii unei cantități mari de acizi cu eliberarea ionilor de hidrogen. Și, ca urmare a acestui fapt, acidoza metabolică se dezvoltă datorită creșterii produșilor metabolici acide. Toate componentele țesutului sunt implicate în proces, iar modificarea este ireversibilă, rezultatul fiind autoliza celulelor. Formarea de substanțe care pot nu numai să consolideze, dar și să slăbească alterarea, afectând diferitele componente ale inflamației, adică reglarea microcirculației, exudarea, emigrarea leucocitelor și proliferarea celulelor țesutului conjunctiv. Aceste substanțe biologic active sunt numite mediatori sau modulatori inflamatori. Mediatorii inflamatorii diferă ● la timp activitatea lor: devreme și târziu; ● prin punct de aplicare: afectarea vaselor sau a celulelor; ● după origine: umoral (plasmă) și celular. Sursele de mediatori inflamatorii pot fi proteinele sanguine și fluidele extracelulare, toate celulele sanguine, celulele țesutului conjunctiv, celulele nervoase, elementele non-celulare ale țesutului conjunctiv. distinge preformat și nou format mediatori. Mediatorii preformați sunt sintetizați continuu fără nici o deteriorare, se acumulează în magazine speciale și se eliberează imediat după deteriorare (de exemplu, histamină). Sinteza altor mediatori începe după deteriorare, ca măsură de răspuns. Astfel de mediatori sunt numiți nou formați (de exemplu, prostaglandine). Deteriorarea țesutului este însoțită de activarea unor sisteme sanguine proteolitice speciale, care conduc la apariția în centrul de inflamație a diferitelor peptide care acționează ca mediatori inflamatori. Kininele vasoactive se formează și atunci când sistemul fibrinolitic este activat de factorul Hageman activat, care transformă plasminogenul inactiv care circulă în sânge într-o enzimă activă plasmină. Plasmina desprinde fibrina (și digestia în timp util a fibrinei este necesară pentru vindecarea cu succes a rănilor). În același timp, se formează peptide care sunt capabile să dilueze vasele de sânge și să mențină o permeabilitate vasculară crescută. Plasmina activează sistemul complementar. Sistemul complementar, care include aproximativ 20 de proteine diferite, este activat în plus față de factorul Hageman în două moduri: clasicul este complexul antigen-anticorp și alternativa este lipopolizaharidele celulelor microbiene. Componentele C 3a și C 5a ale complementului sunt implicate în inflamație, care opsonizează și lizează bacteriile, virușii și celulele proprii modificate patologic; contribuie la degranularea celulelor mastocite și bazofilelor cu eliberarea mediatorilor. Componentele complementare cauzează de asemenea aderența, agregarea și degranularea celulelor sanguine, eliberarea enzimelor lizozomale, formarea radicalilor liberi, IL-1, stimularea chemotaxiei, leucopoiezei și sinteza imunoglobulinelor. Mediatorii de origine plasmatică și celulară sunt corelați și acționează pe principiul reacției autocatalitice cu feedback și amplificare reciprocă. Tulburare de microcirculație în centrul inflamației se caracterizează o schimbare a tonusului vaselor microcirculatorii, creșterea curentului părții lichide a sângelui în afara vasului (ie exudarea) și ieșirea în formă de elemente sânge (adică emigrare). pentru răspuns vascular caracteristică 4 etapă : 1) vasospasmul pe termen scurt, 2) hiperemia arterială, 3) hiperemie venoasă, spasm vasele apar sub acțiunea unui agent dăunător asupra țesuturilor și sunt asociate cu faptul că vasoconstrictoarele sunt mai întâi excitate deoarece sunt mai sensibile decât vasodilatatoarele. Spasmul durează până la 40 de secunde și este rapid înlocuit cu hiperemie arterială. Hiperemie arterială formate în următoarele trei moduri: ● ca rezultat al paraliziei vasoconstrictorilor; ● ca urmare a expunerii la mediatori cu activitate vasodilatatoare; ● ca urmare a implementării reflexului axonului. Sfincterile precapilare se relaxează, numărul de capilare crescătoare, iar fluxul sanguin prin vasele zonei afectate poate fi de zece ori mai mare decât cel al țesutului intact. Extinderea vaselor microcirculare, creșterea numărului de capilare și creșterea aprovizionării cu sânge a corpului determină primul semn macroscopic al inflamației - roșeață. Dacă se produce o inflamație la nivelul pielii, a cărei temperatură este sub temperatura curgerii sângelui, temperatura zonei inflamate crește - există febră. Deoarece la prima dată după leziune viteza fluxului sanguin liniar și volumetric în zona inflamației este suficient de mare, sângele care curge din sursa de inflamație conține mai mult oxigen și mai puțin hemoglobină recuperată și, prin urmare, are o culoare roșie aprinsă. Hiperemia arterială în timpul inflamației nu durează mult (de la 15 minute până la o oră) și se transformă întotdeauna în hiperemie venoasă, în care creșterea cantității de sânge pentru organism este combinată cu încetinirea și chiar încetarea completă a fluxului sanguin capilar. Hiperemie venoasă incepe cu expansiunea maxima a sfincterilor precapilare, care devin insensibile la stimulii vasoconstrictori, iar fluxul venos este impiedicat. După aceasta, fluxul sanguin în capilare și arteriole este încetinit. Principalul motiv pentru dezvoltarea hiperemiei venoase este exudarea - ieșirea părții lichide din sânge din microvasculatură în țesutul înconjurător. Exudarea este însoțită de o creștere a vâscozității sângelui, rezistența periferică la creșterea fluxului sanguin, viteza fluxului sanguin scade. În plus, exsudatul comprimă vasele venoase, ceea ce complică fluxul venos și, de asemenea, crește hiperemia venoasă. Dezvoltarea hiperemiei venoase este favorizată prin umflarea în mediul acid al celulelor sanguine, îngroșarea sângelui, desmosomii afectați, starea marginală a leucocitelor, formarea microtrombi. Fluxul de sânge încetinește treptat și dobândește noi caracteristici calitative datorită creșterii presiunii hidrostatice în vase: sângele începe să se miște brusc când sângele se deplasează înainte în momentul sistolului inimii și în momentul diastolului sângele se oprește. Cu o creștere suplimentară a presiunii hidrostatice, sângele din sistol se mișcă înainte, iar în momentul diastolului se întoarce - adică mișcarea asemănătoare pendulului. Împingerea și mișcarea pendulului determină apariția durerii pulsante. Exudarea treptată determină dezvoltarea stazei - un fenomen comun în inflamație. Ca regulă stază apare în vase individuale ale părții venoase a patului microcirculator datorită creșterii drastice a permeabilității acestuia. În același timp, partea lichidă a sângelui trece rapid în spațiul extravascular și vasul rămâne umplut cu o masă de celule sanguine care sunt strâns legate între ele. Viscozitatea ridicată a unei astfel de mase face imposibilă mutarea acesteia prin vase și apare staza. Celulele roșii din sânge formează "coloane de monede", granițele dintre ele sunt șterse treptat și se formează o masă solidă în lumenul vasului - nămol (din limba engleza, nămol - Tina, murdărie). Mecanisme de exudare: exudarea datorată inflamației se datorează în primul rând permeabilității crescute a microvasculatului pentru proteine, ca urmare a unei modificări semnificative a endoteliului vascular. Schimbările în proprietățile celulelor endoteliale ale vaselor microcirculare sunt principala, dar nu singura, cauză a exudării în timpul inflamației. Contribuie la formarea diferitelor exudate crește presiunea hidrostatică în interiorul vaselor de sange microcirculatorii asociate cu extinderea arteriolelor aferente, creșterea presiunii osmotice a unui fluid interstițial datorită acumulării în spațiul extravascular produse active osmotic tesut degradare. Mai semnificativ, procesul de exudare este exprimat în venule și capilare. Exudarea formează al patrulea semn de inflamație - umflare (tumoare). Exudați compoziția (exsudatum) este partea lichidă a sângelui, elementele formate ale sângelui și țesuturile distruse. Compoziția exsudatului emit 5 tipuri de inflamație: ● seroase; ● catarrala (mucoasa); ● fibrinos; ● hemoragic; ● purulente; ● vicios. Exudați funcțiile - ca urmare a exudării, concentrația toxinelor bacteriene și a altor toxine este diluată și distrusă de enzimele proteolitice provenite din plasma sanguină. În timpul exudării, anticorpii serici intră în centrul inflamației, care neutralizează toxinele bacteriene și opsonizează bacteriile. Hiperemia inflamatorie oferă o tranziție spre focalizarea inflamației leucocitelor din sânge, favorizează fagocitoza. Exudatul fibrinogen se transformă în fibrină, firele din care creează o structură care facilitează trecerea leucocitelor în rană. Fibrina joacă un rol important în procesul de vindecare a rănilor. Cu toate acestea, exudarea are și consecințe negative - umflarea țesutului poate duce la sufocare sau la o creștere a presiunii intracraniene care amenință viața. Tulburările microcirculației pot duce la afectarea țesutului ischemic. Depozitarea excesivă a fibrinului poate împiedica repararea ulterioară a țesutului deteriorat și poate contribui la proliferarea excesivă a țesutului conjunctiv. Prin urmare, medicul trebuie să exercite un control efectiv asupra dezvoltării exsudatului. Patofiziologia inflamației (Lectura nr. X) Partea 2. 1. Emigrarea leucocitelor în centrul inflamației. 2. Funcțiile leucocitelor în centrul inflamației. 3. Inflamația acută și cronică. 4. Esența biologică a inflamației. 5. Diagnosticul inflamației. La schimbarea congestie venoasă arterială în leucocite deplasate treptat de tip axial periferic strat - parietală și să înceapă să se lipească de suprafața endoteliya.Voznikaet „distanța leucocitare graniță“ și din acel moment începe migrarea în masă a leucocitelor într-un focar inflamatie. Leucocitele trebuie să depășească două bariere: endoteliul și membrana de bază. Stratul de endoteliu al leucocitelor trece, stoarcerea între celulele endoteliale, iar membrana de bază este dizolvată temporar de proteazele sale. Întregul proces de tranziție a leucocitelor prin peretele vasului durează de la 2 la 12 minute și nu cauzează deteriorarea peretelui vasului. Principalul loc de emigrare a leucocitelor sunt venulele postcapilare. În inflamația acută, neutrofilele emigrează mai întâi și, mult mai târziu, monocite. Eozinofilele, bazofilele și limfocitele sunt, de asemenea, capabile de emigrare. Migrarea la leucocite este asociată cu apariția unor hematractori mediatori speciali în focalizarea inflamatorie. Cele mai puternice substanțe hemataractante sunt lipopolizaharidele, care fac parte din endotoxinele bacteriene. Cel mai puternic hematractant endogen include fragmente ale complementului activat în timpul inflamației, în special C5a, leucotrienă B4, factor de activare a trombocitelor și calicreină. Emiterea de leucocite în centrul de inflamație începe cu aderarea lor la endoteliul vascular al microvasculatului. Adezivitatea crește ca urmare a formării crescute a celulelor endoteliale ale moleculelor ARN speciale și a proteinei lor corespunzătoare. Trecerea leucocitelor prin peretele vascular este rezultatul capacității de a se mișca inerent în aceste celule - adică locomoțiecare este de asemenea activat de hematractori. În interiorul citoplasmei leucocitelor, concentrația de ioni de calciu crește. Aceasta activează sistemul microtubulilor, formând un schelet interior al celulelor, activează complexul actomiozin, îmbunătățește secreția neutrofilelor conținutului lor granulari, inclusiv proteaze de neutrofile pot dizolva membrana bazală a vaselor de sange. Interacțiunea hematractorilor cu receptorii de suprafață ai leucocitelor este însoțită de activarea diferitelor enzime în ele, incluzând fosfolipaza A2 dependentă de calciu, proteine kinazele dependente de calciu: proteina kinaza A și proteina kinaza C. Sub influența hematractorilor din leucocite la polul frontal, gelul cortical se transformă într-un sol, adică devine mai lichid. Solul părții sale centrale este turnat în această parte diluată a leucocitelor. Leucocitele se scurtează în spate și se prelungesc în față. Partea lichefiată a gelului cortic al polului anterior este aruncată înapoi cu forță și astfel leucocitele se mișcă înainte. Leucocitele neutrofile au cea mai mare activitate funcțională. Leucocitele polimorfonucleare sunt primele care vin în centrul inflamației deoarece sunt mai sensibile, sunt mult mai mult în sânge. Ele sunt numite celule. " răspunsul de urgență"și de unică folosință. Monocitele sunt în sânge timp de până la 3 zile, merg la țesut și sunt în ele timp de aproximativ 10 zile. Unele dintre ele sunt diferențiate în macrofage de țesut sedentar, unele sunt inactive și pot fi reactivate. Prin urmare, monocitele sunt numite celule refolosibile. O astfel de secvență de eliberare a celulelor sanguine în afara vasului a fost identificată de către Mechnikov și se numește "legea emigrării" sau "stadiul reacției celulare în timpul inflamației": 1) polinuclear (neutrofile și eozinofile) până la 2 zile, 2) mononucleare (monocite și limfocite) până la 5-6 zile, 3) fibroblastică, caracterizată prin acumularea de histiocite și fibroblaste în centrul inflamației. Cea mai importantă funcție a leucocitelor în centrul inflamației este fagocitoza - adică captarea, uciderea și digestia bacteriilor, precum și digestia produselor de dezintegrare ale țesuturilor și celulelor corpului. În timpul fagocitozelor, există 4 etapă : 1) stadiul de aproximare a fagocitului la obiect; 2) stadiul de aderare a fagocitului la obiect; 3) stadiul de absorbție a fagocitelor obiectului; 4) stadiul transformărilor intracelulare ale obiectului absorbit. Prima etapă se explică prin capacitatea fagocitelor de a chemotaxa. Opsoninii, anticorpii și fragmentele complementare, proteinele plasmatice și lizozimul joacă un rol important în mecanismele lipirii și absorbției ulterioare de către fagocit a unui obiect. Sa constatat că anumite părți ale moleculelor de opsonin se leagă de suprafața celulei atacate și alte părți ale aceleiași molecule - cu membrana fagocitară. Mecanismul de absorbție nu diferă de lipirea - captarea este realizată prin învelirea treptată a celulei microbiene cu un fagocit, adică în esență prin lipirea progresivă a suprafeței fagocitului pe suprafața microbului până când întregul obiect este lipit pe membrana fagocitului. Ca o consecință, obiectul absorbit se află în interiorul fagocitului, închis într-un sac format din partea membranei celulei fagocitare. Această pungă se numește fagozom. Formarea fagozomilor începe stadiul transformărilor intracelulare ale obiectului absorbit în interiorul fagozomului, adică în afara mediului intern al fagocitului. Partea principală a transformărilor intracelulare ale unui obiect absorbit în timpul fagocitozelor este asociată cu degranularea - adică transferul conținutului de granule citoplasmice de fagocite în fagozom. În aceste granule, toate fagocitele obligatorii conțin un număr mare de substanțe biologic active, în principal enzime, care ucid și apoi digeră microbii și alte obiecte absorbite. In neutrofilele 2-3 are formă de granule care conțin lizozimul - dizolvarea lactoferinei peretelui microbian - proteina de legare a fierului și exercitând astfel o acțiune bacteriostatică, myeloperoxidase, proteaza neutra, hidrolaze acide, proteina de vitamina B 12 și altele obligatorii. De îndată ce se formează un fagozom, granulele se apropie cu atenție. Membranele granulelor se îmbină cu membrana fagozomică, iar conținutul granulelor intră în interiorul fagozomului. După cum sa menționat deja, neutrofilele sunt primele leucocite care infiltrează zona inflamării. Acestea asigură o protecție eficientă împotriva infecțiilor bacteriene și fungice. Dacă rana nu este infectată, atunci conținutul de neutrofile din ea scade rapid și după 2 zile macrofagele predomină în focalizarea inflamației. Ca și neutrofilele, macrofagele inflamatorii sunt celulele motile care protejează organismul prin fagocitoză de la diferiți agenți infecțioși. Ele pot, de asemenea, să secrete enzime lizozomale și radicali de oxigen, dar diferă de neutrofile printr-o serie de calități care fac aceste celule deosebit de importante în stadiile ulterioare ale inflamației acute și în mecanismele de vindecare a rănilor: 1. Macrofagele trăiesc mult mai mult (luni și neutrofile - o săptămână). 2. Macrofagele sunt capabile să recunoască și să absoarbă și să distrugă celulele deteriorate și neviabile ale propriului organism, inclusiv neutrofilele. În legătură cu acest lucru este rolul lor extraordinar în "curățarea" exudatului inflamator. Macrofagele sunt celulele principale implicate în dizolvarea și înlăturarea țesutului conjunctiv deteriorat din focalizarea inflamației, care este necesară pentru reconstrucția ulterioară a țesutului. Ei sintetizează și secretă proteaze neutre: elastază, colagenază, activator de plasminogen, distrugând colagenul extracelular și fibrele de elastină ale țesutului conjunctiv. Macrofagele joacă un rol-cheie în vindecarea rănilor. La animalele din experiment, lipsite de celule mononucleare, rănile nu se vindecă. Acest lucru se datorează faptului că macrofage sintetiza factori de creștere pentru fibroblaste și alte celule mezenchimale care produc factori care cresc sinteza de colagen de fibroblasti sunt o sursă de factori care controlează diferitele stadii ale angiogenezei - revascularizare tesutului deteriorate, produc hormoni polipeptidici, care sunt mediatori ai „răspuns de fază acută“ - Interleukina -1 și IL-6 și factorul de necroză tumorală. Inflamația este împărțită în acută și cronică. acutinflamație (inflammatio acuta) se dezvoltă din cauza deteriorărilor bruște - arsuri, degerături, leziuni mecanice, unele infecții. Durata sa de obicei nu depășește câteva zile. Inflamația acută se caracterizează prin reacții exudative pronunțate, în timpul cărora apa, proteinele, celulele sanguine (majoritatea leucocitelor) părăsesc sângele și intră în zona afectată. Inflamația cronică (inflammatio chronica) se dezvoltă atunci când agentul dăunător acționează mult timp. Inflamația cronică durează săptămâni, luni și ani. Acesta este caracterizat nu atât de mult exudat, ca proliferarea fibroblastelor și endoteliul vascular și acumularea în inflamarea celulelor speciale - macrofage, limfocite, celule plasmatice, și fibroblaste. Majoritatea bolilor umane cele mai grave sunt caracterizate de un proces inflamator cronic - lepră, artrită reumatoidă, tuberculoză, pielonefrită cronică, sifilis, ciroză hepatică și așa mai departe. Inflamația cronică este de obicei însoțită de leziuni ireversibile ale parenchimului normal, ale căror defecte sunt umplute cu țesut conjunctiv fibros care deformează organele afectate. În cazul optim, încetarea acțiunii agentului dăunător este însoțită de atenuarea răspunsului inflamator și eliminarea completă a tuturor consecințelor reacțiilor inflamatorii în sine - adică "rezoluția completă a inflamației". Aceasta înseamnă stoparea formării mediatorilor și dispariția lor din zona de distrugere, încetarea emigrării leucocitelor, restabilirea permeabilității vasculare, îndepărtarea fluidelor, a proteinelor, a produselor de degradare a bacteriilor și a celulelor (inclusiv neutrofilele și macrofagele). Dispariția mediatorilor se datorează, în parte, difuzării lor spontane de la sursa inflamației și parțial inactivării prin diferite enzime, cu sistemul de inactivare dezvoltat în cursul inflamației. Dacă creșterea permeabilității vasculare nu a fost asociată cu deteriorarea gravă a celulelor endoteliale, atunci permeabilitatea este rapid normalizată după dispariția mediatorilor. Majoritatea inflamațiilor acumulate în nidus sunt îndepărtate cu fluxul limfatic. Depunerile de fibrină sunt dizolvate de enzimele fibrinolitice din sânge, enzimele celulelor inflamatorii și sunt, de asemenea, îndepărtate de către vasele limfatice. Este posibil ca macrofagele să părăsească și vasele limfatice. O parte din macrofagele încărcate cu substanțe intacte netoxice pot rămâne pentru o lungă perioadă de timp în locul inflamației anterioare. Rezoluția completă a inflamației creează condițiile pentru restabilirea completă a structurii și funcției țesuturilor deteriorate. Cu toate acestea, acest lucru se întâmplă numai cu răni relativ mici de organe și țesuturi care au, de asemenea, o capacitate mare de regenerare - pielea, membranele mucoase și parenchimul organelor interne. Rezolvarea incompletă a inflamației conduce la faptul că recuperarea survine prin cicatrizare. Reacție generală a corpului inflamația depinde de locul, cauza, gradul de deteriorare a organului, apariția insuficienței organului, reactivitatea și rezistența organismului, imunitatea, starea glandelor endocrine, nutriția, constituția, sexul, vârsta, bolile anterioare. Esența biologică a inflamației. II Mechnikov, de 25 de ani (din 1882), a investigat fagocitoza. Metoda sa de patologie comparativă este studiul procesului într-un aspect evolutiv. El a demonstrat că inflamația are loc în toți membrii lumii animalelor. În protecția și nutriția unicelulară sunt aceleași. În bobul multicelulare inferior (burete), toate celulele pot fagocit. În timpul formării straturilor germinale, fagocitoza este atașată la mezoderm. Când se formează un sistem vascular de tip deschis (raci), fagocitele sunt mai ușor de eliberat la focalizarea inflamatorie și, în cele mai mari, reacția vaselor, a sistemului nervos și a țesutului conjunctiv se alătură reacției fagocitare. Aceasta este o reacție a întregului organism, dezvoltată în procesul de evoluție, are o valoare protectoare și adaptivă - fagocitoza este baza protecției, restul este doar accesoriile reacției inflamatorii. Diagnosticul inflamației - pe zonele vizibile ale țesutului, se manifestă prin simptomele de mai sus: roșeață, febră, umflare, durere și afectare a funcției. Metode de evaluare evaluarea funcțională a fagocitelor: a) determinarea activității funcționale a leucocitelor: 1.% din fagocitoză este un indicator extins al% celulelor fagocitare la 100 de fagocite potențiale, 2. Numărul fagocitar este numărul de obiecte de fagocitoză capturate de aceste 100 de fagocite, 3. indicele fagocitar - sau intensitatea absorbției - este numărul de obiecte capturate de fagocitoză, care reprezintă fiecare leucocit fagocitar, 4. intensitatea totală de absorbție este numărul de obiecte de fagocitoză capturate de fagocite conținute în 1 mm 3, 5. completitudinea fagocitozei, 6. indicele de conglomerat - rata de dispariție a colorantului brut din sânge atunci când se administrează intravenos după studii repetate ale sângelui venos în 15-20 de minute, 7. pentru a evalua gradul de vaccinare determina titrul de anticorpi, 8. Compoziția celulară a exudatului este investigată. 9. Determinarea numărului total de leucocite și a formulei leucocitelor. Dependența reacției inflamatorii asupra stării generale - reactivității și rezistenței, care asigură aspectul, evoluția, evoluția și rezultatul inflamației. Inflamația poate fi: ● normergic - cu reactivitate bună la persoanele sănătoase, ● Hiperegic (foarte rapid) - în caz de alergii sau la indivizi colerici, inflamație- este un proces patologic protector filogenetic care apare ca răspuns la deteriorarea țesutului, care include modificări caracteristice ale modificării, microcirculației și proliferării, care vizează, în cele din urmă, izolarea și eliminarea agentului dăunător, a țesuturilor moarte și mai mult sau mai puțin complete recuperarea organelor. Celsus a descris 4 premii de inflamație: roșeață, febră (calor), umflare (tu-mor), durere (dolor). Galen le-a adăugat al cincilea semn - încălcarea funcției (functio laesa). În plus față de acestea, pot exista următoarele simptome comune inflamații: leucocitoză, febră, modificări ale proteinei, compoziție hormonală și enzimatică a sângelui, ESR crescut etc. Dinamica procesului inflamator, indiferent de motivele care îl determină, este întotdeauna destul de standard. Există 3 componente ale inflamației: modificări, tulburări de microcirculare și hemorheologie cu exudare și emigrare de leucocite, proliferare. care schimbă(daune) este o încălcare a organizării structurale și funcționale a celulelor și a substanței intercelulare a țesuturilor și organelor, care este însoțită de o încălcare a activității lor vitale. Este obișnuit să se distingă modificările primare și secundare. Modificarea primară apare ca răspuns la efectul direct al factorului care provoacă inflamația. Reacțiile modificării primare ca și cum ar prelungi acțiunea factorului dăunător. Factorul în sine nu mai poate fi în contact cu corpul. Alterările secundare au loc sub influența atât a factorului care provoacă inflamația, cât și a factorilor de alterări primare. Efectul factorului dăunător se manifestă în primul rând pe membranele celulare, inclusiv cele lizozomale. Lizozomii sunt reactivi. Se duc afară și dăunează tuturor elementelor din celulă. Astfel, modificarea secundară este în primul rând auto-rău. În același timp, modificarea secundară este o componentă rezonabilă și necesară a inflamației - ca proces protector și adaptiv. Atacurile suplimentare contraceptive vizează localizarea precoce a factorului etiologic și a țesutului corporal deteriorat sub influența sa. La prețul daunelor, se obțin multe alte fenomene importante de protecție: activarea metabolismului, implicarea mediatorilor inflamatori și celulari, creșterea fagocitozelor etc. Schimbări metabolice la apariția inflamației apare predominant datorită hidrati de carbon. Inițial, datorită activării enzimelor tisulare, se intensifică atât fosforilarea oxidativă a carbohidraților, cât și a glicolizei. Ulterior, glicoliza începe să predomină asupra respirației. Acest lucru se datorează faptului că: 1. Creșterea consumului de oxigen de către țesutul inflamat. 2. Circulația sângelui este perturbată. Sângele scade conținutul de oxigen. 3. Acumularea în leziune a leucocitelor, enzimelor lizozomale, care descompun glucoza în principal anaerob, crește. 4. Se produce daune și reducerea numărului de mitocondrii. Produsele metabolismului carbohidrat sub-oxidat se acumulează în țesături: acizi lactici și tricarboxilici. încălcare metabolismul grasimilor constă în faptul că sub acțiunea enzimelor în primul rând lizozomale în focar inflamație acută Grăsimile se descompun pentru a forma acizi grași. În izbucnirea inflamației tulburate brusc schimb de proteine și acizi nucleici. Sub acțiunea enzimelor lizozomale și a altor enzime, se produce defalcarea proteinelor și acizilor nucleici la aminoacizi, polipeptide, nucleotide, nucleozide (adenozină). Ca urmare a tulburărilor metabolice ale carbohidraților, grăsimilor și proteinelor, produsele metabolice acide se acumulează în țesutul inflamat și dezvoltă metabolice acidoză. La început, este compensată de rezervele alcaline de sânge și de lichid de țesut. În viitor, cu epuizarea locală a rezervelor alcaline și cu dificultatea fluxului de sânge proaspăt, acidoza devine necompensată. Cu purulență acută pH-ul inflamației poate ajunge la 5,4 și la cronică - 6,6. Aci-dozele creează condiții favorabile pentru acțiunea anumitor enzime lizozomale, în special glicozidazele, care descompun componentele carbohidraților ale țesutului conjunctiv. Concentrația de ioni de hidrogen crește cu atât mai mult, cu atât inflamația este mai intensă. În direcția de la centru la periferie, concentrația de ioni de hidrogen scade treptat. Într-un mediu acid, disocierea sărurilor crește. Ca urmare, conținutul de ioni K, Na, Ca crește în focalizarea inflamației. Acest lucru se datorează, de asemenea, distrugerii celulelor și eliberării acestor săruri. Datorită formării reduse de macrogre, balanța de potasiu-sodiu din celulă este perturbată. Potasiul începe să părăsească celulele, sodiul, dimpotrivă, intră în celulă. Se prezintă hiperionul și diizonia. În același timp, concentrația moleculară crește, ca și în procesul de distrugere a țesuturilor și metabolismul afectat, moleculele mari se descompun în multe mici. Datorită creșterii concentrației ionice și moleculare, se dezvoltă hiperosmia. Hiperconia duce la hiperosmia - o creștere a concentrației de proteine în focalizarea inflamației. Hiperconia apare deoarece: 1) proteina este eliberată din sânge în focar inflamator, datorită faptului că acidoza și enzimele lizozomale măresc permeabilitatea peretelui vascular la proteină; 2) în condițiile acidozei, fisiunea proteinelor grosiere la fine. Mediatorii inflamatorii mediatori/ intermediari / inflamație - este un complex de substanțe fiziologic active care mediază acțiunea factorilor care cauzează inflamații și determină dezvoltarea și rezultatele inflamației. În timpul inflamației, ele se excretă în cantități mari și devin mediatori. pentru că ei sunt capabili să consolideze sau să slăbească manifestarea procesului inflamator pe care ei îl numesc modulatori. Legătura mediator este importantă în patogeneza inflamației. Principalele grupuri de mediatori inflamatori sunt: 1. Aminele biogenice - histamina, serotonina. Histamina, unul dintre cei mai importanți mediatori, este secretizată de bazofile și celulele mastocite și își realizează acțiunea prin intermediul receptorilor membranari. Eliberarea de histamină este una dintre primele reacții ale țesuturilor de deteriorare. Histamina determină vasodilatația, crește permeabilitatea vasculară datorată rotunjirii celulelor endoteliale și slăbirea contactelor intercelulare, crește producția pro-taglandinei E 2, reduce eliberarea enzimelor lizozomale, neutrofile. Să apară o persoană mâncărimi ale pielii, arsuri și durere. După eliberare, histamina este foarte rapid distrusă de enzima histaminază. Prin urmare, acțiunea sa se oprește rapid și alți mediatori, în special serotonina, sunt pornite. Acesta este conținut în neuro-creier, bazofile, trombocite. În centrul inflamației, serotonina în doze moderate determină dilatarea arteriolelor, reducerea miocitului în pereții venulelor și congestia venoasă. In plus, creste permeabilitatea peretelui vascular, creste cheagurile de sange, provoaca un sentiment de durere. Aminele biogenice interacționează între ele și cu alți mediatori inflamatori. De exemplu Al doilea grup de mediatori: sisteme plasmatice / kinine, complement, componente ale sistemului component, factori de coagulare a sângelui /. Cele mai importante kinine sunt bradikinina și kallidina. Punctul de plecare al activării sistemului de kinină este activarea factorului de coagulare 12 - factorul Hageman în cazul afectării țesutului. Acest factor transformă prekallikreiny în kallikreiny. Acestea din urmă acționează asupra kininogenului de proteine plasmatice și a plasmichininelor care se formează din acesta. Ele determină dilatarea arteriolelor și sporesc permeabilitatea venulelor, reduc mușchiul neted al venelor și măresc tensiunea arterială. Kininele inhibă emigrarea neutrofilelor, stimulează migrarea limfocitelor, secreția de limfokine și provoacă un sentiment de durere. Complementul este un sistem complex de plasmă care cuprinde cel puțin 18 proteine. Oferă liza celulelor străine și native modificate. Fragmentele complementare pot crește permeabilitatea vasculară, pot elibera hidrolaze lizozomale, participă la formarea leucotrienelor. Sistemul hemostazei și fibrinolizei promovează tromboza și formarea fibrinopeptidelor. Ele cresc permeabilitatea vaselor de sânge, stimulează formarea de kinine. Al treilea grup de mediatori sunt produse de acid arahidonic - prostaglandine și leucotriene. PG sunt produse de aproape toate tipurile de celule nucleare, dar predominant de leucocite. PG îmbunătățesc sau slăbesc acțiunea altor mediatori, inhibă sau măresc agregarea plachetară, dilată sau diluează vasele de sânge și măresc temperatura corpului. Leucotrienele se formează în membranele trombocitelor, bazofilelor, celulelor endoteliale. Ele cauzează agregarea leucocitelor, spasmul microvascular, permeabilitatea crescută, bronhospasmul. Al patrulea grup de mediatori - radicali de oxigen și hidroperoxid de lipide. În mitocondriile celulelor se formează radiații de oxigen, cum ar fi peroxidul de hidrogen, radicalul hidroxil etc. Când mitocondriile sunt deteriorate, radicalii acide sunt eliberați, interacționând cu lipidele membranare, formând hidroperoxiduri lipidice. Întregul complex de procese pentru generarea de radicali de oxigen și hidroperoxid de lipide se numește "sistem oxidativ". În centrul inflamației, procesele cu radicali liberi sunt activate și afectează membranele celulelor microbiene și proprii. Se formează așa-numita "explozie oxidativă". Este baza activității bactericide a fagocitelor. În plus, radicalii cresc permeabilitatea microvaselor, pot stimula proliferarea. Grupul 5 al mediatorilor este un mediator al leucocitelor polimorfonucleare / PMN / monocitelor și limfocitelor. PMN-urile emit un grup de mediatori extrem de activi care provoacă diverse reacții în focalizarea inflamatorie, formând manifestările sale. Unul dintre reprezentanți este factorul de activare a plachetelor (PAF). Ea crește permeabilitatea vaselor, provoacă agregarea plachetară, emigrarea leucocitelor. În plus, leucocitele secretă mediatori, cum ar fi prostaglanul E2, leucotrienele, tromboxanul A2 (crește coagularea sângelui, îngustă vasele coronare), prostaciclina (extinde vasele de sânge și reduce coagularea sângelui). Prostaciclinele și leucotrienele sunt importante la originea durerii inflamatorii. Monocitele și limfocitele secretă monokine și limfokine. De exemplu, limfocitele secretă un factor care inhibă macrofagele, factorul de stimulare a macrofagelor. Limfocienii coordonează interacțiunea dintre neutrofage, microfage și limfocite, care reglează răspunsul inflamator în general. Antimediatori de inflamație În toate stadiile de inflamație, substanțele care împiedică acumularea excesivă de mediatori sau opresc influența mediatorilor sunt eliberați și acționează. Acestea sunt în principal enzime: histaminază, inhibitori de carboxipeptidază kinină, inhibitori de esterază ai fracțiunii de complement. Eozinofilele joacă un rol important în formarea și livrarea anti-medicamentelor la focalizarea inflamatorie. Din anti-mediatori umorali, un rol important îl joacă alfa-1-antitripsina, care se formează în hepatocite. Este un inhibitor de protează. După cum rezultă din definiție A doua componentă a inflamației este o încălcare a microcirculației și a hemorheologiei în focalizarea inflamației. Se disting următoarele etape ale tulburărilor circulatorii: 1. Formarea hiperemiei arteriale. 2. Stadiul hiperemiei venoase, care trece prin mixt. 3. Următorul poate să vină stază de sânge. Forma rapidă a histaminei, kininelor, prostaglandinelor și a altor mediatori inflamatorii dilată arterele, arteriolele și asigură formarea hiperemiei arteriale. Un rol important în dezvoltarea hiperemiei arteriale și întreținerea acesteia aparține modificării sensibilității alfa-adrenoreceptorilor vaselor în condiții de aci-doză. Ca urmare, există o scădere a reacției vaselor la adrenalină și la influențele simpatice, care contribuie la extinderea sfincterilor arteriol și precapilare. În centrul inflamației datorate acidozelor, dioniei (concentrație crescută a ionilor K + în lichidul de țesut), efectul vasoconstrictiv al sfincterilor precapilare scade, de asemenea. Toți acești factori conduc la formarea hiperemiei arteriale. Hiperemia arterială se caracterizează prin creșterea volumului și a vitezei liniare a fluxului sanguin, a numărului de capilare care funcționează. O creștere a fluxului de sânge bogat în oxigen contribuie la creșterea proceselor redox și generarea de căldură. Prin urmare, în stadiul hiperemiei arteriale, o creștere a temperaturii în inflamația oculară este înregistrată subiectiv și obiectiv. Când inflamația crește permeabilitatea vaselor de sânge, ceea ce contribuie la eliberarea proteinelor și a apei în centrul inflamației. Mai întâi, există albumină, în legătură cu care crește cantitatea de globulină și fibriogen în sânge. Acest lucru implică o creștere a vâscozității și a concentrației sanguine, rezultatul fiind o încetinire a fluxului sanguin și formarea de agregate de celule roșii din sânge. Ca rezultat al acumulării de lichid și mai târziu a elementelor formate în țesut, vastele limfatice și sanguine sunt comprimate, ceea ce face dificilă scurgerea sângelui și a limfei. Agregarea elementelor uniforme, formarea lor de pastă și nămol se dezvoltă în vase. Pentru dulciuri, este caracteristică agregarea eritrocitelor sub formă de coloane de monede. Cu un dulce, membrana eritrocitară nu se descompune, astfel încât nămolul se poate descompune. În paralel cu aceasta, sistemul de coagulare a sângelui este activat prin formarea cheagurilor de sânge și a tromboembolismului. Toate aceste modificări contribuie la creșterea vâscozității dinamice a sângelui și la deteriorarea proprietăților sale reologice. De asemenea, cauza formării microtrombozelor și a hemoragiei este afectarea directă a peretelui vascular, un factor care determină inflamația, activarea factorului Hageman, acțiunea mediatorilor / enzimelor lizozomale, bradikinina, kallidina /. Celulele roșii din sânge părăsesc vasele prin spațiile interendoteliale. Astfel, hiperemia arterială se alătură foarte rapid venelor, ale căror manifestări cresc progresiv. În stadiul hiperemiei venoase, scurgerea sângelui din sursa de inflamație este perturbată, viteza liniară și volumetrică a fluxului sanguin scade, presiunea hidrostatică crește, iar fluxul de sânge asemănător cu jogul și pendulul se dezvoltă. Odată cu dezvoltarea inflamației și a hiperemiei venoase, apare o încetinire progresivă a fluxului sanguin. Aceasta se datorează: a) unei creșteri excesive a suprafeței secțiunii transversale a dorsului vascular datorită dilatării maxime a capilarelor și deschiderii venelor; b) un obstacol mecanic în calea fluxului de sânge și limfă de la focalizarea inflamației, în principal datorită comprimării vaselor venoase și limfatice, ) o creștere a rezistenței la fluxul sanguin datorită rugozității peretelui interior al vaselor mici de la leucocitele aderente la acesta, precum și umflarea celulelor endoteliale d) îngroșarea în continuare a sângelui și creșterea vâscozității sale datorită creșterii despre eliberarea fluidului din vase în țesut. În cele din urmă, există o oprire a mișcării sângelui - stază. Staza este înregistrată inițial în capilare și venule separate, mai târziu acoperă tot mai multe vase. La urma urmei, staza se dezvoltă în ateriole. În funcție de severitatea inflamației, staza poate fi de scurtă durată, poate persista ore întregi sau poate fi ireversibilă. Consecința stazei poate fi schimbările ireversibile ale celulelor sanguine și ale țesuturilor. transpirație transpirație - aceasta este ieșirea părții lichide a sângelui în inflamație. Ea se realizează în trei moduri: 1. Prin intermediul fantelor interendoteliale, a căror mărime crește datorită reducerii celulelor endoteliale din microfibre. 2. Prin corpul celulelor endoteliale prin canale specializate. 3. Calea de micropinocitoză sub formă de conducere activă a celor mai mici picături prin corpul celulei. Au fost identificate două faze de creștere a permeabilității peretelui vascular în focar inflamator: 1. Creșterea rapidă a permeabilității vasculare datorată acțiunii substanțelor vasoactive. 2. Întârziere (întârziată, lungă) asociată cu acțiunea PMC-leucocitelor. Granulele de leucocite conțin substanțe biologic active care sunt eliberate în timpul degranulării și fagocitozei. Procesul de acumulare a leucocitelor PMN și degranularea lor este un proces lung. Acesta este motivul pentru care furnizează a doua fază a creșterii permeabilității. Creșterea permeabilității vasculare se datorează următoarelor factori: 1. Acțiunea directă a factorului (otrăvuri animale, toxine bacteriene etc.). 2. Acțiunea unui BAS (histamină, serotonină, kinine etc.) 3. Acidoză. Aceasta duce la lichefierea coloizilor și slăbirea conexiunilor interendoteliale. Permeabilitatea crescută a vaselor conduce la eliberarea proteinelor și a elementelor sangvine în zona inflamată. Eliberarea apei și a substanțelor dizolvate în ea se datorează: 1. Creșterii ariei de filtrare și difuziei. 2. Creșterea tensiunii arteriale în capilare și venule. 3. Creșterea presiunii osmotice în țesutul inflamat. Edemul limfatic. Este chemat fluidul care intră în țesutul inflamat ekssu- luigi Datome. Conține o cantitate mare de proteine (30-50 g / l), celule din sânge, celule de țesut deteriorat. Exudatul noninflamator - transudat, conține mult mai puțină proteină, corpusculă sanguină, celule de țesut deteriorat. În paralel cu eliberarea proteinelor și a apei în timpul inflamației, procesul de emigrare a leucocitelor se desfășoară. Migrarea la leucocite Ieșirea leucocitelor este precedată de mișcarea peretelui și starea lor, care se observă în special în stadiul hiperemiei venoase. Acest fenomen se explică printr-o scădere a încărcăturii negative a leucocitelor, microcoagulării în apropierea peretelui, ca urmare a faptului că microfibrele inhibă mișcarea leucocitelor și contribuie la starea lor de perete aproape. Mai mult I.I.Mechnikov a remarcat că leucocitele PMN apar mai întâi în inflamație, apoi monocite și ultimele limfocite. Leucocitele emigrează în două moduri: leucocitele PMN ieșesc prin interendoteliene și celulele mononucleare prin corpul celulelor endoteliale. Ultimul proces este cel mai consumator de timp și acest lucru explică de ce celulele mononucleare apar ulterior în zona inflamată. Membrana bazală a elementelor sangvine este depășită pe baza unei scăderi reversibile izotermice a vâscozității unei soluții coloidale (tixotropie), adică tranziția gelului la sol atunci când leucocita este atașată la membrană. Leucocita, depășind cu ușurință solul, se dovedește a fi în afara vasului, iar membrana se transformă din nou într-un gel. În acest proces, enzimele sunt implicate, și mai presus de toate colajul-Naza. O anumită influență asupra secvenței de emigrare are pH-ul sursei de inflamație. La pH 7,4-7,2, leucocitele PMN se acumulează, la pH 7,0-6,8, celulele mononucleare și la pH 6,7, toate leucocitele mor în nidul inflamației pentru a forma puroi. Important în emigrarea leucocitelor aparține chemotak-sisu. Se formează cu participarea complementului. Utilizarea inhibitorilor complementului previne deteriorarea vaselor și eliberarea leucocitelor. Chemotaxa este stimulată de streptokinază. Chemotoxinele apar când deteriorarea mecanică țesut, cu inflamație infecțioasă datorată acțiunii endotoxinelor. Chemotoxinele sunt, de asemenea, formate de limfocite în timpul defalcării gamaglobulinelor. Chemotaxa este stimulată de produsele metabolice ale țesuturilor, bacteriilor, virusurilor și sistemului de kallikreină. Un anumit rol în emigrarea leucocitelor îl joacă așa-numitele surfactanți, care pot reduce tensiunea superficială. De exemplu: acizi organici. Prin modificarea tensiunii superficiale a leucocitelor, acestea îi determină pe aceștia să dezvolte proeminențe citoplasmatice și să formeze pseudopodia. Treptat, întregul leucocit se deplasează în el, depășind în întregime vasul. Soarta leucocitelor eliberate din vase depinde de mediul în care acestea cad. Dacă inflamația este aseptică în natură, atunci leucocitele emigrate mor rapid în timpul 3-5 zile. Dacă inflamația are un caracter septic, atunci numărul de leucocite în focalizarea inflamatorie crește progresiv. Începe supurația. Unele leucocite situate în centrul focarului inflamator mor. Partea prezintă activitate fagocitară. Activitatea enzimatică este în creștere: mieloperoxidază, hidrolaze acide care distrug bacteriile localizate extracelular. În ciuda faptului că placa bacteriană este cauza principală a dezvoltării bolilor parodontale inflamatorii, numai efectul acesteia nu poate explica gravitatea distrugerii parodontale. Reacția organismului joacă un rol esențial în dezvoltarea boala parodontală. Corpul uman are un set complex de mecanisme de protecție interdependente destinate eliminării microorganismelor, realizării vindecării și menținerii unei stări sănătoase. Paradoxal, același sistem, care este destinat să protejeze și să vindece organismul, duce la afectarea țesutului în bolile parodontale. Imunologia este un subiect extrem de complex. Mai mult decât atât, este destul de dificil să se separe astfel de noțiuni ca răspuns inflamator și imun, deoarece în multe situații acțiunea lor se suprapune reciproc. Acest capitol oferă o prezentare generală a manifestărilor răspunsului inflamator și imun, precum și rolul lor în vindecarea și distrugerea bolii parodontale. Vor fi abordate următoarele subiecte:
inflamație Inflamația este o secvență clară a evenimentelor care se dezvoltă ca răspuns la orice leziune sau infecție, având astfel un caracter "nespecific". Inflamația este răspunsul primar care are loc înainte de activarea sistemului imunitar. Procesul de inflamație se caracterizează prin trei etape:
Înainte de a începe discutarea procesului în sine, să prezentăm principalele elemente celulare și moleculare ale inflamației. Elementele celulare ale inflamației Principalele celule responsabile pentru inflamație sunt leucocitele (PMN), care se formează în măduva osoasă din aceleași celule stem ca monocitele. Markerii specifici ai suprafeței celulare determină ce cale va duce la dezvoltarea promiloelocitelor - de-a lungul căii de formare a macrofagelor sau PMN. Aceste markere dispar după finalizarea diferențierii. Prezența mai multor PMN în epiteliul atașat este considerată normală. Creșterea numărului lor este un semn al inițierii reacției organismului. PMN sunt fagocite și reprezintă până la 70% din numărul total de leucocite. Citoplasma PMN conține elemente care sunt responsabile de mișcarea celulelor în timpul activării chemotaxisului, precum și de lizozomii care distrug bacteriile. Distrugerea bacteriilor de către aceste celule, de obicei, dar nu întotdeauna, apare după ce microorganismele sunt absorbite de PMN (adică după fagocitoză). Următoarele celule implicate în răspunsul inflamator sunt macrofagele, care sunt formate din monocite circulante și apar în zona inflamației după PMN. Macrofagele sunt celule mari cu aceleași abilități fagocitare cu PMN. În plus, macrofagele joacă un rol important în răspunsul imun. Limfocitele penetrează ultima zonă a inflamației și sunt asociate în primul rând cu inflamația cronică. În plus, limfocitele sunt celulele principale ale sistemului imunitar. Celulele mamare sunt aceleași ca bazofilele circulante. Ei eliberează histamina, factorul de activare a plachetelor (PAF), prostaglandina E2 și leucotrienii (LTB4 și LTD4), fiecare dintre aceste elemente are un efect inflamator pronunțat. Plachetele eliberează serotonina (un mediator important al inflamației). Componentele moleculare ale inflamației Histamina crește permeabilitatea pereților vaselor de sânge, facilitând astfel accesul celulelor inflamatorii în zona afectată. Histamina este eliberată de celulele mastocite și bazofilele. Serotonina (5-hidroxi-triptamina) crește, de asemenea, permeabilitatea vasculară. Basofilele, neutrofilele și macrofagele eliberează factorul de activare a trombocitelor (PAF). PAF crește eliberarea de serotonină din trombocite. Factorul de chemotaxie neutrofil (NCF) este eliberat din celulele mastocitare și reglează chemotaxia PMN. Chemokinele sunt eliberate de leucocite. Acestea constituie un grup mare de citokine care provoacă degranularea celulelor mastocite și chemotaxia PMN. Avertisment: Terminologia poate părea destul de confuză. Toate moleculele care afectează răspunsul imun sau inflamator sunt numite citokine. În concordanță cu aceasta, toate chemokinele sunt citokine, dar există un număr mare de citokine care nu sunt chemokine. Suplimentul activat SZ provoacă degranularea celulară. Suplimentul activat C5a conduce la degranularea celulelor mastocite, chemotaxia fagocitară, activarea PMN și creșterea permeabilității capilare. Bradykinina (un element al sistemului kininic) provoacă vasodilatație și crește permeabilitatea vasculară. Fibrinopeptidele sunt produse ale mecanismului de coagulare și afectează chemotaxia PMN și a macrofagelor. Prostaglandina E2 (PGE2) este un produs al ciclooxigenazei și provoacă vasodilatație, simultan cu o creștere a permeabilității vasculare sub acțiunea histaminei și bradikininei. Leukotriena B4 (LTB4) este formată în timpul ciclului de lipoxigenază. Stimulează chemotaxia PMN și în mod sinergie cu PGE2 conduce la o creștere a permeabilității peretelui vascular. Leukotrienul D4 (LTD4), care se formează și în timpul ciclului de lipoxigenază, crește permeabilitatea vasculară. Factorul de chemotaxie neutrofil (NCF) este eliberat de bazofili. Selectinele sunt un grup de trei molecule care facilitează migrarea PMN și a macrofagelor prin peretele vascular. Selectins E și selectins P sunt specifici pentru PMN, iar selecția în L este pentru macrofage. Selectine încetinesc mișcarea celulelor, ceea ce contribuie la aderarea acestora la peretele vaselor. Cele trei grupuri, inclusiv grupul cunoscut sub numele de ICAMS, includ cel puțin 12 molecule care îndeplinesc funcții similare. Inflamația acută în bolile parodontale După cum sa menționat mai sus, procesul de inflamare acută include trei etape. Pe măsură ce placa bacteriană se acumulează în canelură, apar următoarele evenimente. Sursa de sânge crește din cauza expansiunii vaselor de sânge din zona afectată. Unii mediatori cauzează vasodilatație, de exemplu, histamină și PGE2. Serotonina, C5a, bradikinina, fibrinopeptidele, PGE2, LTB2 și LTD2 măresc permeabilitatea peretelui vascular și măresc spațiul dintre celulele endoteliale. Selectins și ICAMS încetinesc mișcarea PMN, permițând acesteia din urmă să pătrundă în țesut conjunctiv. Migrația și funcția fagocitară a PMN sunt reglementate de factori chemotactici, cum ar fi NCF. Chemokines, C5a, fibrinopeptide LTB4 și, de asemenea, să promoveze fagocitoza și chemotaxia neutrofilelor. Principalele celule fagocitare, care sunt implicate în răspunsul organismului la invazia infectioase sunt polimorfonucleare neutrofile și macrofage. Distrugerea microorganismelor, de obicei, dar nu întotdeauna, are loc după absorbția lor de către celule. Deteriorarea anumitor membrane celulare poate duce la formarea și eliberarea factorilor care duc la apariția simptomelor clinice ale inflamației.
Unsprezece proteine clasice
Granulele sunt de asemenea numite lizozomi sau "pachete sinucidere". enzime care distrug celulele bacteriene și celulele organismului fagocite Fagocitoză independentă de oxigen Acest proces are loc ca urmare a unui număr mare de substanțe distructive prezente în organite care sunt localizate în citoplasmă fagocite. Astfel de organele sunt numite granule sau lizozomi. Activitatea enzimei distructive duce la eliberarea conținutului de granule și alți factori care au legătură cu grupările cationice ale proteinelor, proteaza neutre, hidrolaze acide și alte substanțe, cum ar fi lactoferina. Enzimele distrug bacteriile după ce sunt absorbite de fagocite. Cu toate acestea, în procesul de fagocitoză, unele enzime poate „scurgeri“ de macrofage și de a interacționa cu structurile din jurul celulei. Posibil, acest fenomen este de mare importanță în canelurile de fluid sau buzunare în cazul în care bacteriile distrugerea începe fără absorbție prealabilă, care ajută la protejarea tesuturilor parodontale. Mai mult decât atât, enzimele lizozomale pot juca un rol important în neutralizarea acțiunii enzimelor distructive și a toxinelor sintetizate și eliberate de bacterii, indiferent dacă aceste enzime și toxine absorbite anterior de fagocite. Fagocitoză dependentă de oxigen Acest proces duce la distrugerea bacteriilor localizate în organele celulare, numite phagolysosomes. În timpul acestuia, oxidanți toxici și peroxid de hidrogen sunt eliberați din radicalii de oxigen și enzima lizozomală mieloperoxidază, ceea ce duce la moartea masivă a celulelor bacteriene ca urmare a deteriorării peretelui lor celular. În cursul multor studii, sa studiat relația dintre neutrofilele polimorfonucleare (PMN) și starea țesuturilor parodontale. Bolile parodontale sunt mai frecvente și mai severe în prezența neutrofilelor la oameni sau animale, cum ar fi agranulocitoza sau insuficiența de aderare la leucocite. La animalele cu scăderea numărului sau a insuficienței congenitale a PMN, sa produs distrugerea parodontală rapidă și pierderea dinților. Studiile clinice care implică un număr mare de pacienți au demonstrat că prezența insuficienței funcționale a PMN la pacienți este un factor de risc ridicat pentru distrugerea țesuturilor parodontale. În 1996, la Congresul Internațional de Parodontologie, Offenbacker a sugerat că pacienții cu PMN normali sunt susceptibili să dezvolte gingivită, dar nu și parodontita, indiferent de gradul de încărcare bacteriană. Pe de altă parte, prezența insuficienței funcționale a PMN în majoritatea cazurilor este însoțită de o pierdere de atașament. Rezultatele acestor studii sugerează că PMN joacă un rol crucial în asigurarea unei condiții parodontale sănătoase, dar pot duce la distrugerea țesuturilor parodontale. Distrugerea țesuturilor corporale Este bine cunoscut faptul că organismul în sine conduce la o distrugere semnificativă a propriilor țesuturi în timpul dezvoltării bolilor parodontale. Astfel de leziuni pot fi considerate ca o reacție patologică în prezența cronicilor boala inflamatorie. Următoarele substanțe au capacitatea de a distruge țesuturile parodontale în procesul de reacție defensivă a organismului împotriva bacteriilor și a produselor metabolice ale acestora.
Sistem de completare serică Sistemul de complement al serului constă din mai mult de 20 de proteine din zer care, atunci când sunt activate, posedă activitate biologică. Acest sistem joacă un rol extrem de important în răspunsul inflamator și imun. Există două mecanisme principale de activare a proteinelor din sistemul de complement. Primul mecanism clasic este activat după ce anticorpul se leagă de suprafața peretelui bacterian. Al doilea mecanism alternativ poate fi activat direct de componentele peretelui unor bacterii gram-negative. Astfel de componente sunt numite endotoxine. Mai jos sunt doar câțiva dintre mulții factori de activare a complementului seric care sunt implicați în ambele mecanisme.
Biologic factori activi produși în sistemul complement seric este probabil să joace un rol important în protejarea organismului împotriva infestării microbiene in tesutul periodontal, deoarece acestea conduc la distrugerea bacteriilor și a altor mecanisme de deschidere de apărare, care permit reducerea concentrației de microorganisme. Ca și în cazul tuturor mecanismelor de protecție atunci când complementul este activat, există o posibilitate de deteriorare a țesuturilor parodontale. La finalul acestui capitol se va discuta despre particularitățile afectării țesuturilor parodontale prin anticorpi și fagocite induse de complement. Cu toate acestea, pe lângă aceasta, datorită activării sistemului de complement, poate să apară distrugerea membranelor celulelor proprii ale corpului, în special celulele roșii din sânge. Activarea complementului poate duce la distrugerea țesuturilor parodontale, care determină simptomele clinice ale bolii. IMUNOLOGIE În mod tradițional, considerăm două părți ale sistemului imunitar: imunitate celulară și imunitate umorală. În ciuda oportunității unei astfel de separări, imunologii încearcă în prezent să caracterizeze sistemul imunitar prin elemente care recunosc antigene celulare și prin elemente care recunosc antigene libere. Elemente celulare ale sistemului imunitar
Citokine și alte elemente moleculare Citokinele nu sunt legate de molecule de anticorpi, care au capacitatea de a afecta multe componente ale răspunsului imun și inflamator, cum ar fi cascada compliment, bradikinină, procesul de coagulare și cascada acidului arahidonic. Cele mai importante citokine includ:
Imunoglobuline (anticorpi)
Răspunsul imun în boala parodontală Odată cu acumularea de plăci bacteriene în zona canelurii, trece o scurtă perioadă de timp (de obicei, câteva zile), timp în care anticorpii nu sunt detectați. După câteva zile, organismul începe să reacționeze la prezența bacteriilor și a produselor lor metabolice. Fibroblastele, macrofagele și limfocitele eliberează IL-1, IL-2, IL-6 și IL-8. Se produce activarea selectinelor și 1C AM, care inițiază diapedesis (percolarea prin peretele vascular), migrarea și chemotaxia leucocitelor polimorfonucleare. Procesul de diapedeză este accelerat, iar PMN este urmat de macrofage. Ambele tipuri de celule sunt activate de citokine. Din punct de vedere clinic, acest lucru se manifestă prin roșeață primară cu gingivită. Antigenii sunt "eliberați" celulelor B și monocitelor folosind celule T helper. În cele din urmă, citokinele sunt eliberate. Aceasta conduce la producerea de celule B, care formează anticorpi specifici pentru fiecare antigen. Antigenii suferă opsonizare și fagocitoză, ducând la eliberarea de substanțe care dăunează colagenului și substanței principale. SZa și C5a conduc la eliberarea histaminei de către mastocitele, aceasta cauzează vasodilatație și facilitează migrarea către zona interesată a unui număr mai mare de celule de protecție. În cele din urmă, epiteliul ulceratului canelurilor, care contribuie la o penetrare și mai rapidă a antigenilor bacterieni. În acest moment, gingiile se umflă, sângerau și pot fi puțin dureroase. Citokinele produse de fibroblaste, PMN și alte celule pot juca un rol atât de protejat și dăunător. Zona afectată este infiltrate cu limfocite și celule plasmatice. În absența tratamentului sau în cazul insuficienței mecanismelor de apărare, pierderea atașamentului apare ca urmare a acțiunii bacteriilor și ca rezultat al răspunsului organismului la un iritant bacterian. concluzie Într-o stare de sănătate între bacterii și mecanismele de apărare ale corpului există un echilibru. Odată cu dezvoltarea bolii, acest echilibru este perturbat, bacteriile și eforturile organismului de a distruge bacteriile și de a le vindeca, duc la distrugerea țesuturilor parodontale. Un astfel de dezechilibru poate apărea ca urmare a acțiunii factorilor de virulență, a mecanismelor de apărare sau a factorilor externi, de exemplu, sub influența fumatului. Alphabetul parodontal |
| Citește: |
|---|
Cele mai populare:
Birch agățat sau rău
|
nou
- Programul de hidratare intensă a pielii pe coaja cosmeticelor
- Ce ai nevoie pentru pulbere acrilică
- Ce înseamnă mascota de bufniță?
- Analizele pentru pancreatită: ce trebuie făcut și ce indicatori indică
- Owl - un talisman pentru a atrage bani și noroc
- Ce pasăre țipă noaptea cu vocea unui pisoi?
- Colesterolul și stresul
- Manichiura acasa
- Efect facial
- Ce este un om după un picior rupt?