サイトセクション
編集者の選択:
広告宣伝
| 人間の免疫システムとその臓器 人間の免疫システム |
|
免疫系は特定の組織、器官および細胞の集まりです。 これはかなり複雑な構造です。 次に、そこに含まれている要素と、免疫システムの機能について調べます。 一般的な情報免疫システムの主な機能 - 体内に閉じ込められた異物の駆除、そしてさまざまな病状からの保護。 構造は、真菌性、ウイルス性、細菌性の感染に対するバリアです。 人が弱いときや仕事に失敗したときには、体内への外来物質の侵入の可能性が高まります。 その結果、さまざまな病気が発生する可能性があります。 歴史的背景「免疫」の概念は、ロシアの科学者Mechnikovとドイツの指導者Erlichによって科学に導入されました。 彼らは身体の様々な病理との闘争の過程で活性化されている既存のものを調査した。 まず第一に、科学者たちは感染に対する反応に興味を持っていました。 1908年に、免疫反応を研究する分野での彼らの研究はノーベル賞を受賞しました。 また、行われた研究とフランス人ルイパスツールの作品への重要な貢献。 彼は人間にとって危険であった多くの感染症に対する予防接種方法を開発しました。 当初、身体の保護構造は感染を排除するためだけにそれらの活性を指示すると考えられていました。 しかし、その後のイギリス人メダワールによる調査は、免疫メカニズムがあらゆるエイリアンエージェントの侵入に作用し、実際にあらゆる有害な干渉に反応することを証明した。 今日では、保護構造の下で主に様々な抗原に対する体の耐性を理解しています。 さらに、免疫は身体の反応であり、駆除だけでなく「敵」を排除することも目的としています。 身体の防御がなければ、人々は通常の環境条件では存在できません。 免疫の存在は、病理学に対処して、老年まで生きることを可能にします。 免疫システム臓器それらは2つの大きなグループに分けられます。 中枢免疫系は保護要素の形成に関与しています。 ヒトでは、胸腺と骨髄はこの構造の一部です。 免疫系の末梢器官は、成熟した防御要素が抗原を中和する環境です。 構造のこの部分には、消化管のリンパ節、脾臓が含まれます。 CNSの皮膚および神経膠細胞が保護特性を有することも確立されている。 上記に加えて、免疫系のバリア内およびバリアフリーの組織および器官もある。 第一のカテゴリーは皮膚を含む。 免疫組織の関門組織および臓器:中枢神経系、眼、精巣、胎児(妊娠中)、胸腺実質。 構造化タスクリンパ系構造中の免疫担当細胞は、主にリンパ球に代表されます。 それらは構成保護成分間でリサイクルされる。 骨髄や胸腺には戻らないと考えられています。 臓器の免疫系の機能は以下の通りです:  リンパ節この要素は柔らかいティッシュによって形作られます。 リンパ節は楕円形です。 大きさは0.2〜1.0 cmで、免疫担当細胞が多数含まれています。 教育には、毛細血管を通って流れるリンパと血液の交換のための大きな表面を形成することを可能にする特別な構造があります。 後者は細動脈から来て、細静脈を通過します。 リンパ節には細胞の免疫化と抗体の形成があります。 さらに、地層は、異物および小粒子を濾過する。 体の各部分のリンパ節には、独自の抗体セットがあります。 脾臓外見上、それは大きなリンパ節に似ています。 以上が臓器の免疫系の主な機能です。 脾臓は他にもいくつかの作業を行います。 例えば、リンパ球の産生に加えて、血液がその中で濾過され、その要素が保存されます。 古くて欠陥のある細胞の破壊が起こるのはここです。 脾臓の重さは約140〜200グラムです。 そのリンパ組織は網状細胞のネットワークとして表されます。 それらは正弦波(毛細血管)の周りに位置しています。 基本的に、脾臓は赤血球または白血球で満たされています。 これらの細胞は互いに接触しておらず、組成および量が異なる。 平滑筋莢膜ストランドの減少と共に、いくつかの可動要素が排出される。 その結果、脾臓の容積が減少します。 この全過程はノルエピネフリンとアドレナリンによって刺激されます。 これらの化合物は節後交感神経線維または副腎の脳領域によって分泌されます。 骨髄こちらの商品は柔らかい海綿状の生地です。 それは平らで管状の骨の内側にあります。 免疫系の中枢器官は必要な要素を作り出し、それらは体の各ゾーンにさらに分布しています。 骨髄では、血小板、赤血球、白血球が産生されます。 他の血球と同様に、免疫能力を獲得した後に成熟します。 言い換えれば、受容体はそれらの膜上に形成され、他の類似のものとの要素の類似性を特徴付けるであろう。 扁桃腺、腸の胸腺、胸腺などの免疫系の器官の保護特性の獲得のための条件を作り出すことに加えて。 後者では、Bリンパ球の成熟が起こり、膨大な数(Tリンパ球の百分の一から二百倍大きい)の微絨毛を有する。 血流は、正弦波を含む血管を通って行われます。 骨髄を通してそれらを通してホルモン、タンパク質および他の化合物だけでなく浸透します。 シヌソイドは、血球を動かすためのチャネルです。 ストレス下では、電流はほぼ半分になります。 鎮静作用により、血液循環は8倍になります。 パイエル板これらの元素は腸壁に集中しています。 それらはリンパ組織の塊の形で提示される。 主な役割は循環システムに属します。 それはリンパ節を結ぶリンパ管からなる。 液体はこれらのチャンネルを通って輸送されます。 彼女は色がありません。 多数のリンパ球が体液中に存在します。 これらの要素は病気から体を保護します。 胸腺胸腺とも呼ばれます。 胸腺では、リンパ系の要素が増殖して成熟します。 胸腺は内分泌機能を果たします。 サイモシンはその上皮から血中に放出されます。 さらに、胸腺は免疫産生器官です。 その中でTリンパ球の形成が起こる。 このプロセスは、子供の頃に体内に浸透した外来抗原に対する受容体を持つ要素の分割によるものです。 Tリンパ球の形成は、血中のそれらの数にかかわらず行われる。 抗原のプロセスや含有量には影響しません。 若い人や子供の胸腺は、年配の人よりも活発です。 何年にもわたって、胸腺のサイズは縮小されており、その作業はそれほど速くはありません。 Tリンパ球の抑制はストレス下で起こります。 それは、例えば、風邪、暖かさ、精神的 - 精神的ストレス、失血、絶食、過度の身体運動についてであり得る。 ストレスを受けている人々では、免疫力は弱いです。 その他の項目免疫系の器官にも付録が含まれています。 腸管扁桃とも呼ばれます。 結腸の最初の部分の活動の変化の影響下で、リンパ組織の量も変化します。 そのスキームが下に位置する免疫系の器官も扁桃腺を含みます。 それらは咽頭の両側にあります。 扁桃腺はリンパ組織の小さな蓄積によって表されます。 体の主な擁護者免疫系の二次臓器および中枢臓器は上記の通りである。 この記事で紹介されているスキームは、その構造が体全体に分布していることを示しています。 主な防御者はリンパ球です。 罹患した要素(腫瘍、感染した、病的に危険な)または外来の微生物の破壊の原因となるのはこれらの細胞です。 最も重要なのはTおよびBリンパ球です。 彼らの研究は他の免疫細胞と連携して行われています。 それらはすべて、体内への異物の侵入を防ぎます。 初期段階では、Tリンパ球は何らかの形で正常な(それ自身の)タンパク質と他のタンパク質を区別するために「学習」しています。 胸腺が最も活発になるのはこの時期の間なので、この過程は小児期の胸腺で起こります。 身体保護ワーク免疫システムは長い進化の過程で形成されたと言われるべきです。 現代の人間では、この構造はデバッグされたメカニズムとして機能します。 それは人が環境条件の悪影響に対処するのを助けます。 構造のタスクは、認識だけでなく、身体に入った異物、そして腐敗産物、病理学的に変化した要素の排除も含みます。 免疫システムは、多数の異物や微生物を識別することができます。 構造の主な目的は、内部環境とその生物学的個性の整合性を保つことです。 認識プロセス免疫システムはどのように「敵」を定義しますか? このプロセスは遺伝子レベルで起こります。 ここで各細胞は与えられた人だけに特有のそれ自身の遺伝情報を持っていると言われるべきです。 それは身体への浸透またはそれの変化を検出する過程で保護構造によって分析されます。 入ってくるエージェントの遺伝情報がそれ自身のものと一致するならば、これは敵ではありません。 そうでなければ、それに応じて、それはエイリアンエージェントです。 免疫学では、「敵」は抗原と呼ばれます。 保護構造の悪意のある要素の検出にそのメカニズムが含まれた後、「闘争」が始まります。 それぞれの特定の抗原に対して、免疫系は特定の細胞 - 抗体を産生します。 それらは抗原に結合してそれらを中和する。 アレルギー反応それは防衛メカニズムの一つです。 この状態はアレルゲンに対する反応性の増加を特徴としています。 これらの「敵」には、体に悪影響を及ぼす物や化合物が含まれます。 アレルゲンは外部と内部です。 最初のものには、例えば、食品、医薬品、さまざまな化学物質(消臭剤、香水など)が含まれます。 内部アレルゲンは、一般に、性質が変化した生物自体の組織です。 たとえば、やけどの場合、防御システムは死んだ構造物を異星人として認識します。 この点で、彼女はそれらに対する抗体を生産し始めます。 ミツバチ、スズメバチ、その他の昆虫に対する反応も同様です。 アレルギー反応の発症は、連続的または激しく起こり得る。 子供の免疫システムその形成は妊娠の最初の数週間で始まります。 子供の免疫システムは出生後も進化し続けます。 主要な保護要素の敷設は胸腺と胎児の骨髄で行われます。 赤ちゃんが子宮内にいる間、彼の体は少数の微生物で発見されます。 これに関して、その保護機構は不活性である。 出生前は、子供は母親の免疫グロブリンによる感染から保護されています。 それが何らかの要因によって悪影響を受けた場合、乳児の保護具の適切な形成および発達が損なわれる可能性があります。 この場合出産後、子供は他の子供よりも病気になることがあります。 しかし、物事は異なるように起こる可能性があります。 例えば、妊娠中に、子供の母親は感染症を患う可能性があります。 そして胎児はこの病状に対する強い免疫を形成することができます。 生後、体は膨大な数の細菌に攻撃されます。 免疫システムはそれらに抵抗しなければなりません。 人生の最初の年の間に、体の保護構造は抗原の認識と破壊において一種の「訓練」を受けます。 同時に、微生物との接触が記憶されます。 その結果、「免疫学的記憶」が形成される。 既知の抗原に対する反応のより迅速な出現のために必要である。 私たちは新生児の免疫力が弱いと仮定しなければなりません、彼はいつも危険に対処することができるというわけではありません。 この場合、母親から子宮内に由来する抗体の助けを借りてください。 彼らは人生の最初の約4ヶ月間、体内に存在しています。 次の2か月にわたって、母親由来のタンパク質は徐々に破壊されていきます。 4〜6ヶ月の期間では、赤ちゃんは最も病気にかかりやすいです。 子供の免疫システムの集中的な形成は7年まで起こります。 開発の過程で、体は新しい抗原と知り合いになります。 この期間全体の免疫システムは、成人向けに訓練され準備されています。 壊れやすい体を助ける方法は?専門家は、出生前に子供の免疫システムの世話をすることをお勧めします。 これは、妊婦が保護構造を強化する必要があることを意味します。 出生前の期間では、女性は特別な微量栄養素とビタミンを摂取するために、正しく食べる必要があります。 適度な運動も免疫にとって重要です。 生後1年目の赤ちゃんは母乳を飲まなければなりません。 それは少なくとも4 - 5ヶ月間母乳育児を継続することをお勧めします。 赤ちゃんの体の中の牛乳で保護要素を貫通する。 この期間中、それらは免疫にとって非常に重要です。 子供はインフルエンザの流行中に鼻に牛乳を埋めることさえできます。 それは多くの有用な化合物を含み、あなたの子供がマイナス要因に対処するのを助けます。 追加の方法免疫システムの訓練はさまざまな方法で行うことができます。 最も一般的なのは、硬化、マッサージ、換気のよい部屋での体操、日光浴と空気浴、水泳です。 免疫のためのさまざまな手段もあります。 そのうちの一つは予防接種です。 それらは、防御機構を活性化し、免疫グロブリンの産生を刺激する能力を有する。 特別な血清の導入により、導入された物質に対する身体構造の記憶が形成される。 免疫のためのもう一つの手段は特別な準備です。 彼らは体の保護構造の活動を刺激します。 これらの薬は免疫刺激薬と呼ばれています。 これらは、インターフェロン製剤(「Laferon」、「Reaferon」)、インターフェロン原(「Poludan」、「Abrizol」、「Prodigiosan」)、白血球産生刺激剤 - 「メチルウラシル」、「ペントキシル」、微生物起源の免疫刺激剤 - 「Prognozan」、「Pyrogenogen」です。 、 "Bronhomunal"、植物由来の免疫賦活剤 - レモングラスのチンキ剤、Eleutherococcusの抽出物、ビタミンなど。 その他 免疫学者や小児科医だけがこれらの薬を処方することができます。 このグループの薬物を単独で使用することはお勧めできません。 免疫療法の問題は、基礎療法の有効性が低いこと、悪性腫瘍、自己免疫およびアレルギー性疾患、全身性疾患、高レベルを引き起こすウイルス感染を背景とした慢性および再発の傾向がある感染性および炎症性疾患の着実な成長に起因しています。 罹患率、死亡率および身体障害。 人の間で広がっている体性および感染性疾患に加えて、人体は社会的影響(不適切で不十分な栄養、住居環境、職業上の危険)、環境要因、医療措置(手術、ストレスなど)によって悪影響を受けます。 免疫系が最初に罹患し、二次免疫不全が起こる 根本的な疾患治療の方法および戦術の絶え間ない改善、ならびに非薬物治療方法の関与によるディープリザーブ薬物の使用にもかかわらず、治療の有効性はかなり低いレベルのままである。 多くの場合、疾患の発症、経過および転帰におけるこれらの特徴の原因は、免疫系に対するある種の違反の患者における存在である。 近年世界中の多くの国で実施された研究は、免疫系における障害のレベルおよび程度を考慮して、指向性作用の免疫向性薬を使用して様々な病理学的形態の疾患の治療および予防に対する新しい臨床アプローチを開発および導入することを可能にした。 再発の予防および疾患の治療、ならびに免疫不全の予防における重要な側面は、基礎療法と合理的な免疫矯正との組み合わせである。 現在、免疫薬理学の緊急の課題の1つは、有効性および使用の安全性などの重要な特性を組み合わせた新薬の開発です。 免疫と免疫システム免疫 - 体の遺伝的恒常性、その構造的、機能的、生化学的完全性および抗原性の個性を保存および維持することを目的とした、外因性および内因性の遺伝的外来物質に対する体の保護。 免疫は進化の過程で生み出されるすべての生物にとって最も重要な特徴の一つです。 防衛メカニズムの運用の原則は、異星人の構造の認識、処理、排除にあります。 防御は、非特異的(先天的、自然)免疫と特異的(後天的)免疫の2つのシステムを利用して行われます。 これらの2つのシステムは、体を保護する単一のプロセスの2つの段階です。 非特異的免疫は防御の最前線としてそしてその最終段階として作用し、そして獲得免疫のシステムは、プロセスの最終段階において外来物質の特異的認識および記憶および強力な先天的免疫ツールの接続の中間機能を果たす。 先天性免疫システムは、炎症や食作用、保護タンパク質(補体、インターフェロン、フィブロネクチンなど)、および細胞や組織を破壊する有害物質、あるいはむしろ有害な物質にのみ反応します。 、この破壊の微粒子製品に。
免疫系の臓器は、一次(中枢)と二次(末梢)に分けられます。 一次(中央)には胸腺とFabriciusバッグが含まれ、鳥にのみ見られます。 ヒトでは、Fabriciusバッグの役割は、リンパ球の幹前駆細胞を供給する骨髄によって行われます。 免疫系の両方の中枢器官はリンパ球集団の分化の場所です。 胸腺はTリンパ球(胸腺依存性リンパ球)を供給し、Bリンパ球は骨髄で形成されます。 末梢リンパ器官には、脾臓、リンパ節、扁桃腺、ならびに腸および気管支に関連するリンパ組織が含まれる。 それらが抗原と接触していないので、誕生時までに、それらはまだ実質的に形成されていない。 リンパ球産生は抗原刺激の存在下でのみ行われる。 免疫系の末梢臓器は、免疫系の中枢臓器からのBリンパ球およびTリンパ球によって占められており、各集団はそれ自身のゾーンに移動する - 胸腺依存性および胸腺非依存性。 これらの臓器内の抗原と接触した後、リンパ球はリサイクルされるので、抗原がリンパ球に気付かれなくなることはありません。 免疫系は感染から体を守り、損傷を受けた、老化しそして遺伝子組み換えされた細胞やそれ自身の体の分子を取り除きます。 免疫システムは、おそらく、身体の最もユニークなシステムの1つであり、自己規制および自治の特性、他のシステムおよび身体の臓器との多数の解剖学的および機能的関連性を有している。 免疫系はリンパ系組織によって表されます。リンパ系組織はほぼすべての臓器や系で多かれ少なかれ表され、一方ではこの系の統合的役割を決定し、他方では様々な有害因子が内因性の場合に起こるその指標的役割を決定します。 そして外因性。 免疫システムは体の最も動的なシステムの1つです、それは敏感で、体の変化に反応する最初のもののうちの1つです、その規制は一連の要因、メカニズム、プロセスを通して直接および逆の関係のシステムで実行されます。 免疫系の機能は、外因性(社会的、環境的、医学的など)と内因性(体性および感染性の疾患、内分泌障害など)に分類することができる十分に多数の要因によって影響を受ける。 これらの要因の影響の結果はシステムの機能的な活動における変化です:システム全体またはその個々のリンクの活性化、あるいはその抑制。 免疫系を阻害または刺激する因子の過度の(持続的かつ強力な)効果は、サイトカインの調節不全、細胞性および体液性免疫系の機能の崩壊、ならびに身体の自然な抵抗性の要因として現れる免疫不全の発症につながる。 二次免疫不全(VID)。免疫系の状態は、他の臓器(心臓、肝臓、肺)と同様に、通常の状態の免疫系に内在する形態学的、機能的および臨床的指標の複合体によって特徴付けられます。 彼らは免疫状態を決定します。 これらの指標の1つ以上の変化は、免疫状態の違反、すなわち基準からの逸脱を示し、免疫不全として解釈されます。 その結果、免疫不全症は、免疫応答の1つまたは複数のメカニズムの欠陥による免疫状態の変化です。 一次(先天性)および二次(後天性)免疫不全症、ならびに免疫系自体が感染因子の標的となる状態(AIDS、T細胞白血病)がある。 二次IDは一次IDよりはるかに一般的であり、免疫システムの最初は正常に機能している個人で形成されます。 二次免疫不全では、免疫系のTおよびB系、ならびに自然の抵抗性因子(食作用、補体、インターフェロンなど)が影響を受ける可能性があり、免疫系の保護機能の低下、免疫系間の規制関係の低下を招く 。 二次的な(獲得された)形態のIDの発生の原因は様々な要因であり得るが、ほとんどの場合これらの形態のIDは関連している:
したがって、外観は、社会的、環境的、医学的、職業的および他の要因の多数が生物に影響を与えるときに発生する可能性があります。 この結果、人口の1人に占めるVIDの数はかなりの数字で表され、個々のチームで80〜90%に達しています。 二次免疫不全症における免疫障害と臨床症状その形式によると、VIEWは次のようになります。
UIDの臨床症状は非常に多様であり、4つの主要な症候群、すなわち感染性、アレルギー性、自己免疫性および免疫増殖性で現れる。 感染症症候群それは、さまざまな病因および局在性の急性および慢性の感染性および炎症性疾患、条件付き病原性微生物によって引き起こされる化膿性 - 炎症性感染症の経過の繰り返しの特徴として現れる。 潜在的に二次免疫不全症の発症につながる可能性がある要因の多様性と罹患率を考えると、彼の人生のすべての人が特定の要因またはそれらの組み合わせの長期的な影響にさらされ、二次免疫不全を発症する本当の危険にさらされていると仮定することは論理的です。 これに関して、特に近年では、すでに生じている免疫不全状態の発症および矯正を防ぐために、合理的な免疫向性効果が本当に必要とされている。 海外でも私たちの国でも登録されており、臨床診療に使用されている免疫調節薬のリストは現在非常に広く、400項目以上にのぼります。 免疫向性薬の主な要件は以下のとおりです。
現在、免疫療法の基本原則が開発され承認されています。
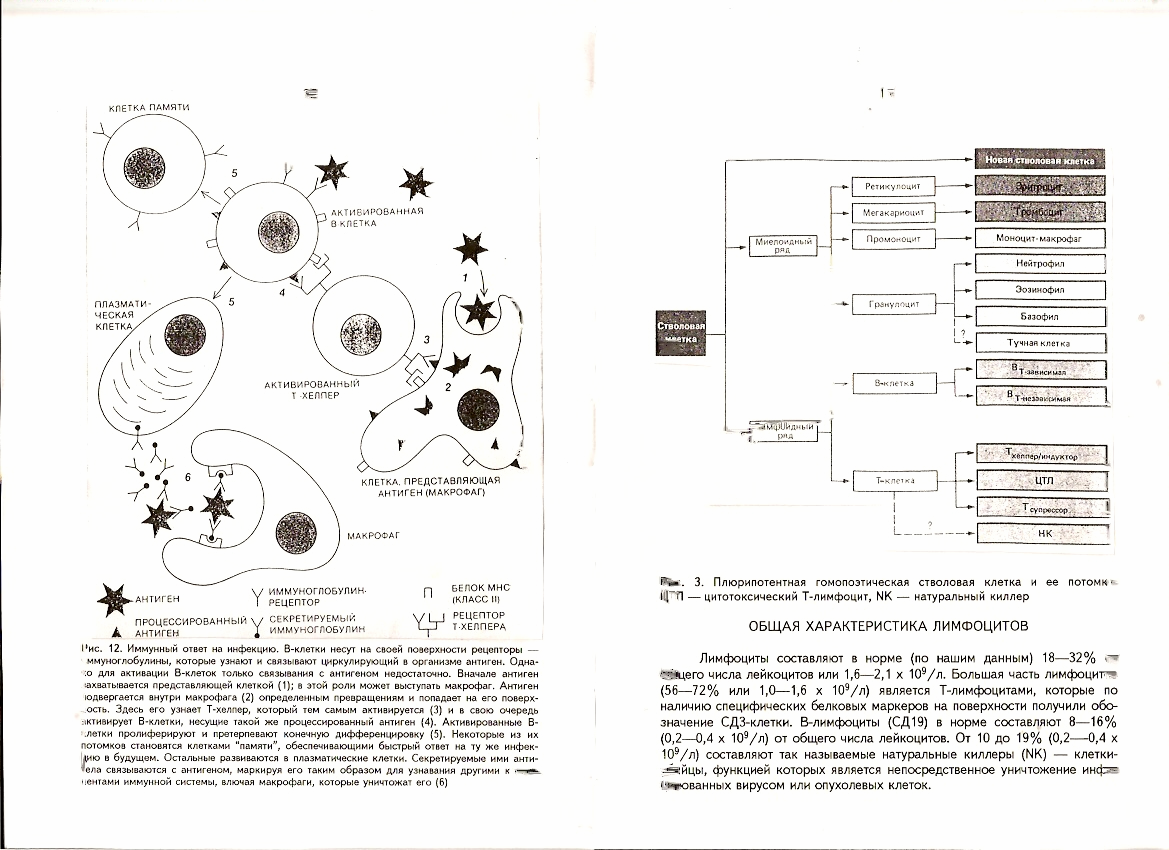
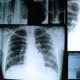
しかしながら、全ての使用されている免疫調節剤が合理的免疫療法および免疫予防の要件および原理に適合しているわけではない。 ロシア医学科学アカデミーの学者によって設計されています。 一次および二次免疫不全の原因および発生メカニズムを考慮して、ベクターおよび免疫系に対する作用の性質、作用機序による免疫調節剤のヴォロビョフ分類は、それぞれの場合において最も効果的なモジュレーターを選択することを可能にする(MZhEI、2002、№4)。 既存の一連の免疫調節剤は、その有効性およびそれらの安全性、使いやすさ、経済性などを決定する他のいくつかの特性において等しくない。 ヒト、動物における免疫過程の調節に関与する物質に基づいている、天然の、天然の、いわゆる内因性免疫調節剤は、人体にとって最も許容されかつ適切である。 内因性免疫調節剤は、インターロイキン、インターフェロン、胸腺のペプチドからの調製物、骨髄および免疫担当細胞を含むことが知られている。 このクラスの免疫調節剤の中で、新薬は現在かなり興味深いものである。 " " 会社 "4Life Research。LC"、アメリカ。 微生物学、ウイルス学および免疫学の学科長MMA。 M.A. セシェノフ、 免疫系は器官、組織、細胞の集まりであり、その働きは身体をさまざまな病気から直接保護し、すでに体内に入っている異物を破壊することを目的としています。 このシステムは感染性病原体(バクテリア、ウイルス、真菌)の邪魔になります。 免疫が失敗すると、感染の可能性が高まり、それはまた、多発性硬化症を含む自己免疫疾患の発生にもつながります。 ヒトの免疫系に侵入する臓器:リンパ腺(結節)、扁桃腺、胸腺(胸腺)、骨髄、脾臓、および腸リンパ系の形成(パイエル板)。 それらは、リンパ節を結ぶ管路からなる複雑な循環システムによって統合されています。 リンパ節- 軟組織のこの形成は、長さ0.2〜1.0 cmの楕円形で、リンパ球を多数含んでいます。 扁桃は咽頭の両側に位置するリンパ組織の小さな塊です。 脾臓は大きなリンパ節に非常に似ている器官です。 脾臓の機能は多様である:それは血液のためのフィルター、そしてその細胞のための貯蔵庫、そしてリンパ球の生産のための場所である。 古くて劣った血球が破壊されるのは脾臓です。 免疫系のこの器官は、胃の近くの左心気膜下の胃にあります。 胸腺(胸腺) 胸骨の後ろにあります。 胸腺のリンパ球は増殖して「学ぶ」。 子供や若い人たちでは、胸腺が活発で、年をとるほど、受動的で臓器が小さくなります。 骨髄は、管状の骨と平らな骨の内側にある柔らかい海綿状の組織です。 骨髄の主な仕事は、白血球、赤血球、血小板といった血球の産生です。 パイエルのパッチ - これは腸壁、より具体的には虫垂(虫垂突起)のリンパ組織の濃度です。 しかしながら、主な役割は、リンパ節を結んでリンパを輸送するダクトからなる循環系によって果たされる。 リンパ液(リンパ液)- それはリンパ管を通って流れる色のない液体です、それは多くのリンパ球を含みます - 白血球は病気から体を保護するのに関与します。 リンパ球は、比喩的に言えば、免疫系の「兵士」であり、それらは外来生物またはそれら自身の罹患細胞(感染、腫瘍など)の破壊に関与している。 最も重要な種類のリンパ球は、Bリンパ球とTリンパ球です。 それらは他の免疫細胞と一緒に働き、異物(感染因子、外来タンパク質など)が体に侵入することを許しません。 ヒト免疫系の発達の最初の段階で、身体はTリンパ球を「教え」、外来タンパク質と身体の正常な(それらの)タンパク質を区別します。 この年齢では胸腺が最も活発であるため、この学習過程は幼児期の胸腺(胸腺)で行われます。 子供が思春期に達すると、胸腺の大きさが小さくなり、活動が喪失します。 興味深い事実:例えば、多発性硬化症のような多くの自己免疫疾患では、患者の免疫系は自身の生物の健康な組織を「認識せず」、それらを異質細胞として扱い、それらを攻撃し破壊し始めます。 人間の免疫システムの役割免疫システム 多細胞生物と共に出現し、それらの生存への助力として発達した。 それは遺伝的に外来の細胞や環境から来る物質に対する体の保護を保証する器官と組織を組み合わせたものです。 免疫系の機能の組織とメカニズムによると、神経系に似ています。 これらのシステムは両方とも、異なるシグナルに応答することができる中枢および末梢器官によって代表され、多数の受容体構造および特異的記憶を有する。 免疫系の中枢器官には、赤い骨髄、末梢 - リンパ節、脾臓、胸腺、扁桃腺、虫垂などがあります。 免疫系の細胞の中で主な場所は白血球です。 彼らの助けを借りて、身体は異物と接触したときに異なる形の免疫応答、例えば特異的抗体の形成を提供することができる。 テキストに間違いを見つけましたか? それを選択し、さらにいくつかの単語を入力し、Ctrl + Enterを押す 免疫研究の歴史現代科学における「免疫」の概念は、ロシアの科学者によって紹介されました。 Mechnikovとドイツの医師P. Ehrlichは、主に感染性の様々な病気との闘いで体の保護反応を研究しました。 この分野での彼らのコラボレーションは1908年にノーベル賞を授与されました。 免疫学の科学への大きな貢献は、フランスの科学者ルイスパスツールの仕事によってもなされました。そして、彼は多くの危険な感染に対する予防接種の方法を開発しました。 「免疫」という言葉はラテン語の「免疫」から来ており、これは「何かからの純粋」を意味します。 当初、免疫系は感染症から私たちを守るだけであると考えられていました。 しかし、20世紀半ばのイギリスの科学者P. Medawarの研究は、免疫が一般的に人体との異質で有害な干渉から保護することを証明しました。 現在、免疫とは、まず第一に感染に対する抵抗性、そして第二に身体からの反応であり、彼にとっては異質のものでありそれからの破壊と除去を目的としたものであり、脅威となっている。 人々が免疫を持っていなければ、彼らは単に存在することができなかったことは明らかであり、そしてそれがまさにその存在であることが病気と闘い成功し老齢まで生きることを可能にしている。 免疫系の働き免疫システムは、人間の進化の長い年月にわたって形成されてきたし、確立されたメカニズムとして機能します。 それは私たちが病気や有害な環境影響と戦うのを助けます。 免疫の仕事には、病的に変化した細胞を破壊するだけでなく、外部から侵入する外来物質、および生物自体の中で形成される崩壊産物の両方を同定し、破壊し、引き出すことが含まれる。 免疫システムは多くの「部外者」を認識することができます。 それらの中にはウイルス、バクテリア、植物または動物起源の有毒物質、原生動物、真菌、アレルゲンがある。 それはまた癌細胞に変わり、それ故に彼ら自身の危険な細胞になった敵の数を意味します。 免疫の主な目的は、侵入に対する保護を提供し、体の内部環境、その生物学的個性の完全性を維持することです。 「部外者」の認識はどうですか? このプロセスは遺伝子レベルで行われます。 事実は、各細胞がこの特定の生物にのみ固有のそれ自身の遺伝情報(これはラベルと呼ぶことができる)を運ぶということです。 体内への浸透または変化を検出したときに分析するのは彼女の免疫システムです。 情報が一致する場合(ラベルが使用可能)、それ自体が一致しない場合(ラベルが存在しない場合)、それは他の人を意味します。 免疫学では、外来物質は抗原と呼ばれます。 免疫システムがそれらを検出すると、防御機構が即座に活性化され、「部外者」に対する闘争が始まります。 そして、それぞれの特定の抗原を破壊するために、体は特定の細胞を作り出し、それらは抗体と呼ばれます。 彼らは鍵をかける鍵のように抗原に接近します。 抗体は抗原に結合してそれを除去するので、体は病気と闘います。 アレルギー反応人間の主な免疫反応のひとつは、アレルゲンに対する体の反応の亢進状態です。 アレルゲンは対応する反応の出現に寄与する物質です。 アレルギーを誘発する内的要因と外的要因を割り当てます。 いくつかの食品(卵、チョコレート、柑橘類)、様々な化学物質(香水、消臭剤)、および薬は、外部アレルゲンに関連しています。 内部アレルゲンはそれ自身の細胞で、通常は性質が変化しています。 たとえば、やけどをすると、死んだ組織は異物と認識され、それらに対する抗体が生成されます。 ミツバチ、マルハナバチおよび他の昆虫の咬傷でも同じ反応が起こり得る。 アレルギーは激しくまたは連続的に発症します。 アレルゲンが初めて身体に作用すると、免疫系はそれに対して過敏性の抗体を産生し蓄積する。 同じアレルゲンが体内に再導入されると、アレルギー反応が起こります。例えば、皮膚の発疹、浮腫、発赤、およびかゆみが現れます。 記事の著者:医学博士、一般開業医Mochalov Pavel Aleksandrovich 「免疫系」の概念は、共通の起源、機能的相互作用および共通の調節機構によって接続された異なる器官および細胞の統一を意味する。 免疫系の主要な細胞であるリンパ球は、他の血液細胞と同様に骨髄の幹細胞から発生します。 集団の1つであるB細胞はここでその発生を終え、そして別のクラスのリンパ球であるT細胞は胸腺(胸腺)においてさらに分化する。 T細胞の分化は2段階で起こります。最初は皮質層で活発に増殖し、次に胸腺ホルモンの作用を受けて髄質で増殖し、微小環境因子がさまざまな亜集団の成熟Tリンパ球に変化します(図3)。 骨髄と胸腺 免疫系の中心的な器官です。 末梢リンパ系臓器には多数の リンパ組織の蓄積 消化管、気道および尿生殖路の粘膜の下に位置する、 リンパ節と脾臓。 最も効果的な免疫応答は末梢リンパ系器官で起こる。 リンパ節は濾過され、体の組織から流れるリンパをモニターし、そして脾臓は血液の細胞学的組成を制御します。 これらの臓器ではT領域とB領域が分離されています。 リンパ組織(扁桃腺、パイエル板、虫垂)は、クラス1dA保護抗体の合成に関与している。 免疫応答の出現に必要な、リンパ球と抗原との相互作用は、リンパ節で起こります。 マクロファージおよび他の提示細胞は必然的にこれに関与している。 図 多能性ホモ造血幹細胞およびその子孫:TSC - 細胞傷害性Tリンパ球、NK - ナチュラルキラー リンパ球の一般的な特徴 正常なリンパ球は(我々のデータによれば)白血球の総数の18〜32%、すなわち1.6〜2.1×10 9 / Lです。 ほとんどのリンパ球(56〜72%または1.0〜1.6×10 9 / l)はTリンパ球であり、これは表面上の特異的タンパク質マーカーの存在によりSDZ細胞と呼ばれてきた。 Bリンパ球(SD19)は通常、白血球総数の8〜16%(0.2〜0.4×10 "/ l)を占めます。10〜19%(0.2〜0.4×10 9 / l) いわゆるナチュラルキラー(NK)を作る - その機能がウイルス感染細胞または腫瘍細胞の直接破壊であるキラー細胞。 リンパ球 - これらは抗体を産生する細胞です。 によると クローン選択 40年前にF. Burnetによって提案された理論は、骨髄内で成熟を完了した各Bリンパ球は、ある特定の特異性の抗体を合成する、すなわちある特定の抗原を認識するようにプログラムされています。 Bリンパ球中で合成された抗体はその細胞膜に結合したままであり、そこでそれらは受容体分子として表面に位置する(約10”の抗体分子が各B細胞の表面上に発現される)。抗体は膜上の抗原に結合する。 リンパ球はただ1つの特異性の抗体を合成するようにプログラムされているので、B細胞によって合成された免疫グロブリンはそれらの元のものと同一になるであろう。 抗原によって認識される抗原性マーカーは比較的小さな分子構造であるため、通常、多くのクローンが1回の感染に反応します。 ウイルスやバクテリアはそれ自身の上に多くの抗原マーカーを持っていますそのような各クローンの複製は2つのタイプの細胞の形成につながります。 免疫細胞 記憶:同じ抗原が摂取されると、それらはより速くそしてより強い応答を提供します(図4)。 図 一次および二次応答。 破傷風トキソイドをウサギに2回投与した。 抗原との繰り返し接触による反応はより速くなり、そしてより高い強度で進行する。 記憶細胞は、ワクチン接種の結果として反復感染後に発生する免疫の原因となります。 選択されたクローンの他の細胞は最終分化を受ける。 それらは大きなサイズに成長し、繁殖を停止しそして抗体を活発に分泌し始める。 そのようなBリンパ球は呼ばれます プラズマセル それらは数日しか生存しないが、それらは異なるクラスに属する、所与の抗原に特異的な多数の抗体を産生することに成功した:IgA、IgM、IgGなど。特定のタイプの微生物に対する獲得免疫は特異的である。 抗体分子自体は外来生物を破壊することはできません。 敵がそれを破壊する他の防御システムを認識できるように、それらはそれを「マーク」するだけです。 その一つが補体系です。 この場合の補体系の活性化は前述のものとは異なり、経路自体は「古典的」と呼ばれる。 この経路に沿った開始は、微生物に結合した抗体がC1-エステラーゼのカスケードの最初の成分に結合して活性化する瞬間に起こり、その作用下でSZ-コンバターゼと呼ばれる酵素活性複合体(C4c 2b)が形成される。 形成されたSZaおよびSzvは、別の方法と同様に作用して、膜侵襲複合体(MAC)を形成し、そして急性の炎症反応を引き起こす。 さらに、抗原 - 抗体複合体は、外来粒子を吸収および消化するマクロファージを引き付ける。 いくつかの抗体を負荷した細菌は食細胞に非常にしっかりと結合する。 近接して配置された3つの抗体は、1つの抗体よりも1000倍強いマクロファージに細菌を引き付けると推定される。 抗体とは何ですか、またそれは抗原をどのように認識しますか? 抗体 抗体は、その化学組成によって、分子量が15万から90万の糖タンパク質に属するプラズマタンパク質であり、既知のタンパク質の中で最も多様なものであり、特定の生物にとって「外来」の抗原と相補対を形成することができる。 免疫グロブリンの構造の研究は、英国の免疫学者R. Porterおよびアメリカの生化学者J. Edelmanによって1959年に行われた実験によって可能になった。R。Porterは抗体、特にIgG、パパインを処理し、免疫グロブリン分子の3つのフラグメントを得た。 抗原と結合する能力。 それゆえ、それらはFabフラグメント(抗原結合フラグメント)と呼ばれた。 第3の断片は結晶化することができ、これに関連してそれをFc断片と命名した(結晶化英語断片断片)。 5
図 抗体分子中のアミノ酸の変動性。 用語「V領域」および「C領域」は、それぞれ可変領域および定常領域を指すために使用される。 「VL」および「CL」はこれらの軽鎖領域の名称であり、そして「VH」および「CH」は重い。 既に述べたように、各抗体分子の組成は、同一対の軽鎖および重鎖を含む。 免疫グロブリン分子は、それぞれ2対の肺(英語の軽鎖 - 軽鎖)および2対の重鎖(英国の重鎖 - 重鎖)、ならびにH鎖を有する。 二量体対:軽鎖および重鎖は、すべての免疫グロブリンの主な構造単位である。 5つのサブクラスの重鎖があり、それは文字μ、Γ、Α、、とそれに対応する5つのクラスの免疫グロブリンM、G、A、E、D、さらに2つのクラスの軽鎖とxで表されます。 アミノ酸配列に起因する重鎖と軽鎖は、可変部分と定常部分から構成され、定常セグメントはドメインと呼ばれるいくつかの相同領域から構成されています(French domeina - region)。 全ての可変領域において、アミノ酸組成の高度の可変性を有する超可変領域もある。 健康な個体の血清は少なくとも10 8の異なるIgを含む。 免疫グロブリンの主な機能は、それが免疫複合体の形成に関与することであり、これはFabフラグメント中の活性中心の存在によって保証される。 さらに、それは補体系の活性化に関与し、Fcフラグメントに対する受容体を有する細胞上に定着することができ、そしてそれによって食作用を増強し、そして抗体に依存する細胞性細胞傷害性にも関与することができる。 ヒトでは、5種類の既知の鎖、したがって5種類のIgクラスが定義されている。 IgGは最も一般的な免疫グロブリンであり、その血清は免疫グロブリンの総数の約5%であり、これは6.9から22g / lである。 抗原導入後のクラスG免疫グロブリンは14日目までに出現する。 IgGは血管壁を貫通するため、体内に存在するIgGの最大50%が存在する間質腔に見られ、さらに胎盤を通過するため、出生後最初の数ヶ月で胎児や新生児に免疫をもたらします。 血清中のIgMは、5量体の形で提示されます。 5つのIgM構造分子が放射状に位置し、Fcフラグメントは円の中心に向けられ、そしてFabフラグメントは外側に向けられる。 このクラスの免疫グロブリンの抗体は免疫の瞬間から2-3日目に産生され、胸腺非依存性抗原はIgMのみを産生し、それは血管床にのみ存在し、胎盤を貫通せず、補体系の強力な活性化剤です。 母親の血清中のIgMの量は0.48 - 2 g / lであり、胎児におけるその存在は子宮内感染を示しています。 IgAは全血清免疫グロブリンの10〜15%しか占めていませんが、分泌型IgA(SIgA)の形で存在する血管外分泌物(唾液、涙、食品ジュース、鼻粘膜の分泌物、人乳)が主です。 人乳中、特に初乳中の大量のSIgAの存在は、新生児の胃腸管および口腔粘膜を様々な抗原から、そしてとりわけ感染症の病原体から保護する。 血清中IgA濃度は0.7 - 0.5 g / lです。 明らかに、IgEの主な機能は、IgAによって形成された「防御線」を突破した感染性物質に対する局所的な急性炎症反応の誘導を通して体の外部粘膜を保護することである。 IgDは非常に少量で血清中に見出され、そして血清免疫グロブリンとしてのその役割は完全には明らかではない。 受容体として、IgDはBリンパ球上にあり、それは成熟細胞と比較して膜上に現れるので、その存在はBリンパ球の成熟の証拠として役立ち得る。 おそらく、IgD-受容体相互作用はリンパ球の活性化および抑制を制御する。 抗体の巨大な多様性の遺伝的基盤はまだ完全には理解されていません。 最も普及しているのはW. Dreyer and F. Burnet(1965)のモデルであり、これは抗体を構成する各ポリペプチドに別々の遺伝子は必要ないと仮定している。 軽鎖および類似の重鎖のV、IおよびC領域を独立してコードし、そして最後に増殖性B細胞の突然変異をコードするわずか数百の遺伝子セグメントの組み合わせの結果として、非常に多様なタンパク質が出現する(図6および7)。 Tリンパ球 免疫反応において重要です。 Bリンパ球とは異なり、それらの分化は胸腺における成熟(訓練)を必要とするが、Bリンパ球に関しては、抗原の提示はリンパ節において起こる。 通常、それらの機能において互いに異なる4つのTリンパ球亜集団がある:Tヘルパー、Tサプレッサー、TインダクターおよびTキラー。 T-キラーは抗原に直接作用し、残りは調節機能を果たします。 Tリンパ球の各亜集団がクローン化される。 抗原依存性分化は、抗原の認識から始まり、抗原と、抗原と相互作用する(すなわち協調する)他の免疫適格細胞の両方に特異的な効果を及ぼし得るリンパ球の形成で終わる。 さらに、ヘルパー、サプレッサーおよび細胞傷害性リンパ球は異なる方法で抗原を認識します。 ヘルパーおよびサプレッサーについては、亜集団はそれら自身の誘導因子を有する。 インターロイキンの影響下で、インデューサ細胞メディエーター、抗原と接触するようになるTリンパ球は増殖し、そしてエフェクター細胞および免疫学的記憶細胞に分化する。 抗原依存性分化の過程において、Tヘルパーはメディエーターを分泌し始め、TキラーBリンパ球が増殖するのを刺激する。 Tキラー CD8マーカーを有する(細胞傷害性リンパ球)。 これらの細胞の主な機能は、変異体、腫瘍細胞、または体の細胞を同定することです。 ウイルスに感染している。 加えて、T-キラーは移植の拒絶反応および多くの自己免疫過程において主導的な役割を果たす。 ナチュラルキラー細胞(NK)とは異なり、これらの細胞は、Bリンパ球と同様に多数の表面受容体をクローン的に発現するので、非常に広い特異性を有する。 それら自身の変化した細胞または移植細胞を発見したT−キラーは抗原依存性分化の段階を経てそして真のキラー、すなわち特異的な細胞傷害性効果を有することができるT−リンパ球に変わる。
図 6.抗体遺伝子は断片的な構成をしています。 それらのセグメントは、互いに距離をおいて(時には有意に)ゲノム内に位置しています。 哺乳動物抗体において、軽鎖は2つのタイプのものである。 タイプlightの軽鎖用マウスには、ほとんどの可変ドメインをコードする2つのVセグメントと4つのCセグメントがあります。 各Cセグメントの開始前に、Jセグメントと呼ばれる短いDNAフラグメントがあります。 Vセグメントに接続できます。 Vセグメントの各Vセグメントは、任意のJ - Cペアに接続できます。タイプχの軽鎖には、数百のVセグメント、4つのJセグメント、1つのCセグメントがあります。 重鎖の遺伝子もまた組織化されているが、さらに断片化されている:VおよびJセグメントに加えて、まだ約20のDセグメントがある。 これら3組のセグメント(軽鎖ƛ、軽鎖χおよび重鎖)は3つの異なる染色体上に位置している。 T細胞受容体遺伝子は抗体の重鎖の遺伝子のように構成されている。
図 χ鎖遺伝子の例を用いた個々の断片からの免疫グロブリン遺伝子の組立て。 まず、ランダムに選択されたセグメントVとJ(この場合はV2とJ2)が接続され、それらの間にあるセグメント(V3、V4とJ1)が「破棄」されます。 次に、V2の始まりからDNAの終わりまでの遺伝子の全長が転写される。 得られたRNAはスプライスされる。 得られたmRNAはタンパク質に翻訳される。 すべてのプロセスは特別な酵素を使って行われます。 細胞溶解の実施は、キラー細胞の特定のタンパク質 - パーフォリン(穿孔)を犠牲にして行われる。 T-キラーは、細胞マーカー(クラス1の主要組織適合遺伝子複合体(MHC)の分子)との複合体でのみ抗原を認識することができ、すべての細胞に存在します(図8)。
図 ウイルス感染細胞の破壊。 ナチュラルキラー細胞(NK)の非特異的破壊メカニズムは抗体の助けを借りて標的に集中することができ、そして抗体依存性細胞傷害(ASCC)が起こる。 細胞傷害性Tリンパ球(CTL)は、MHCクラスIに結合した表面抗原の特異的認識の結果として標的に付着する。 Tヘルパー Tリンパ球の関与なしの大部分の天然抗原免疫応答は行われていない。 これは細胞間協同を必要とし、その初期段階で免疫応答を誘導するために極めて重要である抗原認識プロセスがある。 抗原を認識するTヘルパー細胞は、免疫系の主成分、すなわちB細胞およびこの抗原に特異的な他のT細胞を刺激する。 遊離抗原を認識することができるBリンパ球とは異なり、Tヘルパー細胞は、食細胞膜上でのみ、そして必然的にMHCクラス2と組み合わせて抗原を認識する。これは、MHCシステム遺伝子の産物による免疫応答の遺伝的制御を示唆する。 Tヘルパーによる抗原認識は、体液性免疫応答および細胞形態の免疫応答の増強の両方における中心的プロセスである。 Tインダクタ 特別な細胞群は、ヘルパー細胞およびサプレッサー細胞の抗原依存性分化において重要な役割を果たしており、B細胞には影響を及ぼさないT-インダクターからなる。 Tヘルパーインダクタ(itTx)とTサプレッサインダクタ(ITC)があります。 それらの人も他の人も特定の調停者と彼らの機能を実行します。 抗原認識は、MHCシステムの製品の参加なしに起こる。 従って、T-誘導因子は未処理の抗原提示細胞を用いて抗原に結合することができる。 免責の種類と形態 「獲得免疫」という用語を組み合わせた特定の防御因子は、まず第一に、体の免疫システムと、特定の抗原に完全に反応する能力によって異なります。 比抵抗の原因に応じて、次のものがあります。 天然(種) 免疫。ある種類の動物または人の微生物に対する免疫が他の種の病気を引き起こすことがあるもの(例えば、人間にとって犬のペスト)。 獲得した、 病原体と接触した後の生物の個体発生の過程で形成される。 感染症の結果として獲得された免疫 感染後と呼ばれるワクチン投与後 予防接種後。 獲得免疫は能動的でも受動的でもよい。 能動免疫は、感染性疾患の移入または弱毒化した病原体もしくはワクチンの一部としてのその断片の体内への人工的導入の後に形成される。 結果として、微生物またはそれらの毒素に結合することができる特異的抗体が形成される。 受動免疫 彼の病気や予防接種の後に別の体内で発達した既製の抗体を体内に導入した後に起こる。 例えば、ジフテリア細菌の毒素で免疫された動物の血清は、ヒトの病気を予防します。 一種の受動免疫は 胎盤免疫、 母親からの血液を通して胎児抗体を準備することに関連しています。 これらの中で最も安定しているのは自然免疫であり、最も安定していないのは受動的であり、外来抗体が体から除去されるまで平均15〜20日間持続する。 抗体が向けられている目的に応じて、放出する 抗菌剤および抗毒剤 免疫。 前者の場合、それは様々な微生物に対するものであり、後者の場合はそれらが産生する毒素に対するものである(例えば破傷風およびボツリヌス中毒)。 考慮されている免疫の種類は概略的に表すことができる(図9および10)。
図 9.先天性免疫と獲得免疫を組み合わせた2つのトライアド。
図 先天性免疫と獲得免疫のメカニズム間の相互作用の簡略図。 免疫応答の異なる形態による細胞間協調 体液性応答、細胞性応答、免疫学的記憶、免疫学的寛容性の4種類の免疫応答を区別するのが通例です。 体液性反応 は、エフェクター機能(認識、接着および食作用の誘発、補体の活性化)を実行する特異的抗体(免疫グロブリン)の産生を表す。 細胞性免疫応答 直接または分泌されたメディエーター - リンホカインを通して - のいずれかでそれらの機能を果たす多数の抗原特異的活性Tリンパ球の形成である。 免疫学的記憶- 最初の会合よりも強く抗原(病原体)との2回目の接触に反応する身体の能力です。 免疫寛容、 免疫系がそれ自身の生物の抗原に反応しないときの免疫反応の反対。 すべての場合において、免疫応答は免疫系の様々な種類の細胞、すなわちマクロファージの相互作用の結果です。 TおよびBリンパ球 セル間でやり取りする方法は2つあります。 第1は、マクロファージ、Tヘルパー(MHCクラスIIと組み合わせて思い出す)によって膜に埋め込まれた抗原を直接認識して、対応するBリンパ球およびTリンパ球の相補的受容体に対する抗原の直接作用であり、これはそれぞれの増殖および分化の引き金シグナルとなる クローンタイプ 別の経路はサイトカインと呼ばれる特定の可溶性バイオポリマーによって仲介される。 この場合、活性化マクロファージはモノカインを産生する。 インターロイキン-1 Tヘルパーを刺激する(IL - 1)、そして次にそれらは様々なリンホカインを産生する:インターロイキン-2、3、および他のものは他のTリンパ球およびBリンパ球を刺激する(図11)。 このような細胞間相互作用のメカニズムをさらに詳しく考えてみましょう(図12と13)。 図 様々な形態の免疫応答における細胞間協力。
図 感染に対する免疫反応。 B細胞はその表面に受容体を持っています - 体内を循環する抗原を認識して結合する免疫グロブリン。 しかしながら、B細胞の活性化のためには、抗原に結合するだけでは十分ではない。 最初に、抗原は提示細胞によって捕捉されます(1)。 この役割でマクロファージに作用することができます。 抗原はマクロファージ内部である種の変換にさらされ(2)、その表面に落ちます。 ここで彼はTヘルパーによって認識され、それによって活性化され(8)、次に同じプロセシングされた抗原を有するB細胞を活性化する(4)。 活性化されたB細胞は増殖し、有限の分化を遂げます(5)。 その子孫の中には「記憶」細胞となり、将来的に同じ感染に対する素早い対応を可能にするものがあります。 残りはプラズマ細胞に成長します。 それらが分泌する抗体は抗原に結合するので、それを破壊するであろうマクロファージを含む免疫系の他の成分による認識のためにそれを標識する(6)。
図 ウイルス感染に対する免疫応答。 ウイルスが細胞に侵入すると、ウイルスタンパク質が細胞膜に残ります。 細胞傷害性T細胞は、それらがMHCクラスIタンパク質に隣接している場合、そのような外来分子を特異的に認識し、それが宿主細胞の免疫学的同一性を決定する。 細胞傷害性T細胞が感染細胞を殺す 体液性免疫反応 Bリンパ球からの分化の過程で形成される形質細胞による抗体(免疫グロブリン)の産生です。 抗体は、補体の活性化のための代替経路を誘発したり、食細胞の活性化を妨げたりしない微生物に結合するための特異的なアダプターの役割を果たす。 B細胞は3つの異なるタイプの抗原に反応することができます: 胸腺非依存性の1型抗原、例えば高濃度の細菌性リポ多糖は、Bリンパ球の大部分をポリクローナル(すなわち、非特異的)に活性化することができる。 肺炎球菌多糖類などのいくつかの線状抗原は、特殊化マクロファージの表面に長期間持続し、B細胞を刺激することがあります。 両タイプの胸腺非依存性抗原は1dMしか産生せず、記憶細胞を形成しません。 B細胞の対応する受容体と接触した抗原のほとんどは、それを独立して活性化することができず、担体としてのTヘルパーの助けを必要とする。この種の抗原は胸腺依存性と呼ばれる。 したがって、体液性応答の初期段階は、Tヘルパーによる、またはマクロファージ膜上のBリンパ球による直接的な抗原性エピトープの認識にある。 この認識は、必然的にクラスIIの主要組織適合遺伝子複合体(MHC)の関与によって起こる。 次に、Bリンパ球はそれらの免疫グロブリン受容体に結合する抗原を表し、それはMHCクラスIIと組み合わせてその表面に発現される。 しかし、本格的な体液性応答のためには、B細胞は2回目の投与を受けるべきである 非特異的シグナル 細胞性メディエーターを介して入る活性化:Tヘルパーによって産生されるIL - 1(モノカイン)マクロファージ、BSF - 1mなど。 したがって、特定の体液性応答 - 特定の抗体の合成 - は、3種類の細胞が関与して発生します。 抗原提示マクロファージ、TヘルパーおよびBリンパ球は、後者が2つのシグナルを受け取るはずである。 そうでなければ、他の形の体液性反応が実現される。 対応するTヘルパー細胞の非存在下でBリンパ球が抗原情報を受け取ると、免疫寛容が形成される。 メディエーターシグナル(サイトカイン)のみを受け取ると、非特異的免疫グロブリンの合成が始まります。 Tヘルパーの関与なしに微生物がマクロファージ膜上のエピトープを認識すると、IgMのみが合成される。 Tヘルパーは、マクロファージの膜上のMHCクラスIIと組み合わせて抗原を認識し、それは部分的にプロセシングしてそれをその表面に提示した。 免疫炎症の細胞応答はまた、感染の焦点においてマクロファージを引き付けそして保持するいくつかの因子へのTヘルパーの割り当てを含む。 細胞傷害性リンパ球とも呼ばれるTキラーは、特定の生物のすべての細胞に存在するMHC 1と組み合わせて抗原を認識します。 このタイプのリンパ球の活性化は、活性化Tヘルパーによって産生されるIL-2の影響下で起こる。 T-キラーはまたγ-インターフェロンを産生し、それはマクロファージに対するその効果に加えて、ウイルスの隣接細胞への侵入を制限する能力を有する。 活性化T細胞はインターロイキン−2を分泌し、これは細胞のIL − 2に対する受容体による分裂を刺激する:B−リンパ球およびT−キラーはBSF − 1リンホカインを分泌し、B細胞を活性化し、B細胞増殖因子(BCCrF = 11)および 他のリンホカイン 細胞が成熟するにつれて、増殖刺激リンホカインの効果は弱まる。 恒常性を維持するためのメカニズムとしての自己調節の必要性は、他の亜集団の免疫応答を増強するT細胞、活性がこれらのプロセスを制御不能に保つことである細胞とは対照的に存在することを前提とする。 抑制細胞の誘導物質は、MHCクラスII産物の抗原決定基( - )を有する細胞によって提示される抗原と接触すると活性化される。 抗原特異的、イディオタイプ特異的、および非特異的なサプレッサー細胞が圧縮に関与しており、前者は免疫に使用される抗原に対する免疫応答のみを抑制します。 非特異的サプレッサーは、無関係の抗原に対する免疫応答を抑制するタンパク質因子を分泌します。 抑制細胞は、細胞性応答と体液性応答の両方を抑制することができます。 サプレッサー細胞の活性に関連しているのは免疫学的耐性を維持する現象である。 免疫寛容とは、特定の抗原に対する反応が選択的に欠如していることを意味し、身体自身の構成要素に免疫活性が欠如していることを説明します。 研究が示しているように[f。 免疫学的に未成熟のリンパ系細胞と出生前の期間で相互作用する潜在的抗原は、免疫系が成熟すると将来的にそれらに対する特異的免疫応答を不可能にする。 出生前の期間に一種の「自殺」が起こると考えられています - 自己反応性T細胞の自己排除。 この現象はと呼ばれます クローン欠失 誘導寛容は常に一時的であることが判明し、そしてT細胞はB細胞よりもはるかに容易に寛容になるが、後者は必要な支持なしに免疫応答を生じさせることができない。 一次反応と二次反応の違いが特徴 免疫学的記憶 体液性免疫応答および細胞性免疫応答の両方は、一定の動力学を有し、そして抗原の反復侵入の際に、はるかに速く発達しそして定性的特徴を有する。 体液性タイプの一次免疫応答[抗体合成]にはいくつかの段階がある。 第一段階 - 潜伏期 - は抗原が導入された瞬間から最大4日間持続し、この間に抗原の食作用が起こり、その処理およびTおよびBリンパ球の構造成分の提示、協同的相互作用、Tリンパ球の抗原依存性分化が起こる。 この段階では、Bリンパ球はまだ抗体産生細胞に変わっていないので、特異的抗体は血清中で実際には検出されない。 この段階ではわずかな量の抗サルモネラ抗体しか検出できないことが確立されている[Arkhipov G. S.、Atkenov S. B.、1990](抗体は免疫複合体の分解を促進する特別な物質を加えた後に決定される)。 ) 抗体合成の第2段階は、その力価の「対数」倍増です。この段階で、得られたプラズマ細胞は特異的抗体を合成し、クローン細胞が免疫応答に含まれるのでそれらの力価は24時間ごとに2倍になります。 第三段階、抗体合成の安定化が始まり、この期間は免疫グロブリンの産生と免疫複合体(抗原 - 抗体)の形でのそれらの除去との間の動的平衡によって特徴付けられる。 抗体価の減少が、しかしゼロではない - iminatsii抗原は、第4工程を発生します。 主にYgMに関連する抗体は主に一次免疫応答において合成されることに留意すべきである。 一次免疫応答の終わりになって初めてIgGの合成に切り替わります。 一次免疫応答の重要な特徴は、T-およびB-リンパ球記憶の形成であり、これは体内で数日から数十年持続し、免疫記憶を引き起こす可能性がある。 免疫学的記憶とは、免疫系をこの抗原と再接触させたときに免疫反応を加速および強化する能力です。 二次免疫応答において、抗体力価の潜伏期および対数倍増期はほぼ半分になる。 さらに、IgGは主に合成され、その最大レベルは一次免疫応答中の抗体の最大レベルを有意に超える(図4参照)。 免疫システムの運用改善 免疫システムは体の内部環境の恒常性を調節する強力な要因の1つです。 免疫系の破壊は、感染に対する感受性の急激な増加、腫瘍の可能性の増加、自己免疫過程、血液形成障害、再生、および他の病理学的状態をもたらす。 したがって、免疫状態を評価し、様々な免疫病理学の原因を明らかにし、そして障害を矯正するための方法を見出すための方法の開発は、医師の最も重要な活動である。 免疫病理学的状態の分類にはいくつかの原則があります。 まず第一に、彼らは分かれています 先天性と買収。 最初のものは、免疫適格細胞の増殖および分化の遺伝的に決定された障害によって引き起こされる。 違反は、補体のT、Bシステム、食細胞の活動の欠陥による可能性があります。 先天性欠損症の例は胸腺形成不全症候群です。 遺伝的決定論的免疫不全状態は主に生後1ヶ月の子供に見られ、そのような子供は1歳まで生きることはめったにありません。 急性の免疫病理学的状態は、小児および成人においてはるかに一般的です。 それらは、感染性の病原体、例えば、糖尿病、肥満、アテローム性動脈硬化症における代謝障害の結果、放射線療法および外科手術などのいくつかの治療効果によって引き起こされることがあり、それは加齢の自然の仲間である。 ロシア連邦保健医療社会開発省免疫学研究所は、免疫システムの障害(機能不全)を4つの症候群に分類した、免疫学的欠陥の診断カードを開発しました。 感染症症候群(頻繁かつ再発性の感染症)。 アレルギー症候群 自己免疫症候群 免疫増殖症候群 感染症症候群 免疫系の細胞内で病原体が直接繁殖する結果として起こる。 リンパ球、顆粒球およびマクロファージウイルス、リケッチア、真菌、細菌および原生動物における持続性および増殖はこれらの細胞の破壊またはそれらの機能の侵害を引き起こし得る。 例えば、エイズウイルスはTヘルパーを増殖させてそれらの死を引き起こし、感染性単核球症エプスタイン - バーのウイルスは選択的にBリンパ球に影響を及ぼし、ポリクローナル活性化を引き起こす。 同時に、免疫適格細胞は、微生物の毒素の作用によって破壊され得る。 しかしながら、より頻繁には、免疫不全状態は感染中の免疫調節過程の障害の結果として発症する。 ほとんどの感染症では、Tリンパ球の絶対数の増加が最初に起こります。これは、特異的免疫反応のメカニズムの過剰な増幅を制限することを目的とした正常な免疫調節反応です。 その後、微生物の免疫抑制因子のために、Tリンパ球の含有量が減少し、そしてそれは持続的でありそして後退することができない。 そのような感染後またはワクチン接種後の免疫抑制は、抗原特異的および抗原特異的の両方であり得る。 免疫不全状態の背景に対して、日和見感染症が発症し、それは皮膚、呼吸器粘膜、尿路および胃腸管の日和見微生物によって引き起こされる。 体液性免疫(B-リンク)の主な欠陥では、例えばブドウ球菌および連鎖球菌感染症、および細胞性免疫(T-リンク)、ウイルス感染症(ヘルペス、細胞腫)、カンジダ症、クラミジアなどに違反して細菌感染症が優勢である。 AIDS患者を研究した経験は、免疫不全が様々な悪性腫瘍の可能性を有意に増加させることを示しており、これは抗腫瘍制御の重要性を裏付けています。 免疫系の活性の低下は、T細胞、B細胞またはマクロファージの絶対数の低下と共に観察されることができるだけでなく、それらの誘導された分泌活性の改善の間に明らかにされるそれらの貯蔵能力の減少によっても観察される。 免疫系を研究するための多くの方法があり、それらはすべて非常に複雑です:直接および間接凝集反応、免疫電気泳動、免疫蛍光法、酵素免疫測定法、フローサイトメトリーなど。しかし免疫系の「健康」の総合評価は感染に対するその抵抗によって決定できます。 小さな傷はしのぐべきではありません。 膿疱性皮膚疾患はありません。 鼻水、のどの痛み、気管支炎 - これらの「上気道のカタル」はすべて正常に流れ、新しい微生物の免疫が発達するのに必要な時間で約1〜2週間かかります。 これらの病気を避けることはできませんが、1年に2回を超えず、緩やかな経過をたどるべきです。 免疫系のレベルの単純な指標、その正常な機能は、正常な全血球数、ならびにTリンパ球およびBリンパ球の定量的および機能的特徴を評価する基本試験です。 アレルギー反応 大量の抗原が体内に再注入されたとき、または体の免疫反応性が高すぎるときに起こります。 この場合、免疫反応の刺激は過剰(過敏性)であり、そして重大な組織損傷をもたらし得る。 体の感作を引き起こし、その中でアレルギー反応を引き起こす可能性がある抗原は、呼ばれています アレルゲン アレルギー反応の発症における特定の免疫学的メカニズムの主な役割に応じて、それらは通常4つの主要なタイプに分けられます(患者では、原則として、複合反応があります)。 1型(アナフィラキシー)反応 外部アレルゲンに反応して、形質細胞1Å2の対応するクローンが過剰生産することに関連している:花粉、動物のふけ、または室内の塵に住むダニの排泄物。 気管支、鼻粘膜および結膜の組織に固定された1Åとアレルゲンの接触(細胞内に1Åが固定される)は、アレルギー性炎症のメディエータ(ヒスタミンなど)の放出、平滑筋の減少、毛細血管の拡張を引き起こし、喘息または花粉症の症状を引き起こす 。 ますます重要になるのは食物アレルギーです。 食物アレルゲンと胃腸管の肥満細胞上にある特定の1Åとの接触は、下痢や嘔吐などの局所的アナフィラキシー反応を引き起こす可能性があります。 さらに、メディエータの放出により、腸粘膜の透過性およびアレルゲンの吸収が増加する。 血中に浸透したアレルゲンは、関節に沈着した抗体と複合体を形成し、さまざまな臓器に拡散し、さらに局所的なアナフィラキシー反応を引き起こします。 アレルギー症候群の顕著な遺伝的素因があります:人口の約10%がある程度この病気に苦しんでいます。 抗ヒスタミン薬を使用した治療のために、そして重症の場合 - コルチコステロイド。 II型反応(体液性細胞傷害性)。 それらは抗原 - 体の膜細胞の成分 - に対する抗体、主にIgGの産生に基づいています。 そのような抗原は、細胞の自己抗原および体の組織、ならびに二次的に細胞膜に固定されているアレルゲン、例えば薬物アレルゲンであり得る。 原形質膜上に位置するアレルゲンへの抗体の結合は、活性化マクロファージによる細胞損傷を引き起こし得るが、古典的経路に沿った補体系の活性化によって引き起こされる細胞溶解は、損傷の主なメカニズムである。 抗体依存性細胞傷害(ASCC)もまた、顆粒球、単球およびナチュラルキラー細胞の抗体媒介性攻撃が観察された場合に特定の役割を果たす可能性がある。 細胞毒性の例としては、不適合な血液型の輸血、母親(Rh)と胎児(Rh)の不適合性 - 自己赤血球に対する自己抗体形成中の溶血性貧血(補体の単一膜攻撃複合体で十分)、Hashimtromet甲状腺炎、標本、および赤血球膜複合体の標本があります。 腎糸球体の基底膜に対する抗体の形成における甲状腺とグッドパスチャー症候群。 場合によっては、抗原はアミドピリン、クロルプロマジン、セダムなどの薬です。 膜と接触することにより、それらはハプテンから本格的な抗原に変換され、無顆粒球症、血小板減少性紫斑病、および他の疾患を引き起こす可能性があります。 タイプIIIの反応(免疫複合体の形成)。 III型のアレルギー反応は、抗原 - 抗体免疫複合体によって媒介される。 食細胞の病理学では、それらは破壊されずに長い間体内を循環します。 不溶性複合体は基底膜上の組織に沈着し、急性炎症反応を引き起こす可能性があります。関与する多形核白血球食細胞複合体および組織を損傷するタンパク質分解酵素は破壊された食細胞から放出されます。 さらに、免疫複合体は、血小板凝集を引き起こして微小血栓を形成させ、そして酵素活性アミンを放出させる可能性がある。 高レベルの血清抗体を用いると、抗原が体内に浸透する部位に沈殿物が形成される。 皮膚反応は、多形核浸潤、浮腫および紅斑によって特徴付けられ、3〜8時間後に最大に達する(Arthus反応)。 III型のアレルギー反応の例は、農業従事者の喘息性気管支炎、ハト増殖病、および肺アスペルギルス症である。 アレルゲンの空気摂取により、抗体産生の増加は複合体のサイズの増加をもたらし、それらは排除される。 迅速な回復があります。 そうでなければ、抗原の持続性が慢性感染症によるものであるときに起こります。 抗生物質で治療すると、梅毒やハンセン病などの微生物が死んだときに抗原が激しく放出され、III型の暴力的なアレルギー反応が起こります。 抗原が比較的過剰になると、可溶性の複合体が形成され、それが血管透過性を増して腎糸球体、関節、皮膚、および脈絡叢に沈着する。 遊離複合体によって引き起こされる疾患の例は、大量の外来タンパク質の注射によって引き起こされる血清病、全身性狼瘡における糸球体腎炎、連鎖球菌感染、マラリアなどである。罹患組織の罹患抗原に対する原因物質の免疫学的類似性は極めて重要である。 抗体が自己由来のDNAに対して産生される場合、ループスにおいて。 IV型反応(遅延型過敏反応) 抗原と繰り返し接触した後の遅発性症状だけでなく、他の免疫病理学的メカニズムによっても、最初の3つとは異なります。 この種の反応は、抗原と感作リンパ球との相互作用によって引き起こされ、細胞性免疫機構の不適切な機能の結果として組織損傷を引き起こす。 典型的な遅延型過敏反応(HRT)は、ツベルクリンの導入に応答して可溶性メディエーター(リンホカイン)の強力な放出があり、それが紅斑および丘疹の形成につながり、抗原との接触領域に最大で24時間蓄積するMantoux反応である。 マクロファージとリンパ球。 体が感染に対処できない場合、逆説的な状況が発生します。細菌抗原が露出している膜上のマクロファージは、通常のT-キラーによって破壊されます。 肉芽腫が形成されます。 これは結核やハンセン病で見られます。 天然痘とはしかを伴う皮膚の発疹、単純ヘルペスウイルスによって引き起こされる発熱も、遅延アレルギー反応によって引き起こされる可能性があり、その理由は細胞傷害性T細胞によるウイルス感染細胞の激しい破壊である。 持続性抗原によるGSTの永久的誘導は慢性肉芽腫の形成をもたらす。 自己免疫疾患 自己免疫疾患(反応)の概念には、それ自体の免疫適格細胞または抗体がそれら自身の細胞、組織、細胞オルガネラなどに対して「作用する」場合のそのような疾患が含まれる。自己免疫反応の発症の出発点は体内での自己抗原の形成である。 それらは2つのグループに分けられます。 一次自己抗原または真の自己抗原は、免疫系の形成中に胚形成には存在せず、そして成人状態では免疫適格細胞と接触しない正常ないわゆるトランスバリア組織であり、なぜならそれらは組織学的バリアによって決定されるからである。 これに関して、そのような組織はバリアフリーと呼ばれる。 このような抗原の例は、脳組織、内分泌腺、硝子体および眼の水晶体、生殖細胞である。 免疫系(外傷、炎症)からこれらの抗原を分離する組織血行性の障壁が破壊されると、免疫適格細胞は異物としてそれらを認識し、それは自己免疫応答の可能性を伴う免疫応答の形成を伴う。 そのような自己免疫病変は、アジソン病、若年性糖尿病、抗精子抗体によって引き起こされる不妊症、自己免疫性眼炎と考えられるべきです。 一次とは異なり、二次自己抗原は真実ではありません。 それらは、例えば感染性および非感染性炎症ならびに薬物の使用の場合には、様々な外部および内部環境因子の影響下で身体の細胞および組織の成分から形成される。 二次自己抗原の形成は、自己免疫過程の発症機序における主要な場所の1つを占める。 そのため、やけど、凍傷、電離放射線の影響、変性(組織や細胞の変化)に伴って大量の自己抗原が形成されます。 炎症過程では、通常は利用できない免疫適格細胞(細胞表面構造の改変)である隠れた抗原の「露出」、および複雑な抗原(ウイルス粒子および細胞の構造成分)の形成として起こる。 例えば、ウイルス性肝炎では、ウイルス粒子がその原形質膜内のゲノム(遺伝的装置)に挿入され、最終的に細胞死を引き起こす抗体およびTリンパ球の形成を誘導する。 多数の感染細胞の存在下では、肝臓組織全体が死滅する可能性があり、すなわち肝壊死が発症して患者に深刻な結果をもたらす可能性がある。 場合によっては、反応性が変化した患者では、ペニシリン、ブタジオン、ノバインアミドなどの薬を服用するとAyuantigensが形成されます。 そして、アナルギン、アミドピリン、キニジン、フェノールフタレインなどの薬は、血球のタンパク質に親和性があります。 それらと関連して、それらは抗体合成を引き起こし、続いて貧血、白血球減少症、血小板減少症、すなわち体内のこれら形成された要素の含有量の減少を伴う自己免疫損傷を引き起こす複雑な抗原を形成する。 免疫増殖症候群 - 免疫細胞の増殖が促進された一群の疾患:白血病、リンパ腫および骨髄腫。 悪性転換は、有糸分裂を調節する遺伝子の転座、またはウイルス性癌遺伝子の作用と関連していると考えられており、これらはそのような遺伝子と非常に類似している。 例えば、多くのB細胞腫瘍は、q24バンド中の染色体f上に位置する細胞癌原遺伝子の発現増加によって特徴付けられる。 1q(q32)重鎖遺伝子の隣の第14染色体への相互転座の結果として。 他の転座も可能であるが、抗原認識受容体をコードする遺伝子座は常に影響を受ける。 様々なリンパ性悪性新生物において、腫瘍細胞の成熟は分化の様々な段階で停止する。 多くの場合、腫瘍細胞は、類似の正常細胞の発生を阻害し、そして免疫学的欠陥を引き起こす。 彼らは、血液および骨髄中の芽細胞腫細胞を検出すること、血液および骨髄の写真を変えること、免疫細胞の個々の亜集団の濃度を変えること、さらに臨床症状(骨痛、リンパ節増殖など)によって免疫増殖性疾患を診断する。 免疫増殖性疾患の治療は効果がありません。 最も一般的に使用されている骨髄移植。 文学 1. Vershigora A.E. 免疫学の基礎 - 男:医学、1987年 2. Dolgikh V.T. 免疫病理学の基礎教科書 手当:蜂蜜のために。 大学/ V.T.ドルギク。 オムスクgos.med。 【ロストフ/ D】 オムスク:フェニックス、2007年。 - 319с。 3.ドラニクG.N. 臨床免疫学およびアレルギー学 - M:医療情報機関、2003年。-603年代:Il Jaeger L.臨床免疫学:トランス。 - 男:医学、1986年 免疫システムと免疫病理学の主な形態:Proc。 手当:医学系大学の場合/ V. V. クリモフ、E。 コログリボフ他 VV Klimovによって編集された; Sib.gos.med.un-t。 - ロストフ該当せず;トムスク:2006年フェニックス。 - 221秒。 インターフェロンおよびそれらの誘導物質(分子から薬物まで)/ F. エルショフ、O。 キセレフ RAMS - M:出版グループ "GEOTAR - Media"、2005年。 - 356年代、Il。: 臨床免疫学およびアレルギー学:Proc。 大学院医師のシステムのためのマニュアル/編:AVKaraulovなど。 A.V. Karaulovの編集者の下で-M。:医療情報機関、2002.-650年代:Il 8.臨床免疫学およびアレルギー学(A.V. Karaulov編)。 M.医療情報局、2002年。 - 651 p。 9.医学微生物学、ウイルス学、免疫学:教科書/ L.B. Borisov、AMSmirnova、I.S。Freidlinなど - M。:Medicine、2008 細胞の分子生物学:B 5トン/ B.Albarts et al。 英語 - M。:ミール、1986年。 - 第5巻 Petrov R. 免疫学 - 男:医学、1987年 免疫学のRoyt A.基礎:トランス。 - 男:ミール、1991 13. R.ハイトフ 免疫学:教科書。 CD / R.M.が付いている大学のため ハイトフ - 男:GEOTAR-メディア、2006年。 - 311秒:Ill。+ CD-ROM - アプリケーション:p.247-301。 付録1 末梢血中のリンパ球とその亜集団の数
付録2 サイトカインパラメータ
付録3 体液性免疫のパラメータ 付録4 免疫応答に関与する細胞の主な分化マーカー
- これは一連のリンパ組織と体の器官であり、遺伝的に異質な細胞や外部からや体内に形成された物質から体を保護します。 リンパ系組織を含む免疫系の器官は、個人の生涯を通じて内部環境の恒常性(恒常性)を保護する機能を果たします。 彼らは作り出す 免疫担当細胞まず第一に、免疫過程のそれらを含むリンパ細胞と形質細胞は、遺伝的に異質な情報の兆候を運ぶ、細胞またはその中に侵入した細胞または他の異物の認識と破壊を確実にします。 遺伝的制御は、マクロファージの関与により体内で免疫応答を提供するTリンパ球およびBリンパ球の集団を一緒に機能させることによって行われる。 Tリンパ球およびBリンパ球という用語は1969年に導入されました。 イギリスの免疫学者A. Roit。 免疫システム - それは独立したシステムであり、その概念と用語(免疫システム)は1970年代に登場しました。 免疫系は3つの形態機能的特徴を有する。 1)それは体全体に一般化されています。 2)その細胞は常に血流を循環している。 3)それは各抗原に対する特異的抗体を産生する独自の能力を有する。 主役、免疫系の中心的な「姿」は リンパ球. 理論免疫学はL. Pasteur(19世紀)から1960年代までの長い歴史を持ち、臨床免疫学は1960年代から、免疫システムの解剖学的側面として1970年代半ばまで繁栄し始めました。 全く知られていなかった。 そのため、例えば、リンパ節は最近までリンパ系の臓器に起因していたため、虫垂は無秩序と見なされていました。 最後の20 - 25年の間にのみ、免疫系に入る器官と構造の輪が解剖学的に決定されました。 これは人生そのものによってもたらされた実践的経験によって促進された。 1970年代まで いくつかの外国では、子供の扁桃腺および虫垂の「予防的」除去が広く行われており、手術後数年で、これらの人々は頭頸部および腹部腫瘍の発生率が劇的に増加した。 したがって、1970年代に。 直接的な証拠なしに、口蓋扁桃および虫垂の除去を緊急に禁止した。 口蓋扁桃と虫垂が防御機能を果たす免疫系の器官であることがわかった。 1980年代半ばに。 HIV感染の発症後、免疫適格細胞(Tリンパ球)に選択的に影響を及ぼし、そして免疫不全の発症をもたらす、免疫系の器官を単一の全体に組み立てることが可能であった。 免疫系には臓器が含まれています リンパ組織。 リンパ組織には2つの成分があります: 1) ストロマ - 網状細胞および網状繊維からなる網状支持結合組織。 2)リンパ系列の細胞 : 成熟度の異なるリンパ球、形質細胞、マクロファージなど したがって、網状組織およびリンパ系の細胞は一緒になって免疫系を構成する。 免疫系の臓器には、リンパ系組織が造血に密接に関連している骨髄、胸腺(胸腺)、リンパ節、脾臓、消化器の中空臓器壁のリンパ系組織の蓄積、扁桃腺、群リンパ球プラーク、 単一リンパ結節)。 これらの臓器はしばしばリンパ系臓器、または免疫原性臓器と呼ばれます。 機能的には、免疫系の器官は中枢と末梢に分けられます。 に 中央当局 免疫系には骨髄と胸腺があります。 で 骨髄 多能性幹細胞は、(他の血液細胞と共に)Bリンパ球(buces依存性)およびTリンパ球前駆体を形成する。 で 胸腺 Tリンパ球(胸腺依存性)は分化しており、これはこの臓器によって受容されたTリンパ球の前駆体 - 前駆細胞 - から形成される。 将来的には、免疫系の末梢器官への血流を伴うリンパ球のこれらの集団の両方。 体内に存在するリンパ球のほとんどは、さまざまな生息地の間を循環(繰り返し循環)しています。これらの細胞が形成されている免疫系の臓器、リンパ管、血液、また免疫系の臓器などです。 リンパ球は骨髄および胸腺に再入しないと考えられています。 末梢臓器へ 免疫システムは次のとおりです。 1)扁桃リングN. ピロゴフイン。 Waldeyer; 2)呼吸器系(喉頭、気管、気管支)、消化器系(食道、胃、小腸、虫垂、胆嚢)、尿路系(尿管、膀胱、尿道)の中空器官の壁に多数のリンパ節がある。 3)大網のリンパ球結節(「腹腔の免疫ファクトリー」)、子宮。 4)体細胞性(頭頂)、内臓性(内臓性)、および500から1000の量のリンパ流を通して挿入された混合リンパ節(生物学的フィルター)。 5)脾臓が血液の遺伝的「純度」を制御する唯一の器官である。 6)血液、リンパ、組織中に存在する多数のリンパ球および異物の探索。 骨髄 それは同時に造血器官と免疫系の中枢器官です。 成人の骨髄総質量は約2.5〜3 kgです(体重の4.5〜4.7%)。 それの約半分は赤い骨髄です、残りは黄色です。 赤い骨髄は、平らな骨と短い骨の海綿状物質、長い(管状の)骨の骨端の細胞に位置しています。 それは、発達の異なる段階における間質(網状組織)、造血系(骨髄組織)およびリンパ系(リンパ組織)要素からなる。 それは幹細胞 - すべての血球とリンパ球の前駆体 - を含んでいます。 私たちの保護のために働いているリンパ球の数は6兆(6×10 12細胞)です。 成人の体の質量が平均1500 gであるこの数のリンパ球のうち、残りのリンパ球は免疫系の臓器のリンパ組織(100 g)、赤骨髄(100 g)、およびリンパを含む他の組織(1300 g)にあります。 。 1 mm 3の胸管のリンパ球は2,000から20,000のリンパ球です。 (リンパ節を通過する前に)1 mm 3の末梢リンパに平均200個の細胞が含まれています。 新生児では、リンパ球の総質量は約150 gです。 0.3%が血です。 その後、リンパ球の数は急激に増加するので、6ヶ月から6歳までの子供はすでに650 gの体重があり、15歳までには1250 gまで増加し、この間の血中リンパ球の割合はこれらの細胞の総質量の0.2%です。 免疫システム リンパ球 - これらは移動円形セルで、サイズは8から18ミクロンです。 大部分の循環リンパ球は、直径約8ミクロンの小さなリンパ球です。 約10%は、直径12ミクロンの平均リンパ球です。 直径約18ミクロンの大きなリンパ球(リンパ芽球)が、リンパ節と脾臓の繁殖の中心に見られます。 通常、それらは血液やリンパ液を循環しません。 それは小さなリンパ球が主要な免疫適格細胞です。 中リンパ球は、Bリンパ球の形質細胞への分化の初期段階です。 リンパ球の中で区別されます 3グループ:Tリンパ球(胸腺依存性)、Bリンパ球(気道依存性)およびゼロ. 1) Tリンパ球 骨髄では幹細胞から骨髄に発生します。幹細胞は最初に前駆細胞に分化します。 後者は胸腺(胸腺)に血液と共に移され、そこで成熟しそしてTリンパ球に変わり、そして次に骨髄を迂回してリンパ節に落ち着き、脾臓または血液中を循環し、そこでそれらは50〜70%を占める。 すべてのリンパ球 Tリンパ球にはいくつかの形態(集団)があり、それぞれ特定の機能を果たします。 そのうちの1つ - Tヘルパー(ヘルパー)は、Bリンパ球と相互作用し、それらを抗体を産生する形質細胞に変えます。 もう一つは、過剰な反応とBリンパ球の活動を阻止するT抑制因子(抑制因子)です。 さらに他のもの - T-キラー(キラー)は直接細胞性免疫反応を実行する。 彼らは異星人の細胞と相互作用し、それらを破壊します。 このようにして、T-キラーは腫瘍細胞、外来移植の細胞、突然変異細胞を破壊し、それは遺伝的恒常性を維持します。 2) Bリンパ球 幹細胞は骨髄自体の中で発生します。骨髄は現在工場袋(ブルサ)の類似体と見なされています - 鳥のクロアカル腸壁の壁の細胞凝集体。 Bリンパ球は骨髄から血液に入り、そこで循環リンパ球の20〜30%を占めます。 それから、血液で、免疫系の末梢器官(消化器系、呼吸器系、その他の系の中空器官の壁のリンパ節、リンパ節)の末梢器官のボルゾ依存性ゾーンにコロニーを形成します。ここでエフェクター細胞はそれらから分化します。 5つの異なるクラス:IgA、IgG、IgM、IgE、IgD。 Bリンパ球の主な機能は、体液に入る抗体(唾液、涙、血液、リンパ液、尿など)を作ることによって体液性免疫を作り出すことです。 抗体は抗原に結合し、それによって食細胞がそれらを吸収することが可能になる。 3)ゼロリンパ球 免疫系の臓器では分化しませんが、必要に応じて、それらはBおよびTリンパ球に変換することができます。 それらは血液リンパ球の10-20%を占めます。 形態学的には、Tリンパ球とBリンパ球は光学顕微鏡で区別がつかない細胞です。 しかしながら、Tリンパ球上に存在しない顕微鏡(抗原認識受容体)は、走査型電子顕微鏡においてB細胞上で検出される。 免疫系の器官の個体発生の構造と発達には、3つあります。 法律のグループ。 それらのうちのいくつかは免疫系の全ての器官に特徴的であり、他のものは中枢器官専用であり、そしてさらに他のものは免疫系の末梢器官専用である。 免疫系のすべての臓器の一般的なパターン。 1)免疫系の器官の作用組織(実質)はリンパ組織である。 2)免疫系の全ての器官は胚形成の初期に産まれる。 したがって、骨髄および胸腺は、胚形成の4〜5週、リンパ節および脾臓(5〜6週)、口蓋および咽頭扁桃腺(9〜14週)、虫垂リンパ節および小腸リンパ斑(14〜16週)で産生される。 1週間、内腔臓器の粘膜に1個のリンパ球結節 - 16〜18週など 3)出生時に、免疫系の器官は形態学的に形成され、機能的に成熟しておりそして免疫防御の機能を果たす準備ができている。 そうでなければ、子供が生き残ったと想像するのは難しいでしょう。 したがって、出生時には、幹細胞、骨髄組織、およびリンパ組織を含む赤骨髄がすべての骨髄腔を満たしています。 新生児の胸腺は、子供や青年と同じ相対体重で、体重の0.3%を占めます。 免疫系の多くの末梢臓器(口蓋扁桃、虫垂、小腸、大腸など)では、新生児には、すでに繁殖センターを持つものを含むリンパ結節があります。 そのような小結節の存在は、免疫系の器官におけるリンパ組織の完全な形態学的および機能的成熟を示す。 4)免疫系の器官は、小児期および青年期にそれらの最大の発達(質量、大きさ、リンパ節の数、それらの中に生殖中心の存在)に達する。 すべてのリンパ系臓器は、16歳までには発達のピークに達し、免疫原性臓器にはリンパ系結節が4〜6歳までに達します。 1960年代に扁桃腺と虫垂の「予防的」除去が行われるのはそのためです。 いくつかの国の子供たちでは、手術の数年後にそれぞれの領域に臓器腫瘍が出現しました。 5)免疫系の全ての臓器において、リンパ組織の早期退化(逆発達)ならびに脂肪および線維性結合組織によるその置換が観察される。 20〜25歳までに、全てのリンパ系器官は50〜60歳の人々と同じになる。 免疫システムは、既存の免疫保護システムを破壊するのではなく、その若者から保護されなければなりません。 このように、10 - 15年から始まって、赤骨髄の約半分は、次第に太くて不活性な黄色骨髄に変わります。 同様に、10 - 15年から、胸腺のリンパ組織の量は減少し始め、脂肪組織に置き換わります。 最後の50歳は胸腺質量の88〜89%で、新生児では7%にすぎません。 小児および青年では、免疫系の末梢臓器のリンパ結節数が徐々に減少しています。 結節自体が小さくなると同時に、生殖中心はそれらの中に消えます。 結合組織の増殖により、最小のリンパ節はリンパ管に通行できなくなり、リンパ床から遮断されます。 60歳までに、リンパ虫垂にはほとんど残っていない、それは脂肪で満たされ(子供および青年の600〜800個のリンパ結節から、それらの数は100〜150に減少する)、一緒になって腫瘍数の増加により証明される そして高齢者の他の病気。 同時に、リンパ組織の総質量が体内で減少するにつれて、明らかに、免疫系の器官における質的な代償シフトが起こり、大部分の人々に十分に高いレベルで免疫防御を提供する。 免疫系の中枢器官のパターン(特徴) 1)免疫系の中枢器官は、外部からの影響から十分に保護された場所にあります。 例えば、骨髄は骨髄腔にあり、胸腺は広くて硬い胸骨の後ろの胸腔にあります。 2)骨髄と胸腺の両方が、幹細胞からのリンパ球の分化の場所です。 骨髄において、多能性幹細胞は、Bリンパ球およびプレ胸腺細胞(Tリンパ球の前駆体)を形成することによって複雑な分化を形成し、そして胸腺において、骨髄由来のTリンパ球(胸腺細胞)に血液が供給される。 3)免疫系の中枢器官のリンパ組織は微小環境の独特の環境にあり、他の組織と共生している。 骨髄では、この環境は胸腺では骨髄組織、上皮組織です。 明らかに、骨髄組織またはそれによって分泌される物質の存在は幹細胞の発生に影響を及ぼし、その結果、それらの分化はBリンパ球およびプレトミオサイトの形成に向けられる。 胸腺では、生物学的に活性な物質(ホルモン)が産生されます:チモシン、チモポイエチン、胸腺液性因子、プレトミオサイトの分化はTリンパ球形成の経路をたどります。 胸腺および特殊な扁平上皮体(A.ハッサル体)に存在する上皮網状赤血球、ならびに言及されている生物学的に活性な物質が、胸腺依存性リンパ球を構成する因子である可能性が高い。 免疫系の末梢臓器のパターン 1)免疫系の全ての末梢器官は、異物の体内への可能な導入経路上または体内でのそれらの追跡の途中に位置している。 ここでそれらは一種の境界線、セキュリティゾーンを形成します。 リンパ組織。 従って、扁桃腺はリンパ球環N. Pirogov - V.消化器系と気道への入り口のValdeyer。 消化器系、気道系、尿路系の粘膜のリンパ節、リンパ斑、びまん性リンパ系組織は、これらの臓器の外部環境との境界で覆われています(食物塊、それに微生物が含まれている空気、塵埃、尿)。 生物学的フィルターであるリンパ節は、リンパ系が静脈系に流れる頸部の下部の方向に、臓器および組織からの現在のリンパ管の経路上にあります。 脾臓(血液の免疫制御を行う唯一の臓器)は、大動脈から脾動脈に沿った門脈系への血流の経路上にあります。 これらの免疫原性器官に加えて、血液、リンパ、器官および組織中のリンパ球の大きな軍隊は、体内に入ったまたはその中に形成された遺伝的に外来の物質(死細胞、突然変異細胞、腫瘍細胞)の探索、位置確認、認識および破壊の機能を果たす。 細胞、微生物など) 2)免疫系の末梢器官のリンパ系組織は、抗原効果の大きさおよび期間に応じて、その構造を複雑にして通過する。 4段階 (段階)分化。 第一段階 (びまん性リンパ組織) 中空の内臓の粘膜や他の解剖学的構造(一種の抗原に危険な場所)の外観を考慮する必要があります。 散在性のリンパ系組織。 これらは、上皮層の下の粘膜固有層に位置し、数列の細胞を形成するリンパ球です。 形質細胞とマクロファージもそこにあります。 リンパ系の細胞の粘膜における存在は、外部環境(消化管、呼吸器および尿路)に存在する異物(抗原)に出会い、認識し、中和するための身体の準備状態と見なすことができる。 第二段階 (前結節形成) 免疫系の末梢器官の発達は教育です リンパ系細胞のクラスター。 中空の内臓の粘膜および人体の他の領域(胸膜、腹膜、小血管近く、外分泌腺の厚さなど)では、リンパ球が散在的に散在する代わりに、リンパ球が小さな細胞塊に集まる。 これらのクラスターの中心では、細胞は周辺よりもいくらか密に配置されています。 同様の構造は 節前段階 免疫系の末梢器官の形成。 第三段階 (結節形成) 免疫系の末梢臓器におけるリンパ組織の発達は形成です リンパ結節 - 円形または楕円形のリンパ系の細胞の密集した集積。 かなり明確な輪郭を有するそのようなリンパ系結節のリンパ系組織における存在は、リンパ系細胞の局所的再生のための再生中心を形成するそれらの意欲として、免疫系の器官の高い形態学的成熟度の状態として考えられる。 リンパ結節は出生直前または出生直後に現れる。 第4ステージ (リンパ球の自社生産の確立) リンパ組織の発達、免疫系の器官の最高の分化度はリンパ結節に現れると考えられるべきです 生殖中心(発芽、光中心)。 そのような中心は、抗原性刺激への長期の曝露を伴って小結節内に生じ、一方では強力で多様な環境因子の身体への影響、他方では身体の防御の高い活性を示す。 リンパ節に生殖中心の集中的な出現は、幼児期から始まって、小児において観察される。 したがって、1〜3歳の小児では、小腸壁のリンパ結節の70%以上に生殖中心があります。 免疫系の器官のリンパ組織にとって、リンパ結節の存在は、そのような繁殖の中心があってもなくても特徴的である。 生殖中心のないリンパ結節は、以前は呼ばれていました 原発性リンパ結節 それらはびまん性リンパ組織に直接形成されるからである。 繁殖センターを持つリンパ結節は、と呼ばれます 二次結節 なぜなら、再生の中心は二度目のように見えるからである。 結節自体の形成後。 リンパ球形成の部位の一つである繁殖センターは、かなりの数のリンパ芽球、リンパ球、および有糸分裂分裂細胞を含んでいます。 8〜18歳から始めて、リンパ結節の数と大きさは徐々に減少し、生殖中枢は消失します。 40〜60年後、びまん性リンパ組織がリンパ結節の代わりに残り、それは、年齢と共に、大部分が脂肪組織に置き換わる。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 読む: |
|---|
人気:
血 血液型です。 Rhファクター
|





 第二のそして最も複雑なシステム - 後天的免疫 - はリンパ球の機能、外来の高分子を認識して直接あるいは保護タンパク質分子(抗体)の産生によって反応する血液細胞に基づいています。
第二のそして最も複雑なシステム - 後天的免疫 - はリンパ球の機能、外来の高分子を認識して直接あるいは保護タンパク質分子(抗体)の産生によって反応する血液細胞に基づいています。